+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM Structure of RyR1 + Adenosine | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Calcium ion channel / skeletal muscle / nucleotide / homotetramer / TRANSPORT PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報ATP-gated ion channel activity / positive regulation of sequestering of calcium ion / cyclic nucleotide binding / negative regulation of calcium-mediated signaling / negative regulation of insulin secretion involved in cellular response to glucose stimulus / negative regulation of release of sequestered calcium ion into cytosol / terminal cisterna / neuronal action potential propagation / ryanodine receptor complex / insulin secretion involved in cellular response to glucose stimulus ...ATP-gated ion channel activity / positive regulation of sequestering of calcium ion / cyclic nucleotide binding / negative regulation of calcium-mediated signaling / negative regulation of insulin secretion involved in cellular response to glucose stimulus / negative regulation of release of sequestered calcium ion into cytosol / terminal cisterna / neuronal action potential propagation / ryanodine receptor complex / insulin secretion involved in cellular response to glucose stimulus / ryanodine-sensitive calcium-release channel activity / release of sequestered calcium ion into cytosol by sarcoplasmic reticulum / response to redox state / protein maturation by protein folding / ossification involved in bone maturation / 'de novo' protein folding / negative regulation of heart rate / skin development / FK506 binding / organelle membrane / positive regulation of axon regeneration / cellular response to caffeine / channel regulator activity / outflow tract morphogenesis / intracellularly gated calcium channel activity / glutathione transferase / glutathione transferase activity / smooth muscle contraction / response to vitamin E / toxic substance binding / voltage-gated calcium channel activity / smooth endoplasmic reticulum / regulation of cardiac muscle contraction by regulation of the release of sequestered calcium ion / calcium channel inhibitor activity / skeletal muscle fiber development / striated muscle contraction / regulation of release of sequestered calcium ion into cytosol by sarcoplasmic reticulum / T cell proliferation / Ion homeostasis / release of sequestered calcium ion into cytosol / muscle contraction / regulation of cytosolic calcium ion concentration / calcium channel complex / sarcoplasmic reticulum membrane / glutathione metabolic process / cellular response to calcium ion / sarcoplasmic reticulum / peptidylprolyl isomerase / peptidyl-prolyl cis-trans isomerase activity / calcium-mediated signaling / calcium ion transmembrane transport / response to hydrogen peroxide / calcium channel activity / Stimuli-sensing channels / sarcolemma / Z disc / intracellular calcium ion homeostasis / disordered domain specific binding / positive regulation of cytosolic calcium ion concentration / protein refolding / protein homotetramerization / transmembrane transporter binding / calmodulin binding / signaling receptor binding / calcium ion binding / ATP binding / identical protein binding / membrane / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
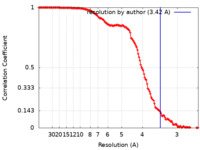
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.42 Å | |||||||||
 データ登録者 データ登録者 | Cholak S / Saville JW / Zhu X / Berezuk AM / Tuttle KS / Haji-Ghassemi O / Van Petegem F / Subramaniam S | |||||||||
| 資金援助 |  カナダ, 2件 カナダ, 2件
| |||||||||
 引用 引用 |  ジャーナル: Structure / 年: 2023 ジャーナル: Structure / 年: 2023タイトル: Allosteric modulation of ryanodine receptor RyR1 by nucleotide derivatives. 著者: Spencer Cholak / James W Saville / Xing Zhu / Alison M Berezuk / Katharine S Tuttle / Omid Haji-Ghassemi / Francisco J Alvarado / Filip Van Petegem / Sriram Subramaniam /   要旨: The coordinated release of Ca from the sarcoplasmic reticulum (SR) is critical for excitation-contraction coupling. This release is facilitated by ryanodine receptors (RyRs) that are embedded in the ...The coordinated release of Ca from the sarcoplasmic reticulum (SR) is critical for excitation-contraction coupling. This release is facilitated by ryanodine receptors (RyRs) that are embedded in the SR membrane. In skeletal muscle, activity of RyR1 is regulated by metabolites such as ATP, which upon binding increase channel open probability (P). To obtain structural insights into the mechanism of RyR1 priming by ATP, we determined several cryo-EM structures of RyR1 bound individually to ATP-γ-S, ADP, AMP, adenosine, adenine, and cAMP. We demonstrate that adenine and adenosine bind RyR1, but AMP is the smallest ATP derivative capable of inducing long-range (>170 Å) structural rearrangements associated with channel activation, establishing a structural basis for key binding site interactions that are the threshold for triggering quaternary structural changes. Our finding that cAMP also induces these structural changes and results in increased channel opening suggests its potential role as an endogenous modulator of RyR1 conductance. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_40426.map.gz emd_40426.map.gz | 121.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-40426-v30.xml emd-40426-v30.xml emd-40426.xml emd-40426.xml | 24.4 KB 24.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_40426_fsc.xml emd_40426_fsc.xml | 13.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_40426.png emd_40426.png | 68.2 KB | ||
| Filedesc metadata |  emd-40426.cif.gz emd-40426.cif.gz | 9.3 KB | ||
| その他 |  emd_40426_half_map_1.map.gz emd_40426_half_map_1.map.gz emd_40426_half_map_2.map.gz emd_40426_half_map_2.map.gz | 226.2 MB 226.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-40426 http://ftp.pdbj.org/pub/emdb/structures/EMD-40426 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-40426 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-40426 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_40426_validation.pdf.gz emd_40426_validation.pdf.gz | 1016.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_40426_full_validation.pdf.gz emd_40426_full_validation.pdf.gz | 1016.1 KB | 表示 | |
| XML形式データ |  emd_40426_validation.xml.gz emd_40426_validation.xml.gz | 22.2 KB | 表示 | |
| CIF形式データ |  emd_40426_validation.cif.gz emd_40426_validation.cif.gz | 29.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-40426 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-40426 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-40426 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-40426 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8serMC  8senC  8seoC  8sepC  8seqC  8sesC  8setC  8seuC  8sevC  8sewC  8sexC  8seyC  8sezC  8sf0C C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_40426.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_40426.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.288 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_40426_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_40426_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : RyR1 in complex with FKBP12.6
| 全体 | 名称: RyR1 in complex with FKBP12.6 |
|---|---|
| 要素 |
|
-超分子 #1: RyR1 in complex with FKBP12.6
| 超分子 | 名称: RyR1 in complex with FKBP12.6 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Ryanodine receptor 1
| 分子 | 名称: Ryanodine receptor 1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 565.908625 KDa |
| 配列 | 文字列: MGDGGEGEDE VQFLRTDDEV VLQCSATVLK EQLKLCLAAE GFGNRLCFLE PTSNAQNVPP DLAICCFTLE QSLSVRALQE MLANTVEAG VESSQGGGHR TLLYGHAILL RHAHSRMYLS CLTTSRSMTD KLAFDVGLQE DATGEACWWT MHPASKQRSE G EKVRVGDD ...文字列: MGDGGEGEDE VQFLRTDDEV VLQCSATVLK EQLKLCLAAE GFGNRLCFLE PTSNAQNVPP DLAICCFTLE QSLSVRALQE MLANTVEAG VESSQGGGHR TLLYGHAILL RHAHSRMYLS CLTTSRSMTD KLAFDVGLQE DATGEACWWT MHPASKQRSE G EKVRVGDD LILVSVSSER YLHLSTASGE LQVDASFMQT LWNMNPICSC CEEGYVTGGH VLRLFHGHMD ECLTISAADS DD QRRLVYY EGGAVCTHAR SLWRLEPLRI SWSGSHLRWG QPLRIRHVTT GRYLALTEDQ GLVVVDACKA HTKATSFCFR VSK EKLDTA PKRDVEGMGP PEIKYGESLC FVQHVASGLW LTYAAPDPKA LRLGVLKKKA ILHQEGHMDD ALFLTRCQQE ESQA ARMIH STAGLYNQFI KGLDSFSGKP RGSGPPAGPA LPIEAVILSL QDLIGYFEPP SEELQHEEKQ SKLRSLRNRQ SLFQE EGML SLVLNCIDRL NVYTTAAHFA EYAGEEAAES WKEIVNLLYE LLASLIRGNR ANCALFSTNL DWVVSKLDRL EASSGI LEV LYCVLIESPE VLNIIQENHI KSIISLLDKH GRNHKVLDVL CSLCVCNGVA VRSNQDLITE NLLPGRELLL QTNLINY VT SIRPNIFVGR AEGSTQYGKW YFEVMVDEVV PFLTAQATHL RVGWALTEGY SPYPGGGEGW GGNGVGDDLY SYGFDGLH L WTGHVARPVT SPGQHLLAPE DVVSCCLDLS VPSISFRING CPVQGVFEAF NLDGLFFPVV SFSAGVKVRF LLGGRHGEF KFLPPPGYAP CHEAVLPRER LRLEPIKEYR REGPRGPHLV GPSRCLSHTD FVPCPVDTVQ IVLPPHLERI REKLAENIHE LWALTRIEQ GWTYGPVRDD NKRLHPCLVN FHSLPEPERN YNLQMSGETL KTLLALGCHV GMADEKAEDN LKKTKLPKTY M MSNGYKPA PLDLSHVRLT PAQTTLVDRL AENGHNVWAR DRVAQGWSYS AVQDIPARRN PRLVPYRLLD EATKRSNRDS LC QAVRTLL GYGYNIEPPD QEPSQVENQS RWDRVRIFRA EKSYTVQSGR WYFEFEAVTT GEMRVGWARP ELRPDVELGA DEL AYVFNG HRGQRWHLGS EPFGRPWQSG DVVGCMIDLT ENTIIFTLNG EVLMSDSGSE TAFREIEIGD GFLPVCSLGP GQVG HLNLG QDVSSLRFFA ICGLQEGFEP FAINMQRPVT TWFSKSLPQF EPVPPEHPHY EVARMDGTVD TPPCLRLAHR TWGSQ NSLV EMLFLRLSLP VQFHQHFRCT AGATPLAPPG LQPPAEDEAR AAEPDPDYEN LRRSAGGWGE AEGGKEGTAK EGTPGG TPQ PGVEAQPVRA ENEKDATTEK NKKRGFLFKA KKAAMMTQPP ATPALPRLPH DVVPADNRDD PEIILNTTTY YYSVRVF AG QEPSCVWVGW VTPDYHQHDM NFDLSKVRAV TVTMGDEQGN VHSSLKCSNC YMVWGGDFVS PGQQGRISHT DLVIGCLV D LATGLMTFTA NGKESNTFFQ VEPNTKLFPA VFVLPTHQNV IQFELGKQKN IMPLSAAMFL SERKNPAPQC PPRLEVQML MPVSWSRMPN HFLQVETRRA GERLGWAVQC QDPLTMMALH IPEENRCMDI LELSERLDLQ RFHSHTLRLY RAVCALGNNR VAHALCSHV DQAQLLHALE DAHLPGPLRA GYYDLLISIH LESACRSRRS MLSEYIVPLT PETRAITLFP PGRKGGNARR H GLPGVGVT TSLRPPHHFS PPCFVAALPA AGVAEAPARL SPAIPLEALR DKALRMLGEA VRDGGQHARD PVGGSVEFQF VP VLKLVST LLVMGIFGDE DVKQILKMIE PEVFTEEEEE EEEEEEEEEE EEEDEEEKEE DEEEEEKEDA EKEEEEAPEG EKE DLEEGL LQMKLPESVK LQMCNLLEYF CDQELQHRVE SLAAFAERYV DKLQANQRSR YALLMRAFTM SAAETARRTR EFRS PPQEQ INMLLHFKDE ADEEDCPLPE DIRQDLQDFH QDLLAHCGIQ LEGEEEEPEE ETSLSSRLRS LLETVRLVKK KEEKP EEEL PAEEKKPQSL QELVSHMVVR WAQEDYVQSP ELVRAMFSLL HRQYDGLGEL LRALPRAYTI SPSSVEDTMS LLECLG QIR SLLIVQMGPQ EENLMIQSIG NIMNNKVFYQ HPNLMRALGM HETVMEVMVN VLGGGETKEI RFPKMVTSCC RFLCYFC RI SRQNQRSMFD HLSYLLENSG IGLGMQGSTP LDVAAASVID NNELALALQE QDLEKVVSYL AGCGLQSCPM LLAKGYPD I GWNPCGGERY LDFLRFAVFV NGESVEENAN VVVRLLIRKP ECFGPALRGE GGSGLLAAIE EAIRISEDPA RDGPGVRRD RRREHFGEEP PEENRVHLGH AIMSFYAALI DLLGRCAPEM HLIQAGKGEA LRIRAILRSL VPLDDLVGII SLPLQIPTLG KDGALVQPK MSASFVPDHK ASMVLFLDRV YGIENQDFLL HVLDVGFLPD MRAAASLDTA TFSTTEMALA LNRYLCLAVL P LITKCAPL FAGTEHRAIM VDSMLHTVYR LSRGRSLTKA QRDVIEDCLM ALCRYIRPSM LQHLLRRLVF DVPILNEFAK MP LKLLTNH YERCWKYYCL PTGWANFGVT SEEELHLTRK LFWGIFDSLA HKKYDQELYR MAMPCLCAIA GALPPDYVDA SYS SKAEKK ATVDAEGNFD PRPVETLNVI IPEKLDSFIN KFAEYTHEKW AFDKIQNNWS YGENVDEELK THPMLRPYKT FSEK DKEIY RWPIKESLKA MIAWEWTIEK AREGEEERTE KKKTRKISQT AQTYDPREGY NPQPPDLSGV TLSRELQAMA EQLAE NYHN TWGRKKKQEL EAKGGGTHPL LVPYDTLTAK EKARDREKAQ ELLKFLQMNG YAVTRGLKDM ELDTSSIEKR FAFGFL QQL LRWMDISQEF IAHLEAVVSS GRVEKSPHEQ EIKFFAKILL PLINQYFTNH CLYFLSTPAK VLGSGGHASN KEKEMIT SL FCKLAALVRH RVSLFGTDAP AVVNCLHILA RSLDARTVMK SGPEIVKAGL RSFFESASED IEKMVENLRL GKVSQART Q VKGVGQNLTY TTVALLPVLT TLFQHIAQHQ FGDDVILDDV QVSCYRTLCS IYSLGTTKNT YVEKLRPALG ECLARLAAA MPVAFLEPQL NEYNACSVYT TKSPRERAIL GLPNSVEEMC PDIPVLDRLM ADIGGLAESG ARYTEMPHVI EITLPMLCSY LPRWWERGP EAPPPALPAG APPPCTAVTS DHLNSLLGNI LRIIVNNLGI DEATWMKRLA VFAQPIVSRA RPELLHSHFI P TIGRLRKR AGKVVAEEEQ LRLEAKAEAE EGELLVRDEF SVLCRDLYAL YPLLIRYVDN NRAHWLTEPN ANAEELFRMV GE IFIYWSK SHNFKREEQN FVVQNEINNM SFLTADSKSK MAKAGDAQSG GSDQERTKKK RRGDRYSVQT SLIVATLKKM LPI GLNMCA PTDQDLIMLA KTRYALKDTD EEVREFLQNN LHLQGKVEGS PSLRWQMALY RGLPGREEDA DDPEKIVRRV QEVS AVLYH LEQTEHPYKS KKAVWHKLLS KQRRRAVVAC FRMTPLYNLP THRACNMFLE SYKAAWILTE DHSFEDRMID DLSKA GEQE EEEEEVEEKK PDPLHQLVLH FSRTALTEKS KLDEDYLYMA YADIMAKSCH LEEGGENGEA EEEEVEVSFE EKEMEK QRL LYQQSRLHTR GAAEMVLQMI SACKGETGAM VSSTLKLGIS ILNGGNAEVQ QKMLDYLKDK KEVGFFQSIQ ALMQTCS VL DLNAFERQNK AEGLGMVNED GTVINRQNGE KVMADDEFTQ DLFRFLQLLC EGHNNDFQNY LRTQTGNTTT INIIICTV D YLLRLQESIS DFYWYYSGKD VIEEQGKRNF SKAMSVAKQV FNSLTEYIQG PCTGNQQSLA HSRLWDAVVG FLHVFAHMM MKLAQDSSQI ELLKELLDLQ KDMVVMLLSL LEGNVVNGMI ARQMVDMLVE SSSNVEMILK FFDMFLKLKD IVGSEAFQDY VTDPRGLIS KKDFQKAMDS QKQFTGPEIQ FLLSCSEADE NEMINFEEFA NRFQEPARDI GFNVAVLLTN LSEHVPHDPR L RNFLELAE SILEYFRPYL GRIEIMGASR RIERIYFEIS ETNRAQWEMP QVKESKRQFI FDVVNEGGEA EKMELFVSFC ED TIFEMQI AAQISEPEGE PEADEDEGMG EAAAEGAEEG AAGAEGAAGT VAAGATARLA AAAARALRGL SYRSLRRRVR RLR RLTARE AATALAALLW AVVARAGAAG AGAAAGALRL LWGSLFGGGL VEGAKKVTVT ELLAGMPDPT SDEVHGEQPA GPGG DADGA GEGEGEGDAA EGDGDEEVAG HEAGPGGAEG VVAVADGGPF RPEGAGGLGD MGDTTPAEPP TPEGSPILKR KLGVD GEEE ELVPEPEPEP EPEPEKADEE NGEKEEVPEA PPEPPKKAPP SPPAKKEEAG GAGMEFWGEL EVQRVKFLNY LSRNFY TLR FLALFLAFAI NFILLFYKVS DSPPGEDDME GSAAGDLAGA GSGGGSGWGS GAGEEAEGDE DENMVYYFLE ESTGYME PA LWCLSLLHTL VAFLCIIGYN CLKVPLVIFK REKELARKLE FDGLYITEQP GDDDVKGQWD RLVLNTPSFP SNYWDKFV K RKVLDKHGDI FGRERIAELL GMDLASLEIT AHNERKPDPP PGLLTWLMSI DVKYQIWKFG VIFTDNSFLY LGWYMVMSL LGHYNNFFFA AHLLDIAMGV KTLRTILSSV THNGKQLVMT VGLLAVVVYL YTVVAFNFFR KFYNKSEDED EPDMKCDDMM TCYLFHMYV GVRAGGGIGD EIEDPAGDEY ELYRVVFDIT FFFFVIVILL AIIQGLIIDA FGELRDQQEQ VKEDMETKCF I CGIGSDYF DTTPHGFETH TLEEHNLANY MFFLMYLINK DETEHTGQES YVWKMYQERC WDFFPAGDCF RKQYEDQLS UniProtKB: Ryanodine receptor 1 |
-分子 #2: Glutathione S-transferase class-mu 26 kDa isozyme,Peptidyl-prolyl...
| 分子 | 名称: Glutathione S-transferase class-mu 26 kDa isozyme,Peptidyl-prolyl cis-trans isomerase FKBP1B タイプ: protein_or_peptide / ID: 2 / コピー数: 4 / 光学異性体: LEVO / EC番号: glutathione transferase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 40.045012 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MKSSHHHHHH GSSMSPILGY WKIKGLVQPT RLLLEYLEEK YEEHLYERDE GDKWRNKKFE LGLEFPNLPY YIDGDVKLTQ SMAIIRYIA DKHNMLGGCP KERAEISMLE GAVLDIRYGV SRIAYSKDFE TLKVDFLSKL PEMLKMFEDR LCHKTYLNGD H VTHPDFML ...文字列: MKSSHHHHHH GSSMSPILGY WKIKGLVQPT RLLLEYLEEK YEEHLYERDE GDKWRNKKFE LGLEFPNLPY YIDGDVKLTQ SMAIIRYIA DKHNMLGGCP KERAEISMLE GAVLDIRYGV SRIAYSKDFE TLKVDFLSKL PEMLKMFEDR LCHKTYLNGD H VTHPDFML YDALDVVLYM DPMCLDAFPK LVCFKKRIEA IPQIDKYLKS SKYIAWPLQG WQATFGGGDH PPKGIEENLY FQ SNAGVEI ETISPGDGRT FPKKGQTCVV HYTGMLQNGK KFDSSRDRNK PFKFRIGKQE VIKGFEEGAA QMSLGQRAKL TCT PDVAYG ATGHPGVIPP NATLIFDVEL LNLE UniProtKB: Glutathione S-transferase class-mu 26 kDa isozyme, Peptidyl-prolyl cis-trans isomerase FKBP1B |
-分子 #3: ADENOSINE
| 分子 | 名称: ADENOSINE / タイプ: ligand / ID: 3 / コピー数: 4 / 式: ADN |
|---|---|
| 分子量 | 理論値: 267.241 Da |
| Chemical component information |  ChemComp-ADN: |
-分子 #4: ZINC ION
| 分子 | 名称: ZINC ION / タイプ: ligand / ID: 4 / コピー数: 4 / 式: ZN |
|---|---|
| 分子量 | 理論値: 65.409 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 支持フィルム - Film thickness: 2 |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 283.15 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 平均電子線量: 40.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 96000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー
























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)