登録情報 データベース : EMDB / ID : EMD-35047タイトル Cryo-EM structure of AfsR-dependent transcription activation complex with afsS promoter 複合体 : Cryo-EM structure of AfsR-dependent transcription activation complex with afsS promoterタンパク質・ペプチド : x 8種DNA : x 2種リガンド : x 2種 / / / 機能・相同性 分子機能 ドメイン・相同性 構成要素
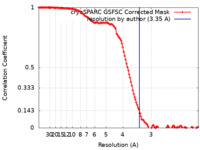
/ / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / / 生物種 Streptomyces coelicolor A3(2) (バクテリア)手法 / / 解像度 : 3.35 Å Wang Y / Zheng J 資金援助 Organization Grant number 国 National Natural Science Foundation of China (NSFC) 31770068, 32070040
ジャーナル : PLoS Biol / 年 : 2024タイトル : Structural and functional characterization of AfsR, an SARP family transcriptional activator of antibiotic biosynthesis in Streptomyces.著者 : Yiqun Wang / Xu Yang / Feng Yu / Zixin Deng / Shuangjun Lin / Jianting Zheng / 要旨 : Streptomyces antibiotic regulatory proteins (SARPs) are widely distributed activators of antibiotic biosynthesis. Streptomyces coelicolor AfsR is an SARP regulator with an additional nucleotide- ... Streptomyces antibiotic regulatory proteins (SARPs) are widely distributed activators of antibiotic biosynthesis. Streptomyces coelicolor AfsR is an SARP regulator with an additional nucleotide-binding oligomerization domain (NOD) and a tetratricopeptide repeat (TPR) domain. Here, we present cryo-electron microscopy (cryo-EM) structures and in vitro assays to demonstrate how the SARP domain activates transcription and how it is modulated by NOD and TPR domains. The structures of transcription initiation complexes (TICs) show that the SARP domain forms a side-by-side dimer to simultaneously engage the afs box overlapping the -35 element and the σHrdB region 4 (R4), resembling a sigma adaptation mechanism. The SARP extensively interacts with the subunits of the RNA polymerase (RNAP) core enzyme including the β-flap tip helix (FTH), the β' zinc-binding domain (ZBD), and the highly flexible C-terminal domain of the α subunit (αCTD). Transcription assays of full-length AfsR and truncated proteins reveal the inhibitory effect of NOD and TPR on SARP transcription activation, which can be eliminated by ATP binding. In vitro phosphorylation hardly affects transcription activation of AfsR, but counteracts the disinhibition of ATP binding. Overall, our results present a detailed molecular view of how AfsR serves to activate transcription. 履歴 登録 2022年12月27日 - ヘッダ(付随情報) 公開 2023年12月27日 - マップ公開 2023年12月27日 - 更新 2024年4月3日 - 現状 2024年4月3日 処理サイト : PDBj / 状態 : 公開
すべて表示 表示を減らす
 データを開く
データを開く 基本情報
基本情報
 マップデータ
マップデータ 試料
試料 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Streptomyces coelicolor A3(2) (バクテリア)
Streptomyces coelicolor A3(2) (バクテリア) データ登録者
データ登録者 中国, 1件
中国, 1件  引用
引用 ジャーナル: PLoS Biol / 年: 2024
ジャーナル: PLoS Biol / 年: 2024
 構造の表示
構造の表示 ダウンロードとリンク
ダウンロードとリンク emd_35047.map.gz
emd_35047.map.gz EMDBマップデータ形式
EMDBマップデータ形式 emd-35047-v30.xml
emd-35047-v30.xml emd-35047.xml
emd-35047.xml EMDBヘッダ
EMDBヘッダ emd_35047_fsc.xml
emd_35047_fsc.xml FSCデータファイル
FSCデータファイル emd_35047.png
emd_35047.png emd_35047_msk_1.map
emd_35047_msk_1.map マスクマップ
マスクマップ emd-35047.cif.gz
emd-35047.cif.gz emd_35047_half_map_1.map.gz
emd_35047_half_map_1.map.gz emd_35047_half_map_2.map.gz
emd_35047_half_map_2.map.gz http://ftp.pdbj.org/pub/emdb/structures/EMD-35047
http://ftp.pdbj.org/pub/emdb/structures/EMD-35047 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-35047
ftp://ftp.pdbj.org/pub/emdb/structures/EMD-35047 emd_35047_validation.pdf.gz
emd_35047_validation.pdf.gz EMDB検証レポート
EMDB検証レポート emd_35047_full_validation.pdf.gz
emd_35047_full_validation.pdf.gz emd_35047_validation.xml.gz
emd_35047_validation.xml.gz emd_35047_validation.cif.gz
emd_35047_validation.cif.gz https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-35047
https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-35047 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-35047
ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-35047 リンク
リンク EMDB (EBI/PDBe) /
EMDB (EBI/PDBe) /  EMDataResource
EMDataResource マップ
マップ ダウンロード / ファイル: emd_35047.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES)
ダウンロード / ファイル: emd_35047.map.gz / 形式: CCP4 / 大きさ: 178 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) emd_35047_msk_1.map
emd_35047_msk_1.map 試料の構成要素
試料の構成要素 解析
解析 試料調製
試料調製 電子顕微鏡法
電子顕微鏡法 FIELD EMISSION GUN
FIELD EMISSION GUN
 画像解析
画像解析
 ムービー
ムービー コントローラー
コントローラー














 Z
Z Y
Y X
X