+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | E.coli phosphoribosylpyrophosphate (PRPP) synthetase type B filament bound with Pi | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報ribose phosphate diphosphokinase complex /  リボースリン酸ジホスホキナーゼ / ribose phosphate diphosphokinase activity / ribonucleoside monophosphate biosynthetic process / 5-phosphoribose 1-diphosphate biosynthetic process / purine nucleotide biosynthetic process / protein hexamerization / リボースリン酸ジホスホキナーゼ / ribose phosphate diphosphokinase activity / ribonucleoside monophosphate biosynthetic process / 5-phosphoribose 1-diphosphate biosynthetic process / purine nucleotide biosynthetic process / protein hexamerization /  phosphate ion binding / phosphate ion binding /  ADP binding / ADP binding /  kinase activity ...ribose phosphate diphosphokinase complex / kinase activity ...ribose phosphate diphosphokinase complex /  リボースリン酸ジホスホキナーゼ / ribose phosphate diphosphokinase activity / ribonucleoside monophosphate biosynthetic process / 5-phosphoribose 1-diphosphate biosynthetic process / purine nucleotide biosynthetic process / protein hexamerization / リボースリン酸ジホスホキナーゼ / ribose phosphate diphosphokinase activity / ribonucleoside monophosphate biosynthetic process / 5-phosphoribose 1-diphosphate biosynthetic process / purine nucleotide biosynthetic process / protein hexamerization /  phosphate ion binding / phosphate ion binding /  ADP binding / ADP binding /  kinase activity / kinase activity /  リン酸化 / magnesium ion binding / リン酸化 / magnesium ion binding /  ATP binding / identical protein binding / ATP binding / identical protein binding /  細胞質基質 / 細胞質基質 /  細胞質 細胞質類似検索 - 分子機能 | |||||||||
| 生物種 |   Escherichia coli str. K-12 substr. MG1655 (大腸菌) Escherichia coli str. K-12 substr. MG1655 (大腸菌) | |||||||||
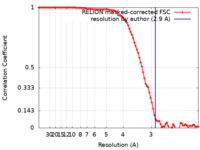
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 2.9 Å クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Hu HH / Lu GM / Chang CC / Liu JL | |||||||||
| 資金援助 |  中国, 2件 中国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2022 ジャーナル: Elife / 年: 2022タイトル: Filamentation modulates allosteric regulation of PRPS. 著者: Huan-Huan Hu / Guang-Ming Lu / Chia-Chun Chang / Yilan Li / Jiale Zhong / Chen-Jun Guo / Xian Zhou / Boqi Yin / Tianyi Zhang / Ji-Long Liu /   要旨: Phosphoribosyl pyrophosphate (PRPP) is a key intermediate in the biosynthesis of purine and pyrimidine nucleotides, histidine, tryptophan, and cofactors NAD and NADP. Abnormal regulation of PRPP ...Phosphoribosyl pyrophosphate (PRPP) is a key intermediate in the biosynthesis of purine and pyrimidine nucleotides, histidine, tryptophan, and cofactors NAD and NADP. Abnormal regulation of PRPP synthase (PRPS) is associated with human disorders, including Arts syndrome, retinal dystrophy, and gouty arthritis. Recent studies have demonstrated that PRPS can form filamentous cytoophidia in eukaryotes. Here, we show that PRPS forms cytoophidia in prokaryotes both in vitro and in vivo. Moreover, we solve two distinct filament structures of PRPS at near-atomic resolution using Cryo-EM. The formation of the two types of filaments is controlled by the binding of different ligands. One filament type is resistant to allosteric inhibition. The structural comparison reveals conformational changes of a regulatory flexible loop, which may regulate the binding of the allosteric inhibitor and the substrate ATP. A noncanonical allosteric AMP/ADP binding site is identified to stabilize the conformation of the regulatory flexible loop. Our findings not only explore a new mechanism of PRPS regulation with structural basis, but also propose an additional layer of cell metabolism through PRPS filamentation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_33309.map.gz emd_33309.map.gz | 40 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-33309-v30.xml emd-33309-v30.xml emd-33309.xml emd-33309.xml | 21.3 KB 21.3 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_33309_fsc.xml emd_33309_fsc.xml | 9.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_33309.png emd_33309.png | 82.7 KB | ||
| マスクデータ |  emd_33309_msk_1.map emd_33309_msk_1.map | 64 MB |  マスクマップ マスクマップ | |
| その他 |  emd_33309_additional_1.map.gz emd_33309_additional_1.map.gz emd_33309_half_map_1.map.gz emd_33309_half_map_1.map.gz emd_33309_half_map_2.map.gz emd_33309_half_map_2.map.gz | 40 MB 49.6 MB 49.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-33309 http://ftp.pdbj.org/pub/emdb/structures/EMD-33309 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-33309 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-33309 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_33309.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_33309.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 1.06 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_33309_msk_1.map emd_33309_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
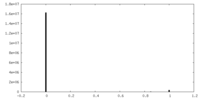
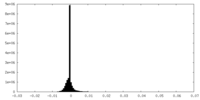
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-追加マップ: C1 symmetry of the type B filament map...
| ファイル | emd_33309_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | C1 symmetry of the type B filament map to show the interface of different hexamers.The mask is not suitable for this map. | ||||||||||||
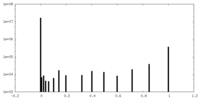
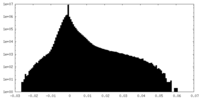
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_33309_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
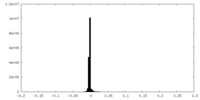
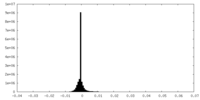
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_33309_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
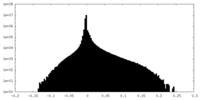
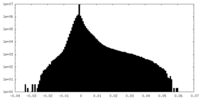
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : E.coli PRPP syhthetase type B filament structure complex with Pi
| 全体 | 名称: E.coli PRPP syhthetase type B filament structure complex with Pi |
|---|---|
| 要素 |
|
-超分子 #1: E.coli PRPP syhthetase type B filament structure complex with Pi
| 超分子 | 名称: E.coli PRPP syhthetase type B filament structure complex with Pi タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Escherichia coli str. K-12 substr. MG1655 (大腸菌) Escherichia coli str. K-12 substr. MG1655 (大腸菌) |
| 組換発現 | 生物種:   Escherichia coli 'BL21-Gold(DE3)pLysS AG' (大腸菌) Escherichia coli 'BL21-Gold(DE3)pLysS AG' (大腸菌) |
-分子 #1: Ribose-phosphate pyrophosphokinase
| 分子 | 名称: Ribose-phosphate pyrophosphokinase / タイプ: protein_or_peptide / ID: 1 / コピー数: 6 / 光学異性体: LEVO / EC番号:  リボースリン酸ジホスホキナーゼ リボースリン酸ジホスホキナーゼ |
|---|---|
| 由来(天然) | 生物種:   Escherichia coli str. K-12 substr. MG1655 (大腸菌) Escherichia coli str. K-12 substr. MG1655 (大腸菌) |
| 分子量 | 理論値: 35.08409 KDa |
| 組換発現 | 生物種:   Escherichia coli 'BL21-Gold(DE3)pLysS AG' (大腸菌) Escherichia coli 'BL21-Gold(DE3)pLysS AG' (大腸菌) |
| 配列 | 文字列: MPDMKLFAGN ATPELAQRIA NRLYTSLGDA AVGRFSDGEV SVQINENVRG GDIFIIQSTC APTNDNLMEL VVMVDALRRA SAGRITAVI PYFGYARQDR RVRSARVPIT AKVVADFLSS VGVDRVLTVD LHAEQIQGFF DVPVDNVFGS PILLEDMLQL N LDNPIVVS ...文字列: MPDMKLFAGN ATPELAQRIA NRLYTSLGDA AVGRFSDGEV SVQINENVRG GDIFIIQSTC APTNDNLMEL VVMVDALRRA SAGRITAVI PYFGYARQDR RVRSARVPIT AKVVADFLSS VGVDRVLTVD LHAEQIQGFF DVPVDNVFGS PILLEDMLQL N LDNPIVVS PDIGGVVRAR AIAKLLNDTD MAIIDKRRPR ANVSQVMHII GDVAGRDCVL VDDMIDTGGT LCKAAEALKE RG AKRVFAY ATHPIFSGNA ANNLRNSVID EVVVCDTIPL SDEIKSLPNV RTLTLSGMLA EAIRRISNEE SISAMFEHHH HHH H |
-分子 #2: PHOSPHATE ION
| 分子 | 名称: PHOSPHATE ION / タイプ: ligand / ID: 2 / コピー数: 12 / 式: PO4 |
|---|---|
| 分子量 | 理論値: 94.971 Da |
| Chemical component information |  ChemComp-PO4: |
-分子 #3: water
| 分子 | 名称: water / タイプ: ligand / ID: 3 / コピー数: 54 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 濃度 | 0.2 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| |||||||||
| グリッド | モデル: UltrAuFoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - トポロジー: CONTINUOUS / 前処理 - タイプ: GLOW DISCHARGE | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV 詳細: blot for 3.5 seconds with blot force of -1 before plunge-freezing. | |||||||||
| 詳細 | The purifide monomer or oligomer protein was incubated with Pi to form this type B filament. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 22500 Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 22500 |
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 撮影したグリッド数: 1 / 実像数: 3131 / 平均露光時間: 4.0 sec. / 平均電子線量: 60.0 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー










 Z
Z Y
Y X
X