+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the human glycosylphosphatidylinositol transamidase complex at 2.53 Angstrom resolution | ||||||||||||||||||
 マップデータ マップデータ | |||||||||||||||||||
 試料 試料 |
| ||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報GPI-anchor transamidase activity / attachment of GPI anchor to protein / GPI-anchor transamidase complex / GPI anchor biosynthetic process / protein retention in ER lumen / Attachment of GPI anchor to uPAR / 加水分解酵素 / regulation of receptor signaling pathway via JAK-STAT / protein disulfide isomerase activity / tubulin binding ...GPI-anchor transamidase activity / attachment of GPI anchor to protein / GPI-anchor transamidase complex / GPI anchor biosynthetic process / protein retention in ER lumen / Attachment of GPI anchor to uPAR / 加水分解酵素 / regulation of receptor signaling pathway via JAK-STAT / protein disulfide isomerase activity / tubulin binding / neuron differentiation / cytoplasmic vesicle / protein-containing complex assembly / neuron apoptotic process / centrosome / endoplasmic reticulum membrane / endoplasmic reticulum / mitochondrion / proteolysis / membrane / plasma membrane / cytosol 類似検索 - 分子機能 | ||||||||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.53 Å | ||||||||||||||||||
 データ登録者 データ登録者 | Xu Y / Li T / Luo Y / Chao Y / Jia G / Zhou Z / Su Z / Qu Q / Li D | ||||||||||||||||||
| 資金援助 |  中国, 5件 中国, 5件
| ||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2022 ジャーナル: Nat Commun / 年: 2022タイトル: Molecular insights into biogenesis of glycosylphosphatidylinositol anchor proteins. 著者: Yidan Xu / Guowen Jia / Tingting Li / Zixuan Zhou / Yitian Luo / Yulin Chao / Juan Bao / Zhaoming Su / Qianhui Qu / Dianfan Li /  要旨: Eukaryotic cells are coated with an abundance of glycosylphosphatidylinositol anchor proteins (GPI-APs) that play crucial roles in fertilization, neurogenesis, and immunity. The removal of a ...Eukaryotic cells are coated with an abundance of glycosylphosphatidylinositol anchor proteins (GPI-APs) that play crucial roles in fertilization, neurogenesis, and immunity. The removal of a hydrophobic signal peptide and covalent attachment of GPI at the new carboxyl terminus are catalyzed by an endoplasmic reticulum membrane GPI transamidase complex (GPI-T) conserved among all eukaryotes. Here, we report the cryo-electron microscopy (cryo-EM) structure of the human GPI-T at a global 2.53-Å resolution, revealing an equimolar heteropentameric assembly. Structure-based mutagenesis suggests a legumain-like mechanism for the recognition and cleavage of proprotein substrates, and an endogenous GPI in the structure defines a composite cavity for the lipid substrate. This elongated active site, stemming from the membrane and spanning an additional ~22-Å space toward the catalytic dyad, is structurally suited for both substrates which feature an amphipathic pattern that matches this geometry. Our work presents an important step towards the mechanistic understanding of GPI-AP biosynthesis. | ||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_32582.map.gz emd_32582.map.gz | 79 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-32582-v30.xml emd-32582-v30.xml emd-32582.xml emd-32582.xml | 28.5 KB 28.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_32582.png emd_32582.png | 82.6 KB | ||
| その他 |  emd_32582_additional_1.map.gz emd_32582_additional_1.map.gz | 42.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-32582 http://ftp.pdbj.org/pub/emdb/structures/EMD-32582 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-32582 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-32582 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_32582_validation.pdf.gz emd_32582_validation.pdf.gz | 505.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_32582_full_validation.pdf.gz emd_32582_full_validation.pdf.gz | 504.7 KB | 表示 | |
| XML形式データ |  emd_32582_validation.xml.gz emd_32582_validation.xml.gz | 6.4 KB | 表示 | |
| CIF形式データ |  emd_32582_validation.cif.gz emd_32582_validation.cif.gz | 7.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-32582 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-32582 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-32582 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-32582 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7wldMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_32582.map.gz / 形式: CCP4 / 大きさ: 83.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_32582.map.gz / 形式: CCP4 / 大きさ: 83.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.85 Å | ||||||||||||||||||||
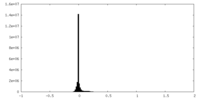
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: unshapened map
| ファイル | emd_32582_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | unshapened map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
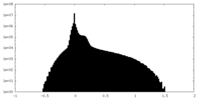
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : GPI transamidase complex
+超分子 #1: GPI transamidase complex
+分子 #1: Glycosylphosphatidylinositol anchor attachment 1 protein
+分子 #2: GPI-anchor transamidase
+分子 #3: GPI transamidase component PIG-S
+分子 #4: GPI transamidase component PIG-T
+分子 #5: Phosphatidylinositol glycan anchor biosynthesis class U protein
+分子 #7: CHOLESTEROL HEMISUCCINATE
+分子 #8: Digitonin
+分子 #9: (4S,7R)-7-[(hexadecanoyloxy)methyl]-4-hydroxy-N,N,N-trimethyl-4,9...
+分子 #10: 1,2-dioleoyl-sn-glycero-3-phosphoethanolamine
+分子 #11: CALCIUM ION
+分子 #12: O-[(R)-{[(2R)-2,3-bis(octadecanoyloxy)propyl]oxy}(hydroxy)phospho...
+分子 #13: 2-acetamido-2-deoxy-beta-D-glucopyranose
+分子 #14: CHOLESTEROL
+分子 #15: 2-azanylethyl [(2~{S},3~{S},4~{S},5~{S},6~{R})-6-(hydroxymethyl)-...
+分子 #16: 2-amino-2-deoxy-alpha-D-glucopyranose
+分子 #17: CARDIOLIPIN
+分子 #18: [(2R)-1-[2-azanylethoxy(oxidanyl)phosphoryl]oxy-3-hexadecanoyloxy...
+分子 #19: [(2~{R})-1-hexadecanoyloxy-3-[[(1~{S},2~{R},3~{R},4~{S},5~{S},6~{...
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 20 mg/mL | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| ||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.026000000000000002 kPa | ||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 53.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.2 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-7wld: |
 ムービー
ムービー コントローラー
コントローラー






 Z
Z Y
Y X
X