+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM map of E.coli FtsH AAA protease | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.2 Å | |||||||||
 データ登録者 データ登録者 | Qiao Z / Gao YG | |||||||||
| 資金援助 |  シンガポール, 1件 シンガポール, 1件
| |||||||||
 引用 引用 |  ジャーナル: Cell Rep / 年: 2022 ジャーナル: Cell Rep / 年: 2022タイトル: Cryo-EM structure of the entire FtsH-HflKC AAA protease complex. 著者: Zhu Qiao / Tatsuhiko Yokoyama / Xin-Fu Yan / Ing Tsyr Beh / Jian Shi / Sandip Basak / Yoshinori Akiyama / Yong-Gui Gao /   要旨: The membrane-bound AAA protease FtsH is the key player controlling protein quality in bacteria. Two single-pass membrane proteins, HflK and HflC, interact with FtsH to modulate its proteolytic ...The membrane-bound AAA protease FtsH is the key player controlling protein quality in bacteria. Two single-pass membrane proteins, HflK and HflC, interact with FtsH to modulate its proteolytic activity. Here, we present structure of the entire FtsH-HflKC complex, comprising 12 copies of both HflK and HflC, all of which interact reciprocally to form a cage, as well as four FtsH hexamers with periplasmic domains and transmembrane helices enclosed inside the cage and cytoplasmic domains situated at the base of the cage. FtsH K61/D62/S63 in the β2-β3 loop in the periplasmic domain directly interact with HflK, contributing to complex formation. Pull-down and in vivo enzymatic activity assays validate the importance of the interacting interface for FtsH-HflKC complex formation. Structural comparison with the substrate-bound human m-AAA protease AFG3L2 offers implications for the HflKC cage in modulating substrate access to FtsH. Together, our findings provide a better understanding of FtsH-type AAA protease holoenzyme assembly and regulation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_32524.map.gz emd_32524.map.gz | 11.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-32524-v30.xml emd-32524-v30.xml emd-32524.xml emd-32524.xml | 9 KB 9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_32524.png emd_32524.png | 36.6 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-32524 http://ftp.pdbj.org/pub/emdb/structures/EMD-32524 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-32524 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-32524 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_32524_validation.pdf.gz emd_32524_validation.pdf.gz | 390.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_32524_full_validation.pdf.gz emd_32524_full_validation.pdf.gz | 390.2 KB | 表示 | |
| XML形式データ |  emd_32524_validation.xml.gz emd_32524_validation.xml.gz | 5.5 KB | 表示 | |
| CIF形式データ |  emd_32524_validation.cif.gz emd_32524_validation.cif.gz | 6.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-32524 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-32524 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-32524 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-32524 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_32524.map.gz / 形式: CCP4 / 大きさ: 15.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_32524.map.gz / 形式: CCP4 / 大きさ: 15.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.3728 Å | ||||||||||||||||||||||||||||||||||||
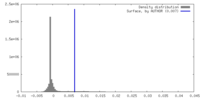
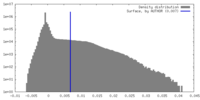
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : FtsH
| 全体 | 名称: FtsH |
|---|---|
| 要素 |
|
-超分子 #1: FtsH
| 超分子 | 名称: FtsH / タイプ: complex / キメラ: Yes / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
-分子 #1: E.Coli FtsH AAA protease
| 分子 | 名称: E.Coli FtsH AAA protease / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MAKNLILWLV IAVVLMSVFQ SFGPSESNGR KVDYSTFLQE VNNDQVREAR INGREINVTK KDSNRYTTY IPVQDPKLLD NLLTKNVKVV GEPPEEPSLL ASIFISWFPM LLLIGVWIFF M RQMQGGGG KGAMSFGKSK ARMLTEDQIK TTFADVAGCD EAKEEVAELV ...文字列: MAKNLILWLV IAVVLMSVFQ SFGPSESNGR KVDYSTFLQE VNNDQVREAR INGREINVTK KDSNRYTTY IPVQDPKLLD NLLTKNVKVV GEPPEEPSLL ASIFISWFPM LLLIGVWIFF M RQMQGGGG KGAMSFGKSK ARMLTEDQIK TTFADVAGCD EAKEEVAELV EYLREPSRFQ KL GGKIPKG VLMVGPPGTG KTLLAKAIAG EAKVPFFTIS GSDFVEMFVG VGASRVRDMF EQA KKAAPC IIFIDEIDAV GRQRGAGLGG GHDEREQTLN QMLVEMDGFE GNEGIIVIAA TNRP DVLDP ALLRPGRFDR QVVVGLPDVR GREQILKVHM RRVPLAPDID AAIIARGTPG FSGAD LANL VNEAALFAAR GNKRVVSMVE FEKAKDKIMM GAERRSMVMT EAQKESTAYH EAGHAI IGR LVPEHDPVHK VTIIPRGRAL GVTFFLPEGD AISASRQKLE SQISTLYGGR LAEEIIY GP EHVSTGASND IKVATNLARN MVTQWGFSEK LGPLLYAEEE GEVFLGRSVA KAKHMSDE T ARIIDQEVKA LIERNYNRAR QLLTDNMDIL HAMKDALMKY ETIDAPQIDD LMARRDVRP PAGWEEPGAS NNSGDNGSPK APRPVDEPRT PNPGNTMSEQ LGDK |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.6 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: OTHER / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.5 µm / 最小 デフォーカス(公称値): 0.5 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 4.2 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 40539 |
|---|---|
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
 ムービー
ムービー コントローラー
コントローラー










 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)