+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of RdrA from Escherichia coli RADAR defense system | |||||||||||||||
 マップデータ マップデータ | E. coli RdrA no split map | |||||||||||||||
 試料 試料 |
| |||||||||||||||
| 機能・相同性 | P-loop containing nucleoside triphosphate hydrolase / Archaeal ATPase 機能・相同性情報 機能・相同性情報 | |||||||||||||||
| 生物種 |   Escherichia coli (大腸菌) Escherichia coli (大腸菌) | |||||||||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 2.52 Å クライオ電子顕微鏡法 / 解像度: 2.52 Å | |||||||||||||||
 データ登録者 データ登録者 | Duncan-Lowey B / Johnson AG / Rawson S / Mayer ML / Kranzusch PJ | |||||||||||||||
| 資金援助 |  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2023 ジャーナル: Cell / 年: 2023タイトル: Cryo-EM structure of the RADAR supramolecular anti-phage defense complex. 著者: Brianna Duncan-Lowey / Nitzan Tal / Alex G Johnson / Shaun Rawson / Megan L Mayer / Shany Doron / Adi Millman / Sarah Melamed / Taya Fedorenko / Assaf Kacen / Alexander Brandis / Tevie ...著者: Brianna Duncan-Lowey / Nitzan Tal / Alex G Johnson / Shaun Rawson / Megan L Mayer / Shany Doron / Adi Millman / Sarah Melamed / Taya Fedorenko / Assaf Kacen / Alexander Brandis / Tevie Mehlman / Gil Amitai / Rotem Sorek / Philip J Kranzusch /   要旨: RADAR is a two-protein bacterial defense system that was reported to defend against phage by "editing" messenger RNA. Here, we determine cryo-EM structures of the RADAR defense complex, revealing ...RADAR is a two-protein bacterial defense system that was reported to defend against phage by "editing" messenger RNA. Here, we determine cryo-EM structures of the RADAR defense complex, revealing RdrA as a heptameric, two-layered AAA+ ATPase and RdrB as a dodecameric, hollow complex with twelve surface-exposed deaminase active sites. RdrA and RdrB join to form a giant assembly up to 10 MDa, with RdrA docked as a funnel over the RdrB active site. Surprisingly, our structures reveal an RdrB active site that targets mononucleotides. We show that RdrB catalyzes ATP-to-ITP conversion in vitro and induces the massive accumulation of inosine mononucleotides during phage infection in vivo, limiting phage replication. Our results define ATP mononucleotide deamination as a determinant of RADAR immunity and reveal supramolecular assembly of a nucleotide-modifying machine as a mechanism of anti-phage defense. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_29323.map.gz emd_29323.map.gz | 259.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-29323-v30.xml emd-29323-v30.xml emd-29323.xml emd-29323.xml | 15.4 KB 15.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_29323.png emd_29323.png | 39.3 KB | ||
| その他 |  emd_29323_half_map_1.map.gz emd_29323_half_map_1.map.gz emd_29323_half_map_2.map.gz emd_29323_half_map_2.map.gz | 254.6 MB 254.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-29323 http://ftp.pdbj.org/pub/emdb/structures/EMD-29323 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29323 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-29323 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_29323.map.gz / 形式: CCP4 / 大きさ: 274.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_29323.map.gz / 形式: CCP4 / 大きさ: 274.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | E. coli RdrA no split map | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.825 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: E. coli RdrA no split half map A
| ファイル | emd_29323_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | E. coli RdrA no split half map A | ||||||||||||
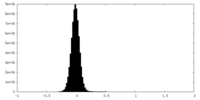
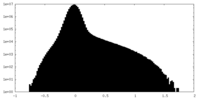
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: E. coli RdrA no split half map B
| ファイル | emd_29323_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | E. coli RdrA no split half map B | ||||||||||||
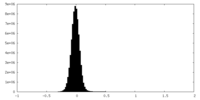
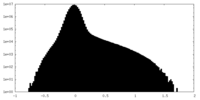
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : E. coli RdrA complex
| 全体 | 名称: E. coli RdrA complex |
|---|---|
| 要素 |
|
-超分子 #1: E. coli RdrA complex
| 超分子 | 名称: E. coli RdrA complex / タイプ: complex / ID: 1 / キメラ: Yes / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
-分子 #1: Archaeal ATPase
| 分子 | 名称: Archaeal ATPase / タイプ: protein_or_peptide / ID: 1 / コピー数: 7 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| 分子量 | 理論値: 107.226594 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| 配列 | 文字列: MTDSVQTETT KGKIIINLFA PNLSGSTKED DLIQKSLRDQ LVESIRNSIA YPDTDKFAGL TRFIDEPGRN VFFVDGTRGA GKTTFINSV VKSLNSDQDD VKVNIKCLPT IDPTKLPRHE PILVTVTARL NKMVSDKLKG YWASNDYRKQ KEQWQNHLAQ L QRGLHLLT ...文字列: MTDSVQTETT KGKIIINLFA PNLSGSTKED DLIQKSLRDQ LVESIRNSIA YPDTDKFAGL TRFIDEPGRN VFFVDGTRGA GKTTFINSV VKSLNSDQDD VKVNIKCLPT IDPTKLPRHE PILVTVTARL NKMVSDKLKG YWASNDYRKQ KEQWQNHLAQ L QRGLHLLT DKEYKPEYFS DALKLDAQLD YSIGGQDLSE IFEELVKRAC EILDCKAILI TFDDIDTQFD AGWDVLESIR KF FNSRKLV VVATGDLRLY SQLIRGKQYE NYSKTLLEQE KESVRLAERG YMVEHLEQQY LLKLFPVQKR IQLKTMLQLV GEK GKAGKE EIKVKTEPSM QDIDAIDVRQ AIGDAVREGL NLREGSDADM YVNELLKQPV RLLMQVLQDF YTKKYHATSV KLDG KQSRN ERPDELSVPN LLRNALYGSM LSNIYRAGLN YEQHRFGMDS LCKDIFTYVK QDRDFNTGFY LRPQSESEAL RNCSI YLAS QVSENCQGSL SKFLQMLLVG CGSVSIFNQF VTELARAEND REKFEQLISE YVAYMSVGRI ESASHWANRC CAVVAN SPN DEKIGVFLGM VQLNRKSRQN MPEGYKKFNI DTENGLAKAA MASSLSTVAS NNLMDFCSVF NLIGAIADIS ACRCERS AI TNAFNKVIAQ TTCIVPPWSE AAVRAEMKGS SKSADNDAAV LDVDLDPKDD GVIDESQQDD ATEFSDAITK VEQWLKNV N EIEIGIRPSA LLIGKVWSRF YFNLNNVADQ HKTRLYRNAE HGRMASQSNA AKIMRFNVLA FLHAVLVEES LYHSVSDRE YIGEGLRLNP VTSVDEFEKK IKIIGEKLKA DNKTWKNTHP LFFLLISCPI LHPFIFPIGG INCSVKALNK ETSFNKLIDE IVGDKLLSD EEWDYLTKNN DQKTNTRQQI FQNTITSLNS STIVGASYDK DTPARKTKSP SLGDSEEK |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 構成要素:
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: OTHER / 撮影モード: OTHER / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 0.5 µm |
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 48.8 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期 角度割当 | タイプ: OTHER |
|---|---|
| 最終 角度割当 | タイプ: OTHER |
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 2.52 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 472729 |
 ムービー
ムービー コントローラー
コントローラー













 Z
Z Y
Y X
X