+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of human Glycine Receptor alpha1-beta heteromer, glycine-bound state 2(expanded open) | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | glycine receptor subunit alpha-1 / glycine receptor subunit beta / Green fluorescent protein / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報taurine binding / glycine-gated chloride channel complex / negative regulation of transmission of nerve impulse / Neurotransmitter receptors and postsynaptic signal transmission / acrosome reaction / positive regulation of acrosome reaction / gamma-aminobutyric acid receptor clustering / postsynaptic specialization / response to alcohol / neuromuscular process controlling posture ...taurine binding / glycine-gated chloride channel complex / negative regulation of transmission of nerve impulse / Neurotransmitter receptors and postsynaptic signal transmission / acrosome reaction / positive regulation of acrosome reaction / gamma-aminobutyric acid receptor clustering / postsynaptic specialization / response to alcohol / neuromuscular process controlling posture / inhibitory synapse / extracellularly glycine-gated ion channel activity / regulation of respiratory gaseous exchange by nervous system process / righting reflex / extracellularly glycine-gated chloride channel activity / synaptic transmission, glycinergic / glycinergic synapse / inhibitory postsynaptic potential / cellular response to ethanol / adult walking behavior / chloride transport / cellular response to zinc ion / neurotransmitter receptor activity / glycine binding / startle response / chloride channel complex / neuronal action potential / transmembrane transporter complex / GABA-ergic synapse / neuropeptide signaling pathway / monoatomic ion transport / muscle contraction / chloride transmembrane transport / ligand-gated monoatomic ion channel activity involved in regulation of presynaptic membrane potential / visual perception / bioluminescence / regulation of membrane potential / generation of precursor metabolites and energy / transmitter-gated monoatomic ion channel activity involved in regulation of postsynaptic membrane potential / cellular response to amino acid stimulus / transmembrane signaling receptor activity / nervous system development / chemical synaptic transmission / postsynaptic membrane / perikaryon / neuron projection / external side of plasma membrane / intracellular membrane-bounded organelle / neuronal cell body / synapse / dendrite / protein-containing complex binding / zinc ion binding / identical protein binding / membrane / plasma membrane / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.9 Å | |||||||||
 データ登録者 データ登録者 | Liu X / Wang W | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: Asymmetric gating of a human hetero-pentameric glycine receptor. 著者: Xiaofen Liu / Weiwei Wang /  要旨: Hetero-pentameric Cys-loop receptors constitute a major type of neurotransmitter receptors that enable signal transmission and processing in the nervous system. Despite intense investigations into ...Hetero-pentameric Cys-loop receptors constitute a major type of neurotransmitter receptors that enable signal transmission and processing in the nervous system. Despite intense investigations into their working mechanism and pharmaceutical potentials, how neurotransmitters activate these receptors remains unclear due to the lack of high-resolution structural information in the activated open state. Here we report near-atomic resolution structures resolved in digitonin consistent with all principle functional states of the human α1β GlyR, which is a major Cys-loop receptor that mediates inhibitory neurotransmission in the central nervous system of adults. Glycine binding induces cooperative and symmetric structural rearrangements in the neurotransmitter-binding extracellular domain but asymmetrical pore dilation in the transmembrane domain. Symmetric response in the extracellular domain is consistent with electrophysiological data showing cooperative glycine activation and contribution from both α1 and β subunits. A set of functionally essential but differentially charged amino acid residues in the transmembrane domain of the α1 and β subunits explains asymmetric activation. These findings provide a foundation for understanding how the gating of the Cys-loop receptor family members diverges to accommodate specific physiological environments. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_27552.map.gz emd_27552.map.gz | 85.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-27552-v30.xml emd-27552-v30.xml emd-27552.xml emd-27552.xml | 20.5 KB 20.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_27552.png emd_27552.png | 108.6 KB | ||
| Filedesc metadata |  emd-27552.cif.gz emd-27552.cif.gz | 7 KB | ||
| その他 |  emd_27552_half_map_1.map.gz emd_27552_half_map_1.map.gz emd_27552_half_map_2.map.gz emd_27552_half_map_2.map.gz | 84.7 MB 84.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-27552 http://ftp.pdbj.org/pub/emdb/structures/EMD-27552 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27552 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-27552 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_27552.map.gz / 形式: CCP4 / 大きさ: 91.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_27552.map.gz / 形式: CCP4 / 大きさ: 91.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.83 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_27552_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
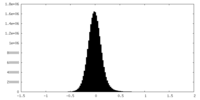
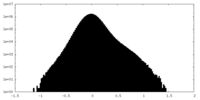
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_27552_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
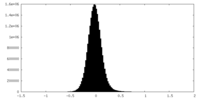
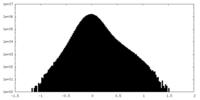
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : heteromeric glycine receptor subunit alpha-1 and beta, glycine-bo...
+超分子 #1: heteromeric glycine receptor subunit alpha-1 and beta, glycine-bo...
+分子 #1: Glycine receptor subunit alpha-1
+分子 #2: Glycine receptor subunit beta,Green fluorescent protein,Glycine r...
+分子 #3: 2-acetamido-2-deoxy-beta-D-glucopyranose
+分子 #4: HEXANE
+分子 #5: HEPTANE
+分子 #6: UNDECANE
+分子 #7: N-OCTANE
+分子 #8: GLYCINE
+分子 #9: nonane
+分子 #10: N-BUTANE
+分子 #11: DECANE
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 6 mg/mL | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| ||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 支持フィルム - 材質: GOLD / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE | ||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 69.6 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 試料ステージ | 試料ホルダーモデル: GATAN LIQUID NITROGEN / ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: PDB ENTRY PDBモデル - PDB ID: |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / 解像度のタイプ: BY AUTHOR / 解像度: 3.9 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 24487 |
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
 ムービー
ムービー コントローラー
コントローラー














 Z
Z Y
Y X
X