+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | SfSTING with cGAMP (masked) | ||||||||||||||||||||||||||||||||||||
 マップデータ マップデータ | SfSTING with cGAMP (masked) sharpened map | ||||||||||||||||||||||||||||||||||||
 試料 試料 |
| ||||||||||||||||||||||||||||||||||||
 キーワード キーワード | STING / bacterial / filament / ANTIVIRAL PROTEIN | ||||||||||||||||||||||||||||||||||||
| 機能・相同性 | Prokaryotic STING domain / Prokaryotic STING domain / CD-NTase-associated protein 12/Pycsar effector protein, TIR domain / CAP12/Pycsar effector protein, TIR domain / NAD+ glycohydrolase / NAD+ nucleosidase activity / defense response to virus / nucleotide binding / CD-NTase-associated protein 12 機能・相同性情報 機能・相同性情報 | ||||||||||||||||||||||||||||||||||||
| 生物種 |  Sphingobacterium faecium (バクテリア) Sphingobacterium faecium (バクテリア) | ||||||||||||||||||||||||||||||||||||
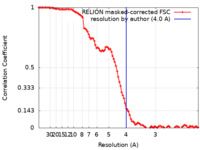
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.0 Å | ||||||||||||||||||||||||||||||||||||
 データ登録者 データ登録者 | Morehouse BR / Yip MCJ / Keszei AFA / McNamara-Bordewick NK / Shao S / Kranzusch PJ | ||||||||||||||||||||||||||||||||||||
| 資金援助 |  米国, 11件 米国, 11件
| ||||||||||||||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2022 ジャーナル: Nature / 年: 2022タイトル: Cryo-EM structure of an active bacterial TIR-STING filament complex. 著者: Benjamin R Morehouse / Matthew C J Yip / Alexander F A Keszei / Nora K McNamara-Bordewick / Sichen Shao / Philip J Kranzusch /  要旨: Stimulator of interferon genes (STING) is an antiviral signalling protein that is broadly conserved in both innate immunity in animals and phage defence in prokaryotes. Activation of STING requires ...Stimulator of interferon genes (STING) is an antiviral signalling protein that is broadly conserved in both innate immunity in animals and phage defence in prokaryotes. Activation of STING requires its assembly into an oligomeric filament structure through binding of a cyclic dinucleotide, but the molecular basis of STING filament assembly and extension remains unknown. Here we use cryogenic electron microscopy to determine the structure of the active Toll/interleukin-1 receptor (TIR)-STING filament complex from a Sphingobacterium faecium cyclic-oligonucleotide-based antiphage signalling system (CBASS) defence operon. Bacterial TIR-STING filament formation is driven by STING interfaces that become exposed on high-affinity recognition of the cognate cyclic dinucleotide signal c-di-GMP. Repeating dimeric STING units stack laterally head-to-head through surface interfaces, which are also essential for human STING tetramer formation and downstream immune signalling in mammals. The active bacterial TIR-STING structure reveals further cross-filament contacts that brace the assembly and coordinate packing of the associated TIR NADase effector domains at the base of the filament to drive NAD hydrolysis. STING interface and cross-filament contacts are essential for cell growth arrest in vivo and reveal a stepwise mechanism of activation whereby STING filament assembly is required for subsequent effector activation. Our results define the structural basis of STING filament formation in prokaryotic antiviral signalling. | ||||||||||||||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_26618.map.gz emd_26618.map.gz | 7.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-26618-v30.xml emd-26618-v30.xml emd-26618.xml emd-26618.xml | 18.4 KB 18.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_26618_fsc.xml emd_26618_fsc.xml | 10 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_26618.png emd_26618.png | 119.1 KB | ||
| Filedesc metadata |  emd-26618.cif.gz emd-26618.cif.gz | 5.8 KB | ||
| その他 |  emd_26618_additional_1.map.gz emd_26618_additional_1.map.gz emd_26618_half_map_1.map.gz emd_26618_half_map_1.map.gz emd_26618_half_map_2.map.gz emd_26618_half_map_2.map.gz | 65.3 MB 65.3 MB 65.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-26618 http://ftp.pdbj.org/pub/emdb/structures/EMD-26618 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-26618 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-26618 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_26618_validation.pdf.gz emd_26618_validation.pdf.gz | 817 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_26618_full_validation.pdf.gz emd_26618_full_validation.pdf.gz | 816.6 KB | 表示 | |
| XML形式データ |  emd_26618_validation.xml.gz emd_26618_validation.xml.gz | 17.1 KB | 表示 | |
| CIF形式データ |  emd_26618_validation.cif.gz emd_26618_validation.cif.gz | 22.3 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-26618 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-26618 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-26618 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-26618 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7unaMC  7un8C  7un9C M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_26618.map.gz / 形式: CCP4 / 大きさ: 83.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_26618.map.gz / 形式: CCP4 / 大きさ: 83.7 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | SfSTING with cGAMP (masked) sharpened map | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.1 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: SfSTING with cGAMP (masked) unsharpened map
| ファイル | emd_26618_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | SfSTING with cGAMP (masked) unsharpened map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: SfSTING with cGAMP (masked) half map 1
| ファイル | emd_26618_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | SfSTING with cGAMP (masked) half map 1 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: SfSTING with cGAMP (masked) half map 2
| ファイル | emd_26618_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | SfSTING with cGAMP (masked) half map 2 | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : SfSTING with cGAMP
| 全体 | 名称: SfSTING with cGAMP |
|---|---|
| 要素 |
|
-超分子 #1: SfSTING with cGAMP
| 超分子 | 名称: SfSTING with cGAMP / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Sphingobacterium faecium (バクテリア) Sphingobacterium faecium (バクテリア) |
-分子 #1: CD-NTase-associated protein 12
| 分子 | 名称: CD-NTase-associated protein 12 / タイプ: protein_or_peptide / ID: 1 / コピー数: 8 / 光学異性体: LEVO / EC番号: NAD+ glycohydrolase |
|---|---|
| 由来(天然) | 生物種:  Sphingobacterium faecium (バクテリア) Sphingobacterium faecium (バクテリア) |
| 分子量 | 理論値: 36.956051 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MHHHHHHGSK KRIFIGSSSE QLTILNEIVD LLGDDVECIP WTDAFALNKS GLDSLIKQTR LADYSILIAT KDDLTKQRGE SLTKPRDNV VFEFGLFLGA AGPEKCYLIA EEDTDLPTDL DGITVAKFTR NSGQYNSLDK IVESIRTHLV KIAEMSQLGL L PSTALAIG ...文字列: MHHHHHHGSK KRIFIGSSSE QLTILNEIVD LLGDDVECIP WTDAFALNKS GLDSLIKQTR LADYSILIAT KDDLTKQRGE SLTKPRDNV VFEFGLFLGA AGPEKCYLIA EEDTDLPTDL DGITVAKFTR NSGQYNSLDK IVESIRTHLV KIAEMSQLGL L PSTALAIG YYNSFIKRVC EEIHGSECVE LEGKKIKVKS FRVDVVIPET LDDNGVGNFT TLYNKRYGLS KATTCTNPAL LG TRGFPFH FKVDPPDANQ ESPVDIHLLD IPSTLSTIVE SLKLYLPSNQ VGQDFDMDYL EMRELENFAK VLKYLIGRNA ATK GYVNVL TNVKL UniProtKB: CD-NTase-associated protein 12 |
-分子 #2: 2-amino-9-[(2R,3R,3aS,5R,7aR,9R,10R,10aS,12R,14aR)-9-(6-amino-9H-...
| 分子 | 名称: 2-amino-9-[(2R,3R,3aS,5R,7aR,9R,10R,10aS,12R,14aR)-9-(6-amino-9H-purin-9-yl)-3,5,10,12-tetrahydroxy-5,12-dioxidooctahydro-2H,7H-difuro[3,2-d:3',2'-j][1,3,7,9,2,8]tetraoxadiphosphacyclododecin- ...名称: 2-amino-9-[(2R,3R,3aS,5R,7aR,9R,10R,10aS,12R,14aR)-9-(6-amino-9H-purin-9-yl)-3,5,10,12-tetrahydroxy-5,12-dioxidooctahydro-2H,7H-difuro[3,2-d:3',2'-j][1,3,7,9,2,8]tetraoxadiphosphacyclododecin-2-yl]-1,9-dihydro-6H-purin-6-one タイプ: ligand / ID: 2 / コピー数: 4 / 式: 4BW |
|---|---|
| 分子量 | 理論値: 674.411 Da |
| Chemical component information | 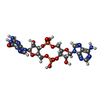 ChemComp-4BW: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 52.9 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.6 µm 最小 デフォーカス(公称値): 1.4000000000000001 µm |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー







 Z
Z Y
Y X
X