+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1eio | ||||||
|---|---|---|---|---|---|---|---|
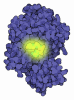
| タイトル | ILEAL LIPID BINDING PROTEIN IN COMPLEX WITH GLYCOCHOLATE | ||||||
 要素 要素 | ILEAL LIPID BINDING PROTEIN | ||||||
 キーワード キーワード | LIPID BINDING PROTEIN / bile acid binding / protein-ligand interaction / LIPID-BINDING PROTEIN | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | ||||||
| 生物種 |  | ||||||
| 手法 | 溶液NMR / distance geometry, simulated annealing | ||||||
 データ登録者 データ登録者 | Luecke, C. / Zhang, F. / Hamilton, J.A. / Sacchettini, J.C. / Rueterjans, H. | ||||||
 引用 引用 |  ジャーナル: Eur.J.Biochem. / 年: 2000 ジャーナル: Eur.J.Biochem. / 年: 2000タイトル: Solution structure of ileal lipid binding protein in complex with glycocholate. 著者: Luecke, C. / Zhang, F. / Hamilton, J.A. / Sacchettini, J.C. / Rueterjans, H. #1:  ジャーナル: Structure / 年: 1996 ジャーナル: Structure / 年: 1996タイトル: Flexibility is a likely determinant of binding in the case of Ileal Lipid Binding Protein 著者: Luecke, C. / Zhang, F. / Rueterjans, H. / Hamilton, J.A. / Sacchettini, J.C. #2:  ジャーナル: Mol.Cell.Biochem. / 年: 1999 ジャーナル: Mol.Cell.Biochem. / 年: 1999タイトル: A comparative study of the backbone dynamics of two closely related lipid binding proteins: bovine heart Fatty Acid Binding Protein and porcine Ileal Lipid Binding Protein 著者: Luecke, C. / Fushman, D. / Ludwig, C. / Hamilton, J.A. / Sacchettini, J.C. / Rueterjans, H. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1eio.cif.gz 1eio.cif.gz | 216.7 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1eio.ent.gz pdb1eio.ent.gz | 173.4 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1eio.json.gz 1eio.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  1eio_validation.pdf.gz 1eio_validation.pdf.gz | 385.8 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  1eio_full_validation.pdf.gz 1eio_full_validation.pdf.gz | 420.6 KB | 表示 | |
| XML形式データ |  1eio_validation.xml.gz 1eio_validation.xml.gz | 12.9 KB | 表示 | |
| CIF形式データ |  1eio_validation.cif.gz 1eio_validation.cif.gz | 20.7 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/ei/1eio https://data.pdbj.org/pub/pdb/validation_reports/ei/1eio ftp://data.pdbj.org/pub/pdb/validation_reports/ei/1eio ftp://data.pdbj.org/pub/pdb/validation_reports/ei/1eio | HTTPS FTP |
-関連構造データ
| 関連構造データ | |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| |||||||||
| NMR アンサンブル |
|
- 要素
要素
| #1: タンパク質 | 分子量: 14093.877 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   |
|---|---|
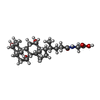
| #2: 化合物 | ChemComp-GCH / |
-実験情報
-実験
| 実験 | 手法: 溶液NMR | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| NMR実験 |
|
- 試料調製
試料調製
| 詳細 | 内容: 3-4mM ILBP/glycocholate complex / 溶媒系: 20mM phosphate; 0.05% azide; 90% H2O, 10% D2O |
|---|---|
| 試料状態 | イオン強度: 20mM KH2PO4 / pH: 5 / 圧: ambient / 温度: 310 K |
| 結晶化 | *PLUS 手法: other / 詳細: NMR |
-NMR測定
| NMRスペクトロメーター |
|
|---|
- 解析
解析
| NMR software |
| ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 手法: distance geometry, simulated annealing / ソフトェア番号: 1 詳細: the ligand was docked into the protein structure by simulated annealing | ||||||||||||||||||||||||
| 代表構造 | 選択基準: lowest energy | ||||||||||||||||||||||||
| NMRアンサンブル | コンフォーマー選択の基準: structures with the lowest energies after docking of ligand 計算したコンフォーマーの数: 8 / 登録したコンフォーマーの数: 5 |
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj