+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the DNA polymerase holoenzyme E9-A20-D4 of vaccinia virus | ||||||||||||||||||||||||
 マップデータ マップデータ | Sharpened map with b=160 A2, masked. | ||||||||||||||||||||||||
 試料 試料 |
| ||||||||||||||||||||||||
 キーワード キーワード | DNA polymerase / holoenzyme / processivity factor / uracil-DNA glycosylase / VIRAL PROTEIN | ||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報uracil-DNA glycosylase / viral DNA genome replication / uracil DNA N-glycosylase activity / 加水分解酵素; エステル加水分解酵素; 5'-リン酸モノエステル産生エンドデオキシリボヌクレアーゼ / nucleotide-excision repair, DNA gap filling / DNA replication proofreading / 3'-5'-DNA exonuclease activity / SOS response / base-excision repair, gap-filling / DNA recombination ...uracil-DNA glycosylase / viral DNA genome replication / uracil DNA N-glycosylase activity / 加水分解酵素; エステル加水分解酵素; 5'-リン酸モノエステル産生エンドデオキシリボヌクレアーゼ / nucleotide-excision repair, DNA gap filling / DNA replication proofreading / 3'-5'-DNA exonuclease activity / SOS response / base-excision repair, gap-filling / DNA recombination / DNA replication / DNA-directed DNA polymerase / DNA-directed DNA polymerase activity / DNA repair / nucleotide binding / DNA binding 類似検索 - 分子機能 | ||||||||||||||||||||||||
| 生物種 |   Vaccinia virus Copenhagen (ウイルス) Vaccinia virus Copenhagen (ウイルス) | ||||||||||||||||||||||||
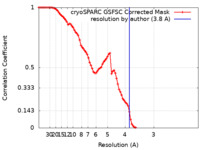
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.8 Å | ||||||||||||||||||||||||
 データ登録者 データ登録者 | Burmeister WP / Ballandras-Colas A / Boettcher B / Grimm C | ||||||||||||||||||||||||
| 資金援助 |  フランス, フランス,  米国, 米国,  ドイツ, 7件 ドイツ, 7件
| ||||||||||||||||||||||||
 引用 引用 |  ジャーナル: PLoS Pathog / 年: 2024 ジャーナル: PLoS Pathog / 年: 2024タイトル: Structure and flexibility of the DNA polymerase holoenzyme of vaccinia virus. 著者: Wim P Burmeister / Laetitia Boutin / Aurelia C Balestra / Henri Gröger / Allison Ballandras-Colas / Stephanie Hutin / Christian Kraft / Clemens Grimm / Bettina Böttcher / Utz Fischer / ...著者: Wim P Burmeister / Laetitia Boutin / Aurelia C Balestra / Henri Gröger / Allison Ballandras-Colas / Stephanie Hutin / Christian Kraft / Clemens Grimm / Bettina Böttcher / Utz Fischer / Nicolas Tarbouriech / Frédéric Iseni /   要旨: The year 2022 was marked by the mpox outbreak caused by the human monkeypox virus (MPXV), which is approximately 98% identical to the vaccinia virus (VACV) at the sequence level with regard to the ...The year 2022 was marked by the mpox outbreak caused by the human monkeypox virus (MPXV), which is approximately 98% identical to the vaccinia virus (VACV) at the sequence level with regard to the proteins involved in DNA replication. We present the production in the baculovirus-insect cell system of the VACV DNA polymerase holoenzyme, which consists of the E9 polymerase in combination with its co-factor, the A20-D4 heterodimer. This led to the 3.8 Å cryo-electron microscopy (cryo-EM) structure of the DNA-free form of the holoenzyme. The model of the holoenzyme was constructed from high-resolution structures of the components of the complex and the A20 structure predicted by AlphaFold 2. The structures do not change in the context of the holoenzyme compared to the previously determined crystal and NMR structures, but the E9 thumb domain became disordered. The E9-A20-D4 structure shows the same compact arrangement with D4 folded back on E9 as observed for the recently solved MPXV holoenzyme structures in the presence and the absence of bound DNA. A conserved interface between E9 and D4 is formed by a cluster of hydrophobic residues. Small-angle X-ray scattering data show that other, more open conformations of E9-A20-D4 without the E9-D4 contact exist in solution using the flexibility of two hinge regions in A20. Biolayer interferometry (BLI) showed that the E9-D4 interaction is indeed weak and transient in the absence of DNA although it is very important, as it has not been possible to obtain viable viruses carrying mutations of key residues within the E9-D4 interface. | ||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_18134.map.gz emd_18134.map.gz | 53 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-18134-v30.xml emd-18134-v30.xml emd-18134.xml emd-18134.xml | 25.1 KB 25.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_18134_fsc.xml emd_18134_fsc.xml | 8.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_18134.png emd_18134.png | 205.8 KB | ||
| Filedesc metadata |  emd-18134.cif.gz emd-18134.cif.gz | 7.8 KB | ||
| その他 |  emd_18134_half_map_1.map.gz emd_18134_half_map_1.map.gz emd_18134_half_map_2.map.gz emd_18134_half_map_2.map.gz | 59.4 MB 59.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-18134 http://ftp.pdbj.org/pub/emdb/structures/EMD-18134 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18134 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-18134 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_18134_validation.pdf.gz emd_18134_validation.pdf.gz | 640.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_18134_full_validation.pdf.gz emd_18134_full_validation.pdf.gz | 640.1 KB | 表示 | |
| XML形式データ |  emd_18134_validation.xml.gz emd_18134_validation.xml.gz | 16.4 KB | 表示 | |
| CIF形式データ |  emd_18134_validation.cif.gz emd_18134_validation.cif.gz | 21.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18134 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18134 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18134 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-18134 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8q3rMC  8qamC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_18134.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_18134.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Sharpened map with b=160 A2, masked. | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.064 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: correct hand, from cryosparc NU refinement
| ファイル | emd_18134_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | correct hand, from cryosparc NU refinement | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: correct hand, from cryosparc NU refinement
| ファイル | emd_18134_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | correct hand, from cryosparc NU refinement | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : E9-A20-D4 DNA polymerase holoenzyme
| 全体 | 名称: E9-A20-D4 DNA polymerase holoenzyme |
|---|---|
| 要素 |
|
-超分子 #1: E9-A20-D4 DNA polymerase holoenzyme
| 超分子 | 名称: E9-A20-D4 DNA polymerase holoenzyme / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all / 詳細: heterotrimer |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 196.825 kDa/nm |
-分子 #1: Uracil-DNA glycosylase
| 分子 | 名称: Uracil-DNA glycosylase / タイプ: protein_or_peptide / ID: 1 / 詳細: D4 carries a N-terminal Strep-tag / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Vaccinia virus Copenhagen (ウイルス) Vaccinia virus Copenhagen (ウイルス) |
| 分子量 | 理論値: 27.468379 KDa |
| 組換発現 | 生物種:  Trichoplusia ni (イラクサキンウワバ) Trichoplusia ni (イラクサキンウワバ) |
| 配列 | 文字列: MASWSHPQFE KSGGGGGLVP RGSAMNSVTV SHAPYTITYH DDWEPVMSQL VEFYNEVASW LLRDETSPIP DKFFIQLKQP LRNKRVCVC GIDPYPKDGT GVPFESPNFT KKSIKEIASS ISRLTGVIDY KGYNLNIIDG VIPWNYYLSC KLGETKSHAI Y WDKISKLL ...文字列: MASWSHPQFE KSGGGGGLVP RGSAMNSVTV SHAPYTITYH DDWEPVMSQL VEFYNEVASW LLRDETSPIP DKFFIQLKQP LRNKRVCVC GIDPYPKDGT GVPFESPNFT KKSIKEIASS ISRLTGVIDY KGYNLNIIDG VIPWNYYLSC KLGETKSHAI Y WDKISKLL LQHITKHVSV LYCLGKTDFS NIRAKLESPV TTIVGYHPAA RDRQFEKDRS FEIINVLLEL DNKAPINWAQ GF IY UniProtKB: Uracil-DNA glycosylase |
-分子 #2: DNA polymerase processivity factor component OPG148
| 分子 | 名称: DNA polymerase processivity factor component OPG148 / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Vaccinia virus Copenhagen (ウイルス) Vaccinia virus Copenhagen (ウイルス) |
| 分子量 | 理論値: 49.247031 KDa |
| 組換発現 | 生物種:  Trichoplusia ni (イラクサキンウワバ) Trichoplusia ni (イラクサキンウワバ) |
| 配列 | 文字列: MTSSADLTNL KELLSLYKSL RFSDSAAIEK YNSLVEWGTS TYWKIGVQKV ANVETSISDY YDEVKNKPFN IDPGYYIFLP VYFGSVFIY SKGKNMVELG SGNSFQIPDD MRSACNKVLD SDNGIDFLRF VLLNNRWIME DAISKYQSPV NIFKLASEYG L NIPKYLEI ...文字列: MTSSADLTNL KELLSLYKSL RFSDSAAIEK YNSLVEWGTS TYWKIGVQKV ANVETSISDY YDEVKNKPFN IDPGYYIFLP VYFGSVFIY SKGKNMVELG SGNSFQIPDD MRSACNKVLD SDNGIDFLRF VLLNNRWIME DAISKYQSPV NIFKLASEYG L NIPKYLEI EIEEDTLFDD ELYSIIERSF DDKFPKISIS YIKLGELRRQ VVDFFKFSFM YIESIKVDRI GDNIFIPSVI TK SGKKILV KDVDHLIRSK VREHTFVKVK KKNTFSILYD YDGNGTETRG EVIKRIIDTI GRDYYVNGKY FSKVGSAGLK QLT NKLDIN ECATVDELVD EINKSGTVKR KIKNQSAFDL SRECLGYPEA DFITLVNNMR FKIENCKVVN FNIENTNCLN NPSI ETIYR NFNQFVSIFN VVTDVKKRLF E UniProtKB: DNA polymerase processivity factor component OPG148 |
-分子 #3: DNA polymerase
| 分子 | 名称: DNA polymerase / タイプ: protein_or_peptide / ID: 3 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Vaccinia virus Copenhagen (ウイルス) Vaccinia virus Copenhagen (ウイルス) |
| 分子量 | 理論値: 120.361484 KDa |
| 組換発現 | 生物種:  Trichoplusia ni (イラクサキンウワバ) Trichoplusia ni (イラクサキンウワバ) |
| 配列 | 文字列: MSYYHHHHHH DYDIPTTENL YFQGAMDPDV RCINWFESHG ENRFLYLKSR CRNGETVFIR FPHYFYYVVT DEIYQSLSPP PFNARPLGK MRTIDIDETI SYNLDIKDRK CSVADMWLIE EPKKRSIQNA TMDEFLNISW FYISNGISPD GCYSLDEQYL T KINNGCYH ...文字列: MSYYHHHHHH DYDIPTTENL YFQGAMDPDV RCINWFESHG ENRFLYLKSR CRNGETVFIR FPHYFYYVVT DEIYQSLSPP PFNARPLGK MRTIDIDETI SYNLDIKDRK CSVADMWLIE EPKKRSIQNA TMDEFLNISW FYISNGISPD GCYSLDEQYL T KINNGCYH CDDPRNCFAK KIPRFDIPRS YLFLDIECHF DKKFPSVFIN PISHTSYCYI DLSGKRLLFT LINEEMLTEQ EI QEAVDRG CLRIQSLMEM DYERELVLCS EIVLLRIAKQ LLELTFDYVV TFNGHNFDLR YITNRLELLT GEKIIFRSPD KKE AVHLCI YERNQSSHKG VGGMANTTFH VNNNNGTIFF DLYSFIQKSE KLDSYKLDSI SKNAFSCMGK VLNRGVREMT FIGD DTTDA KGKAAAFAKV LTTGNYVTVD EDIICKVIRK DIWENGFKVV LLCPTLPNDT YKLSFGKDDV DLAQMYKDYN LNIAL DMAR YCIHDACLCQ YLWEYYGVET KTDAGASTYV LPQSMVFEYR ASTVIKGPLL KLLLETKTIL VRSETKQKFP YEGGKV FAP KQKMFSNNVL IFDYNSLYPN VCIFGNLSPE TLVGVVVSTN RLEEEINNQL LLQKYPPPRY ITVHCEPRLP NLISEIA IF DRSIEGTIPR LLRTFLAERA RYKKMLKQAT SSTEKAIYDS MQYTYKIVAN SVYGLMGFRN SALYSYASAK SCTSIGRR M ILYLESVLNG AELSNGMLRF ANPLSNPFYM DDRDINPIVK TSLPIDYRFR FRSVYGDTDS VFTEIDSQDV DKSIEIAKE LERLINNRVL FNNFKIEFEA VYKNLIMQSK KKYTTMKYSA SSNSKSVPER INKGTSETRR DVSKFHKNMI KTYKTRLSEM LSEGRMNSN QVCIDILRSL ETDLRSEFDS RSSPLELFML SRMHHSNYKS ADNPNMYLVT EYNKNNPETI ELGERYYFAY I CPANVPWT KKLVNIKTYE TIIDRSFKLG SDQRIFYEVY FKRLTSEIVN LLDNKVLCIS FFERMFGSKP TFYEA UniProtKB: DNA polymerase |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.3 mg/mL | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.6 構成要素:
詳細: 35 mM Tris-HCl, pH 8, 150 mM NaCl, 5 mM EDTA, 3.8 mM desthiobiotin | |||||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 90 sec. / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.013000000000000001 kPa | |||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 4096 pixel / デジタル化 - サイズ - 縦: 4096 pixel / 撮影したグリッド数: 1 / 実像数: 1376 / 平均電子線量: 68.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.4 µm 最小 デフォーカス(公称値): 1.4000000000000001 µm 倍率(公称値): 42000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル |
| ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 詳細 | Phenix real-space refinement | ||||||||||||
| 精密化 | 空間: REAL / プロトコル: OTHER | ||||||||||||
| 得られたモデル |  PDB-8q3r: |
 ムービー
ムービー コントローラー
コントローラー







 Z
Z Y
Y X
X