+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the anaerobic ribonucleotide reductase from Prevotella copri in its tetrameric state produced in the presence of dATP and CTP | |||||||||||||||
 マップデータ マップデータ | Map post-processed using DeepEMhancer | |||||||||||||||
 試料 試料 |
| |||||||||||||||
 キーワード キーワード | ribonucleotide reductase glycyl radical enzyme allosteric regulation nucleotide biosynthesis / OXIDOREDUCTASE / BIOSYNTHETIC PROTEIN | |||||||||||||||
| 機能・相同性 | Ribonucleoside-triphosphate reductase, anaerobic / Anaerobic ribonucleoside-triphosphate reductase / ribonucleoside-triphosphate reductase (thioredoxin) activity / ATP-cone domain / ATP cone domain / ATP-cone domain profile. / DNA replication / ATP binding / Anaerobic ribonucleoside-triphosphate reductase 機能・相同性情報 機能・相同性情報 | |||||||||||||||
| 生物種 |  Prevotella copri (バクテリア) / Prevotella copri (バクテリア) /  Segatella copri (バクテリア) Segatella copri (バクテリア) | |||||||||||||||
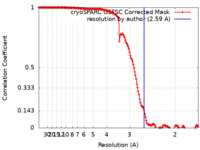
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.59 Å | |||||||||||||||
 データ登録者 データ登録者 | Banerjee I / Bimai O / Sjoberg BM / Logan DT | |||||||||||||||
| 資金援助 |  スウェーデン, スウェーデン,  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2024 ジャーナル: Elife / 年: 2024タイトル: Nucleotide binding to the ATP-cone in anaerobic ribonucleotide reductases allosterically regulates activity by modulating substrate binding. 著者: Ornella Bimai / Ipsita Banerjee / Inna Rozman Grinberg / Ping Huang / Lucas Hultgren / Simon Ekström / Daniel Lundin / Britt-Marie Sjöberg / Derek T Logan /  要旨: A small, nucleotide-binding domain, the ATP-cone, is found at the N-terminus of most ribonucleotide reductase (RNR) catalytic subunits. By binding adenosine triphosphate (ATP) or deoxyadenosine ...A small, nucleotide-binding domain, the ATP-cone, is found at the N-terminus of most ribonucleotide reductase (RNR) catalytic subunits. By binding adenosine triphosphate (ATP) or deoxyadenosine triphosphate (dATP) it regulates the enzyme activity of all classes of RNR. Functional and structural work on aerobic RNRs has revealed a plethora of ways in which dATP inhibits activity by inducing oligomerisation and preventing a productive radical transfer from one subunit to the active site in the other. Anaerobic RNRs, on the other hand, store a stable glycyl radical next to the active site and the basis for their dATP-dependent inhibition is completely unknown. We present biochemical, biophysical, and structural information on the effects of ATP and dATP binding to the anaerobic RNR from . The enzyme exists in a dimer-tetramer equilibrium biased towards dimers when two ATP molecules are bound to the ATP-cone and tetramers when two dATP molecules are bound. In the presence of ATP, NrdD is active and has a fully ordered glycyl radical domain (GRD) in one monomer of the dimer. Binding of dATP to the ATP-cone results in loss of activity and increased dynamics of the GRD, such that it cannot be detected in the cryo-EM structures. The glycyl radical is formed even in the dATP-bound form, but the substrate does not bind. The structures implicate a complex network of interactions in activity regulation that involve the GRD more than 30 Å away from the dATP molecules, the allosteric substrate specificity site and a conserved but previously unseen flap over the active site. Taken together, the results suggest that dATP inhibition in anaerobic RNRs acts by increasing the flexibility of the flap and GRD, thereby preventing both substrate binding and radical mobilisation. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_17360.map.gz emd_17360.map.gz | 318 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-17360-v30.xml emd-17360-v30.xml emd-17360.xml emd-17360.xml | 25.1 KB 25.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_17360_fsc.xml emd_17360_fsc.xml | 14.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_17360.png emd_17360.png | 66.5 KB | ||
| マスクデータ |  emd_17360_msk_1.map emd_17360_msk_1.map | 343 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-17360.cif.gz emd-17360.cif.gz | 7.3 KB | ||
| その他 |  emd_17360_additional_1.map.gz emd_17360_additional_1.map.gz emd_17360_half_map_1.map.gz emd_17360_half_map_1.map.gz emd_17360_half_map_2.map.gz emd_17360_half_map_2.map.gz | 317.5 MB 318.1 MB 318.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-17360 http://ftp.pdbj.org/pub/emdb/structures/EMD-17360 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17360 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-17360 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_17360_validation.pdf.gz emd_17360_validation.pdf.gz | 717.9 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_17360_full_validation.pdf.gz emd_17360_full_validation.pdf.gz | 717.5 KB | 表示 | |
| XML形式データ |  emd_17360_validation.xml.gz emd_17360_validation.xml.gz | 23.8 KB | 表示 | |
| CIF形式データ |  emd_17360_validation.cif.gz emd_17360_validation.cif.gz | 31.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17360 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17360 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17360 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-17360 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8p2cMC  8p23C  8p27C  8p28C  8p2dC  8p2sC  8p39C C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_17360.map.gz / 形式: CCP4 / 大きさ: 343 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_17360.map.gz / 形式: CCP4 / 大きさ: 343 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Map post-processed using DeepEMhancer | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.8464 Å | ||||||||||||||||||||||||||||||||||||
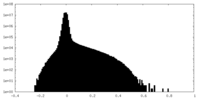
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_17360_msk_1.map emd_17360_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
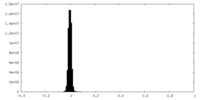
| 密度ヒストグラム |
-追加マップ: Unsharpened map from non-uniform refinement in cryoSPARC
| ファイル | emd_17360_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Unsharpened map from non-uniform refinement in cryoSPARC | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
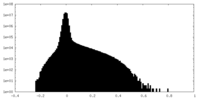
| 密度ヒストグラム |
-ハーフマップ: Half map A from non-uniform refinement in cryoSPARC
| ファイル | emd_17360_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A from non-uniform refinement in cryoSPARC | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half map B from non-uniform refinement in cryoSPARC
| ファイル | emd_17360_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map B from non-uniform refinement in cryoSPARC | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Anaerobic ribonucleotide reductase from Prevotella copri in its t...
| 全体 | 名称: Anaerobic ribonucleotide reductase from Prevotella copri in its tetrameric, dATP/CTP-bound state |
|---|---|
| 要素 |
|
-超分子 #1: Anaerobic ribonucleotide reductase from Prevotella copri in its t...
| 超分子 | 名称: Anaerobic ribonucleotide reductase from Prevotella copri in its tetrameric, dATP/CTP-bound state タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Prevotella copri (バクテリア) Prevotella copri (バクテリア) |
| 分子量 | 理論値: 336.8 KDa |
-分子 #1: Anaerobic ribonucleoside-triphosphate reductase
| 分子 | 名称: Anaerobic ribonucleoside-triphosphate reductase / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Segatella copri (バクテリア) Segatella copri (バクテリア) |
| 分子量 | 理論値: 84.636055 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: GPGSMIQTVV KRDGRIVGFN EQKIMAAIRK AMLHTDKGED TTLIEQITDH ISYRGKSQMS VEAIQDAIEM ELMKSARKDV AQKYIAYRN QRNIARKAKT RDVFMSIVNA KNNDITRENA NMNADTPAGM MMKFASETTK PFVDDYLLSE DVRDAVMHNY I HIHDKDYY ...文字列: GPGSMIQTVV KRDGRIVGFN EQKIMAAIRK AMLHTDKGED TTLIEQITDH ISYRGKSQMS VEAIQDAIEM ELMKSARKDV AQKYIAYRN QRNIARKAKT RDVFMSIVNA KNNDITRENA NMNADTPAGM MMKFASETTK PFVDDYLLSE DVRDAVMHNY I HIHDKDYY PTKSLTCVQH PLDVILNHGF TAGHGSSRPA KRIETAAVLA CISLETCQNE MHGGQAIPAF DFYLAPYVRM SY QEEVKNL EKLTGEDLSN LYDAPIDDYI EKPLDGLQGR ERLEQHAINK TVNRVHQAME AFIHNMNTIH SRGGNQVVFS SIN YGTDTS AEGRCIMREI LQSTYQGVGN GETAIFPIQI WKKKRGVNYL PEDRNYDLYK LACKVTARRF FPNFLNLDAT FNQN EKWRA DDPERYKWEI ATMGCRTRVF EDRWGEKTSI ARGNLSFSTI NIVKLAIECM GIENEKQRID MFFAKLDNIL DITAK QLDE RFQFQKTAMA KQFPLLMKYL WVGAENLKPE ETIESVINHG TLGIGFIGLA ECLVALIGKH HGESEKAQEL GLKIIT YMR DRANEFSEQY HHNYSILATP AEGLSGKFTK KDRKQFGVIP GVTDRDYYTN SNHVPVYYKC TALKKAQIEA PYHDLTR GG HIFYVEIDGD ATHNPSVIES VVDMMDKYNM GYGSVNHNRN RCLDCGYENA DAHLEVCPKC GSHHIDKLQR ITGYLVGT T DRWNSGKLAE LHDRVTHIGG EK UniProtKB: Anaerobic ribonucleoside-triphosphate reductase |
-分子 #2: 2'-DEOXYADENOSINE 5'-TRIPHOSPHATE
| 分子 | 名称: 2'-DEOXYADENOSINE 5'-TRIPHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 12 / 式: DTP |
|---|---|
| 分子量 | 理論値: 491.182 Da |
| Chemical component information |  ChemComp-DTP: |
-分子 #3: MAGNESIUM ION
| 分子 | 名称: MAGNESIUM ION / タイプ: ligand / ID: 3 / コピー数: 4 / 式: MG |
|---|---|
| 分子量 | 理論値: 24.305 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| |||||||||||||||||||||
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. / 前処理 - 雰囲気: OTHER | |||||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV / 詳細: blot force 1, 5s blot time. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum |
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / デジタル化 - サイズ - 横: 5760 pixel / デジタル化 - サイズ - 縦: 4092 pixel / 撮影したグリッド数: 1 / 実像数: 11780 / 平均露光時間: 2.0 sec. / 平均電子線量: 38.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.6 µm / 倍率(公称値): 105000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Source name: PDB / Chain - Initial model type: experimental model |
|---|---|
| 詳細 | Manual fitting was done using Coot and automatic real space refinement used phenix.refine |
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT / 当てはまり具合の基準: correlation coefficient |
| 得られたモデル |  PDB-8p2c: |
 ムービー
ムービー コントローラー
コントローラー











 Z (Sec.)
Z (Sec.) X (Row.)
X (Row.) Y (Col.)
Y (Col.)