+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Human apo TRPM8 in a closed state (composite map) | |||||||||
 マップデータ マップデータ | composite map created by combining consensus map with four copies of focused pre-MHR MHR1/2 map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | calcium ion channel / cold temperature sensor / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報ligand-gated calcium channel activity / thermoception / TRP channels / response to cold / calcium ion transmembrane transport / calcium channel activity / intracellular calcium ion homeostasis / positive regulation of cold-induced thermogenesis / membrane raft / external side of plasma membrane ...ligand-gated calcium channel activity / thermoception / TRP channels / response to cold / calcium ion transmembrane transport / calcium channel activity / intracellular calcium ion homeostasis / positive regulation of cold-induced thermogenesis / membrane raft / external side of plasma membrane / endoplasmic reticulum membrane / identical protein binding / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.65 Å | |||||||||
 データ登録者 データ登録者 | Palchevskyi S / Czarnocki-Cieciura M / Vistoli G / Gervasoni S / Nowak E / Beccari AR / Nowotny M / Talarico C | |||||||||
| 資金援助 |  ポーランド, 1件 ポーランド, 1件
| |||||||||
 引用 引用 |  ジャーナル: Commun Biol / 年: 2023 ジャーナル: Commun Biol / 年: 2023タイトル: Structure of human TRPM8 channel. 著者: Sergii Palchevskyi / Mariusz Czarnocki-Cieciura / Giulio Vistoli / Silvia Gervasoni / Elżbieta Nowak / Andrea R Beccari / Marcin Nowotny / Carmine Talarico /    要旨: TRPM8 is a non-selective cation channel permeable to both monovalent and divalent cations that is activated by multiple factors, such as temperature, voltage, pressure, and changes in osmolality. It ...TRPM8 is a non-selective cation channel permeable to both monovalent and divalent cations that is activated by multiple factors, such as temperature, voltage, pressure, and changes in osmolality. It is a therapeutic target for anticancer drug development, and its modulators can be utilized for several pathological conditions. Here, we present a cryo-electron microscopy structure of a human TRPM8 channel in the closed state that was solved at 2.7 Å resolution. Our structure comprises the most complete model of the N-terminal pre-melastatin homology region. We also visualized several lipids that are bound by the protein and modeled how the human channel interacts with icilin. Analyses of pore helices in available TRPM structures showed that all these structures can be grouped into different closed, desensitized and open state conformations based on the register of the pore helix S6 which positions particular amino acid residues at the channel constriction. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_15981.map.gz emd_15981.map.gz | 10.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-15981-v30.xml emd-15981-v30.xml emd-15981.xml emd-15981.xml | 18 KB 18 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_15981.png emd_15981.png | 153.5 KB | ||
| Filedesc metadata |  emd-15981.cif.gz emd-15981.cif.gz | 7 KB | ||
| その他 |  emd_15981_additional_1.map.gz emd_15981_additional_1.map.gz | 141.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-15981 http://ftp.pdbj.org/pub/emdb/structures/EMD-15981 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15981 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15981 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_15981_validation.pdf.gz emd_15981_validation.pdf.gz | 381.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_15981_full_validation.pdf.gz emd_15981_full_validation.pdf.gz | 380.8 KB | 表示 | |
| XML形式データ |  emd_15981_validation.xml.gz emd_15981_validation.xml.gz | 7.1 KB | 表示 | |
| CIF形式データ |  emd_15981_validation.cif.gz emd_15981_validation.cif.gz | 8.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15981 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15981 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15981 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15981 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8bdcMC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_15981.map.gz / 形式: CCP4 / 大きさ: 282.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_15981.map.gz / 形式: CCP4 / 大きさ: 282.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | composite map created by combining consensus map with four copies of focused pre-MHR MHR1/2 map | ||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.82 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: raw consensus map
| ファイル | emd_15981_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | raw consensus map | ||||||||||||
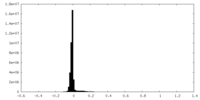
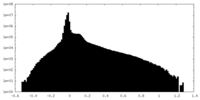
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Human TRPM8 in apo form
| 全体 | 名称: Human TRPM8 in apo form |
|---|---|
| 要素 |
|
-超分子 #1: Human TRPM8 in apo form
| 超分子 | 名称: Human TRPM8 in apo form / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 510 KDa |
-分子 #1: Transient receptor potential cation channel subfamily M member 8
| 分子 | 名称: Transient receptor potential cation channel subfamily M member 8 タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 127.904719 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SNSFRAARLS MRNRRNDTLD STRTLYSSAS RSTDLSYSES DLVNFIQANF KKRECVFFTK DSKATENVCK CGYAQSQHME GTQINQSEK WNYKKHTKEF PTDAFGDIQF ETLGKKGKYI RLSCDTDAEI LYELLTQHWH LKTPNLVISV TGGAKNFALK P RMRKIFSR ...文字列: SNSFRAARLS MRNRRNDTLD STRTLYSSAS RSTDLSYSES DLVNFIQANF KKRECVFFTK DSKATENVCK CGYAQSQHME GTQINQSEK WNYKKHTKEF PTDAFGDIQF ETLGKKGKYI RLSCDTDAEI LYELLTQHWH LKTPNLVISV TGGAKNFALK P RMRKIFSR LIYIAQSKGA WILTGGTHYG LMKYIGEVVR DNTISRSSEE NIVAIGIAAW GMVSNRDTLI RNCDAEGYFL AQ YLMDDFT RDPLYILDNN HTHLLLVDNG CHGHPTVEAK LRNQLEKYIS ERTIQDSNYG GKIPIVCFAQ GGGKETLKAI NTS IKNKIP CVVVEGSGQI ADVIASLVEV EDALTSSAVK EKLVRFLPRT VSRLPEEETE SWIKWLKEIL ECSHLLTVIK MEEA GDEIV SNAISYALYK AFSTSEQDKD NWNGQLKLLL EWNQLDLAND EIFTNDRRWE SADLQEVMFT ALIKDRPKFV RLFLE NGLN LRKFLTHDVL TELFSNHFST LVYRNLQIAK NSYNDALLTF VWKLVANFRR GFRKEDRNGR DEMDIELHDV SPITRH PLQ ALFIWAILQN KKELSKVIWE QTRGCTLAAL GASKLLKTLA KVKNDINAAG ESEELANEYE TRAVELFTEC YSSDEDL AE QLLVYSCEAW GGSNCLELAV EATDQHFIAQ PGVQNFLSKQ WYGEISRDTK NWKIILCLFI IPLVGCGFVS FRKKPVDK H KKLLWYYVAF FTSPFVVFSW NVVFYIAFLL LFAYVLLMDF HSVPHPPELV LYSLVFVLFC DEVRQWYVNG VNYFTDLWN VMDTLGLFYF IAGIVFRLHS SNKSSLYSGR VIFCLDYIIF TLRLIHIFTV SRNLGPKIIM LQRMLIDVFF FLFLFAVWMV AFGVARQGI LRQNEQRWRW IFRSVIYEPY LAMFGQVPSD VDGTTYDFAH CTFTGNESKP LCVELDEHNL PRFPEWITIP L VCIYMLST NILLVNLLVA MFGYTVGTVQ ENNDQVWKFQ RYFLVQEYCS RLNIPFPFIV FAYFYMVVKK CFKCCCKEKN ME SSVCCFK NEDNETLAWE GVMKENYLVK INTKANDTSE EMRHRFRQLD TKLNDLKGLL KEIANKIK UniProtKB: Transient receptor potential cation channel subfamily M member 8 |
-分子 #2: CHOLESTEROL HEMISUCCINATE
| 分子 | 名称: CHOLESTEROL HEMISUCCINATE / タイプ: ligand / ID: 2 / コピー数: 8 / 式: Y01 |
|---|---|
| 分子量 | 理論値: 486.726 Da |
| Chemical component information |  ChemComp-Y01: |
-分子 #3: (2S)-3-(hexadecanoyloxy)-2-[(9Z)-octadec-9-enoyloxy]propyl 2-(tri...
| 分子 | 名称: (2S)-3-(hexadecanoyloxy)-2-[(9Z)-octadec-9-enoyloxy]propyl 2-(trimethylammonio)ethyl phosphate タイプ: ligand / ID: 3 / コピー数: 4 / 式: POV |
|---|---|
| 分子量 | 理論値: 760.076 Da |
| Chemical component information | 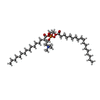 ChemComp-POV: |
-分子 #4: UNDECANE
| 分子 | 名称: UNDECANE / タイプ: ligand / ID: 4 / コピー数: 4 / 式: UND |
|---|---|
| 分子量 | 理論値: 156.308 Da |
| Chemical component information | 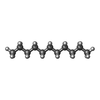 ChemComp-UND: |
-分子 #5: SODIUM ION
| 分子 | 名称: SODIUM ION / タイプ: ligand / ID: 5 / コピー数: 8 |
|---|---|
| 分子量 | 理論値: 22.99 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| グリッド | モデル: UltrAuFoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE 詳細: The grid was glow-discharged from both sides prior to vitrification |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
| 詳細 | protein solubilized by LMNG |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 実像数: 7918 / 平均電子線量: 41.42 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.7 µm / 最小 デフォーカス(公称値): 0.9 µm / 倍率(公称値): 105000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-8bdc: |
 ムービー
ムービー コントローラー
コントローラー






 Z
Z Y
Y X
X