+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of a substrate-bound glutamate transporter homologue GltTk encapsulated within a nanodisc | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Glutamate / transporter / mutant / nanodisc / TRANSPORT PROTEIN | |||||||||
| 機能・相同性 | carboxylic acid transport / Sodium:dicarboxylate symporter / Sodium:dicarboxylate symporter, conserved site / Sodium:dicarboxylate symporter superfamily / Sodium:dicarboxylate symporter family / Sodium:dicarboxylate symporter family signature 1. / symporter activity / membrane / Proton/glutamate symporter, SDF family 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   Thermococcus kodakarensis (古細菌) Thermococcus kodakarensis (古細菌) | |||||||||
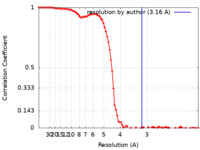
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.25 Å | |||||||||
 データ登録者 データ登録者 | Whittaker JJ / Guskov A | |||||||||
| 資金援助 |  オランダ, 1件 オランダ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2020 ジャーナル: Nat Commun / 年: 2020タイトル: Structural ensemble of a glutamate transporter homologue in lipid nanodisc environment. 著者: Valentina Arkhipova / Albert Guskov / Dirk J Slotboom /   要旨: Glutamate transporters are cation-coupled secondary active membrane transporters that clear the neurotransmitter L-glutamate from the synaptic cleft. These transporters are homotrimers, with each ...Glutamate transporters are cation-coupled secondary active membrane transporters that clear the neurotransmitter L-glutamate from the synaptic cleft. These transporters are homotrimers, with each protomer functioning independently by an elevator-type mechanism, in which a mobile transport domain alternates between inward- and outward-oriented states. Using single-particle cryo-EM we have determined five structures of the glutamate transporter homologue Glt, a Na- L-aspartate symporter, embedded in lipid nanodiscs. Dependent on the substrate concentrations used, the protomers of the trimer adopt a variety of asymmetrical conformations, consistent with the independent movement. Six of the 15 resolved protomers are in a hitherto elusive state of the transport cycle in which the inward-facing transporters are loaded with Na ions. These structures explain how substrate-leakage is prevented - a strict requirement for coupled transport. The belt protein of the lipid nanodiscs bends around the inward oriented protomers, suggesting that membrane deformations occur during transport. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_15393.map.gz emd_15393.map.gz | 59.5 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-15393-v30.xml emd-15393-v30.xml emd-15393.xml emd-15393.xml | 16.9 KB 16.9 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_15393_fsc.xml emd_15393_fsc.xml | 11.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_15393.png emd_15393.png | 123.9 KB | ||
| Filedesc metadata |  emd-15393.cif.gz emd-15393.cif.gz | 6.1 KB | ||
| その他 |  emd_15393_half_map_1.map.gz emd_15393_half_map_1.map.gz emd_15393_half_map_2.map.gz emd_15393_half_map_2.map.gz | 58.7 MB 58.8 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-15393 http://ftp.pdbj.org/pub/emdb/structures/EMD-15393 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15393 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15393 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_15393_validation.pdf.gz emd_15393_validation.pdf.gz | 752.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_15393_full_validation.pdf.gz emd_15393_full_validation.pdf.gz | 752.1 KB | 表示 | |
| XML形式データ |  emd_15393_validation.xml.gz emd_15393_validation.xml.gz | 16.7 KB | 表示 | |
| CIF形式データ |  emd_15393_validation.cif.gz emd_15393_validation.cif.gz | 21.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15393 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15393 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15393 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15393 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8afaMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_15393.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_15393.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.836 Å | ||||||||||||||||||||||||||||||||||||
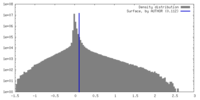
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_15393_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
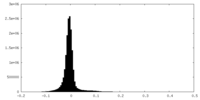
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_15393_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Glutamate transporter homologue GltTK in a lipid nanodisc environ...
| 全体 | 名称: Glutamate transporter homologue GltTK in a lipid nanodisc environment bound with L-aspartate ligands |
|---|---|
| 要素 |
|
-超分子 #1: Glutamate transporter homologue GltTK in a lipid nanodisc environ...
| 超分子 | 名称: Glutamate transporter homologue GltTK in a lipid nanodisc environment bound with L-aspartate ligands タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Thermococcus kodakarensis (古細菌) / 株: BL21(DE3) Thermococcus kodakarensis (古細菌) / 株: BL21(DE3) |
| 分子量 | 理論値: 1.39 MDa |
-分子 #1: Proton/glutamate symporter, SDF family
| 分子 | 名称: Proton/glutamate symporter, SDF family / タイプ: protein_or_peptide / ID: 1 / 詳細: Mutant P208R / コピー数: 3 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Thermococcus kodakarensis (古細菌) / 株: ATCC BAA-918 / JCM 12380 / KOD1 / 細胞: E.coli Thermococcus kodakarensis (古細菌) / 株: ATCC BAA-918 / JCM 12380 / KOD1 / 細胞: E.coli |
| 分子量 | 理論値: 46.745441 KDa |
| 組換発現 | 生物種:   Thermococcus kodakarensis (古細菌) Thermococcus kodakarensis (古細菌) |
| 配列 | 文字列: MGKSLLRRYL DYPVLWKILW GLVLGAVFGL IAGHFGYAGA VKTYIKPFGD LFVRLLKMLV MPIVLASLVV GAASISPARL GRVGVKIVV YYLATSAMAV FFGLIVGRLF NVGANVNLGS GTGKAIEAQP PSLVQTLLNI VPTNPFASLA KGEVLPVIFF A IILGIAIT ...文字列: MGKSLLRRYL DYPVLWKILW GLVLGAVFGL IAGHFGYAGA VKTYIKPFGD LFVRLLKMLV MPIVLASLVV GAASISPARL GRVGVKIVV YYLATSAMAV FFGLIVGRLF NVGANVNLGS GTGKAIEAQP PSLVQTLLNI VPTNPFASLA KGEVLPVIFF A IILGIAIT YLMNRNEERV RKSAETLLRV FDGLAEAMYL IVGGVMQYAR IGVFALIAYV MAEQGVRVVG PLAKVVGAVY TG LFLQIVI TYFILLKVFG IDPIKFIRKA KDAMITAFVT RSSSGTLPVT MRVAEEEMGV DKGIFSFTLP LGATINMDGT ALY QGVTVL FVANAIGHPL TLGQQLVVVL TAVLASIGTA GVPGAGAIML AMVLQSVGLD LTPGSPVALA YAMILGIDAI LDMG RTMVN VTGDLAGTVI VAKTEKELDE SKWISHHHHH HHH UniProtKB: Proton/glutamate symporter, SDF family |
-分子 #2: ASPARTIC ACID
| 分子 | 名称: ASPARTIC ACID / タイプ: ligand / ID: 2 / コピー数: 3 / 式: ASP |
|---|---|
| 分子量 | 理論値: 133.103 Da |
| Chemical component information | 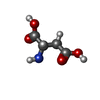 ChemComp-ASP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.5 mg/mL | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
| ||||||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 支持フィルム - Film thickness: 100 | ||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / デジタル化 - スキャナー: OTHER / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 5.0 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー




 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)