+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of Ldh-EtfAB complex from Acetobacterium woodii | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Electron bifurcation / Electron confirmation / Lactate / Lactate dehydrogenase complex / Electron transferring flavoprotein / A. woodii / redox enzyme / FLAVOPROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報lactate dehydrogenase (NAD+,ferredoxin) / D-lactate dehydrogenase activity / FAD binding / flavin adenine dinucleotide binding / 4 iron, 4 sulfur cluster binding / electron transfer activity / oxidoreductase activity / metal ion binding / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Acetobacterium woodii (バクテリア) Acetobacterium woodii (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.43 Å | |||||||||
 データ登録者 データ登録者 | Kayastha K / Ermler U | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Elife / 年: 2022 ジャーナル: Elife / 年: 2022タイトル: Structure-based electron-confurcation mechanism of the Ldh-EtfAB complex. 著者: Kanwal Kayastha / Alexander Katsyv / Christina Himmrich / Sonja Welsch / Jan M Schuller / Ulrich Ermler / Volker Müller /  要旨: Lactate oxidation with NAD as electron acceptor is a highly endergonic reaction. Some anaerobic bacteria overcome the energetic hurdle by flavin-based electron bifurcation/confurcation (FBEB/FBEC) ...Lactate oxidation with NAD as electron acceptor is a highly endergonic reaction. Some anaerobic bacteria overcome the energetic hurdle by flavin-based electron bifurcation/confurcation (FBEB/FBEC) using a lactate dehydrogenase (Ldh) in concert with the electron-transferring proteins EtfA and EtfB. The electron cryo-microscopically characterized (Ldh-EtfAB) complex of at 2.43 Å resolution consists of a mobile EtfAB shuttle domain located between the rigid central Ldh and the peripheral EtfAB base units. The FADs of Ldh and the EtfAB shuttle domain contact each other thereby forming the D (dehydrogenation-connected) state. The intermediary Glu37 and Glu139 may harmonize the redox potentials between the FADs and the pyruvate/lactate pair crucial for FBEC. By integrating Alphafold2 calculations a plausible novel B (bifurcation-connected) state was obtained allowing electron transfer between the EtfAB base and shuttle FADs. Kinetic analysis of enzyme variants suggests a correlation between NAD binding site and D-to-B-state transition implicating a 75° rotation of the EtfAB shuttle domain. The FBEC inactivity when truncating the ferredoxin domain of EtfA substantiates its role as redox relay. Lactate oxidation in Ldh is assisted by the catalytic base His423 and a metal center. On this basis, a comprehensive catalytic mechanism of the FBEC process was proposed. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_13960.map.gz emd_13960.map.gz | 69.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-13960-v30.xml emd-13960-v30.xml emd-13960.xml emd-13960.xml | 18.7 KB 18.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_13960_fsc.xml emd_13960_fsc.xml | 13.1 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_13960.png emd_13960.png | 127.6 KB | ||
| マスクデータ |  emd_13960_msk_1.map emd_13960_msk_1.map | 91.1 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-13960.cif.gz emd-13960.cif.gz | 7.1 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-13960 http://ftp.pdbj.org/pub/emdb/structures/EMD-13960 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-13960 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-13960 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_13960_validation.pdf.gz emd_13960_validation.pdf.gz | 519.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_13960_full_validation.pdf.gz emd_13960_full_validation.pdf.gz | 518.7 KB | 表示 | |
| XML形式データ |  emd_13960_validation.xml.gz emd_13960_validation.xml.gz | 11.4 KB | 表示 | |
| CIF形式データ |  emd_13960_validation.cif.gz emd_13960_validation.cif.gz | 15.2 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13960 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13960 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13960 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13960 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7qh2MC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_13960.map.gz / 形式: CCP4 / 大きさ: 91.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_13960.map.gz / 形式: CCP4 / 大きさ: 91.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.93 Å | ||||||||||||||||||||||||||||||||||||
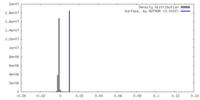
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_13960_msk_1.map emd_13960_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
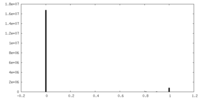
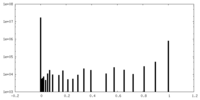
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Ldh-EtfAB complex
| 全体 | 名称: Ldh-EtfAB complex |
|---|---|
| 要素 |
|
-超分子 #1: Ldh-EtfAB complex
| 超分子 | 名称: Ldh-EtfAB complex / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#3 詳細: Complex composed of a dimer of a trimer of EtfA, EtfB and Ldh subunits making a hexameric oligomer state. Each of the subunits contain 1 FAD co-factor making total of 6 FADs. 2 Ldh subunits ...詳細: Complex composed of a dimer of a trimer of EtfA, EtfB and Ldh subunits making a hexameric oligomer state. Each of the subunits contain 1 FAD co-factor making total of 6 FADs. 2 Ldh subunits contain 1 Fe molecule each. |
|---|---|
| 由来(天然) | 生物種:  Acetobacterium woodii (バクテリア) Acetobacterium woodii (バクテリア) |
| 分子量 | 理論値: 220 KDa |
-分子 #1: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctC
| 分子 | 名称: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctC タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO / EC番号: ec: 1.3.1.110 |
|---|---|
| 由来(天然) | 生物種:  Acetobacterium woodii (バクテリア) / 株: ATCC 29683 / DSM 1030 / JCM 2381 / KCTC 1655 / WB1 Acetobacterium woodii (バクテリア) / 株: ATCC 29683 / DSM 1030 / JCM 2381 / KCTC 1655 / WB1 |
| 分子量 | 理論値: 46.222496 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MAGIKIIKEN VDRETFEALA EICPFDAFSY ENDKLEVTAA CKMCKMCLKK GPEGVLILEE DEKVAIDKSL YRGITVYVDH IEGQIHPVT FELIGKAREL AAVIGHPVYA LLMGTNITEK ADELLKYGVD KVFVYDKPEL KHFVIEPYAN VLEDFIEKVK P SSILVGAT ...文字列: MAGIKIIKEN VDRETFEALA EICPFDAFSY ENDKLEVTAA CKMCKMCLKK GPEGVLILEE DEKVAIDKSL YRGITVYVDH IEGQIHPVT FELIGKAREL AAVIGHPVYA LLMGTNITEK ADELLKYGVD KVFVYDKPEL KHFVIEPYAN VLEDFIEKVK P SSILVGAT NVGRSLAPRV AARYRTGLTA DCTILEMKEN TDLVQIRPAF GGNIMAQIVT ENTRPQFCTV RYKVFTAPER VN EPWGDVE MMDIEKAKLV SAIEVMEVIK KEKGIDLSEA ETIVAVGRGV KCEKDLDMIH EFAEKIGATV ACTRPGIEAG WFD ARLQIG LSGRTVKPKL IIALGISGAV QFAAGMQNSE YIIAINSDPK APIFNIAHCG MVGDLYEILP ELLTMIEGPE NNKD TETIS IPEAIETPER MVV UniProtKB: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctC |
-分子 #2: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctB
| 分子 | 名称: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctB タイプ: protein_or_peptide / ID: 2 / コピー数: 2 / 光学異性体: LEVO / EC番号: ec: 1.3.1.110 |
|---|---|
| 由来(天然) | 生物種:  Acetobacterium woodii (バクテリア) / 株: ATCC 29683 / DSM 1030 / JCM 2381 / KCTC 1655 / WB1 Acetobacterium woodii (バクテリア) / 株: ATCC 29683 / DSM 1030 / JCM 2381 / KCTC 1655 / WB1 |
| 分子量 | 理論値: 29.187627 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSKILVCIKQ VPGTSNVEVD PETGVLIRDG VESKLNPYDL FGLETAFRLK EQLGGTITTL SMGPMQSKEV LMESFYMGAD EGCLLSDRK FGGADVVATS YTLAQGTKRL GDFDLIICGK QTTDGDTAQV GPEMAEFLGI PHVTNVIKIL AADEKGLTLQ M NMEESLEI ...文字列: MSKILVCIKQ VPGTSNVEVD PETGVLIRDG VESKLNPYDL FGLETAFRLK EQLGGTITTL SMGPMQSKEV LMESFYMGAD EGCLLSDRK FGGADVVATS YTLAQGTKRL GDFDLIICGK QTTDGDTAQV GPEMAEFLGI PHVTNVIKIL AADEKGLTLQ M NMEESLEI QRVPYPCLIT VDKDIYTPRL PSYKRKLDIS KNPEIKILTL KDMYDTNEKK YGLSGSPTQV ERIFPPESNV EK TSFEGDG KVLAKALLGI LTEKKYLG UniProtKB: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctB |
-分子 #3: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctD
| 分子 | 名称: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctD タイプ: protein_or_peptide / ID: 3 / コピー数: 2 / 光学異性体: LEVO / EC番号: ec: 1.3.1.110 |
|---|---|
| 由来(天然) | 生物種:  Acetobacterium woodii (バクテリア) / 株: ATCC 29683 / DSM 1030 / JCM 2381 / KCTC 1655 / WB1 Acetobacterium woodii (バクテリア) / 株: ATCC 29683 / DSM 1030 / JCM 2381 / KCTC 1655 / WB1 |
| 分子量 | 理論値: 51.267797 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MNYKKVEASD IAAIKELIPA ERVFVGTEIG EDFSHDELGS IHSYPEVLIK VTSTEEVSKI MKYAYEHNIP VVVRGSGTGL VGACVPLFG GIMLETTLMN NILELDTENL TVTVEPGVLL MELSKFVEEN DLFYPPDPGE KSATIAGNIS TNAGGMRAVK Y GVTRDYVR ...文字列: MNYKKVEASD IAAIKELIPA ERVFVGTEIG EDFSHDELGS IHSYPEVLIK VTSTEEVSKI MKYAYEHNIP VVVRGSGTGL VGACVPLFG GIMLETTLMN NILELDTENL TVTVEPGVLL MELSKFVEEN DLFYPPDPGE KSATIAGNIS TNAGGMRAVK Y GVTRDYVR GLTVVLANGE IIELGGKIVK NSSGYSLKDL VIGSEGTLCV ITKAILKLLP LPKMTLSLLI PFENISDAAG IV PKIIKSK AIPTAIEFME RQTILFAEDF LGKKFPDSSS NAYILLTFDG NTKEQVEAEY ETVANLCLAE GAKDVYIVDT VER KDSVWS ARGAFLEAIK ASTTEMDECD VVVPRNRIAE FIEFTHDLAK EMDVRIPSFG HAGDGNLHIY VCRDELCQAD WEAK LAEAM DRMYAKALTF EGLVSGEHGI GYAKRKYLLN DFGTEHLALM AGIKQTFDPK NLLNPKKVCQ MA UniProtKB: Lactate dehydrogenase (NAD(+),ferredoxin) subunit LctD |
-分子 #4: FLAVIN-ADENINE DINUCLEOTIDE
| 分子 | 名称: FLAVIN-ADENINE DINUCLEOTIDE / タイプ: ligand / ID: 4 / コピー数: 6 / 式: FAD |
|---|---|
| 分子量 | 理論値: 785.55 Da |
| Chemical component information |  ChemComp-FAD: |
-分子 #5: FE (III) ION
| 分子 | 名称: FE (III) ION / タイプ: ligand / ID: 5 / コピー数: 2 / 式: FE |
|---|---|
| 分子量 | 理論値: 55.845 Da |
-分子 #6: water
| 分子 | 名称: water / タイプ: ligand / ID: 6 / コピー数: 2 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.8 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
詳細: pH 7.5 | |||||||||
| グリッド | モデル: C-flat-1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 135 sec. / 前処理 - 雰囲気: NITROGEN / 前処理 - 気圧: 38.0 kPa / 詳細: 45mA | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV 詳細: Blot force of +20 and blotting time of 4 seconds before plunging. | |||||||||
| 詳細 | Sample was cross linked with 1 mM of BS3 before grid preparation. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 30 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) デジタル化 - サイズ - 横: 5760 pixel / デジタル化 - サイズ - 縦: 4092 pixel / 実像数: 9788 / 平均露光時間: 6.52 sec. / 平均電子線量: 106.17 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.1 µm / 最小 デフォーカス(公称値): 1.2 µm / 倍率(公称値): 105000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-7qh2: |
 ムービー
ムービー コントローラー
コントローラー







 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)