+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1205 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Three-dimensional structure of a type III glutamine synthetase by single-particle reconstruction. | |||||||||
 マップデータ マップデータ | GSIII from Bacteroides fragilis (negative stain reconstruction) | |||||||||
 試料 試料 |
| |||||||||
| 機能・相同性 | Glutamine synthetase, N-terminal domain 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  Bacteroides fragilis (バクテリア) Bacteroides fragilis (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / ネガティブ染色法 / 解像度: 21.0 Å | |||||||||
 データ登録者 データ登録者 | van Rooyen JM / Abratt VR / Sewell BT | |||||||||
 引用 引用 |  ジャーナル: J Mol Biol / 年: 2006 ジャーナル: J Mol Biol / 年: 2006タイトル: Three-dimensional structure of a type III glutamine synthetase by single-particle reconstruction. 著者: Jason M van Rooyen / Valerie R Abratt / B Trevor Sewell /  要旨: GlnN, the type III glutamine synthetase (GSIII) from the medically important, anaerobic, opportunistic pathogen Bacteroides fragilis, has 82.8 kDa subunits that share only 9% sequence identity with ...GlnN, the type III glutamine synthetase (GSIII) from the medically important, anaerobic, opportunistic pathogen Bacteroides fragilis, has 82.8 kDa subunits that share only 9% sequence identity with the type I glutamine synthetases (GSI), the only family for which a structure is known. Active GlnN was found predominantly in a single peak that eluted from a calibrated gel-filtration chromatography column at a position equaivalent to 0.86(+/-0.08) MDa. Negative-stain electron microscopy enabled the identification of double-ringed particles and single hexameric rings ("pinwheels") resulting from partial staining. A 2D average of these pinwheels showed marked similarity to the corresponding structures found in preparations of GSI, except that the arms of the subunits were 40% longer. Reconstructions from particles embedded in vitreous ice showed that GlnN has a double-ringed, dodecameric structure with a 6-fold dihedral space group (D6) symmetry and dimensions of 17.0 nm parallel with the 6-fold axis and 18.3 nm parallel with the 2-fold axes. The structures, combined with a sequence alignment based on structural principles, showed how many aspects of the structure of GSI, and most notably the alpha/beta barrel fold active site were preserved. There was evidence for the presence of this structure in the reconstructed volume, thus, identifying the indentations between the pinwheel spokes as putative active sites and suggesting conservation of the overall molecular geometry found in GSI despite their low level of global homology. Furthermore, docking of GSI into the reconstruction left sufficient plausibly located unoccupied density to account for the additional residues in GSIII, thus validating the structure. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1205.map.gz emd_1205.map.gz | 86.6 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1205-v30.xml emd-1205-v30.xml emd-1205.xml emd-1205.xml | 9.6 KB 9.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1205.gif 1205.gif | 15.2 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1205 http://ftp.pdbj.org/pub/emdb/structures/EMD-1205 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1205 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1205 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_1205_validation.pdf.gz emd_1205_validation.pdf.gz | 195 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_1205_full_validation.pdf.gz emd_1205_full_validation.pdf.gz | 194.1 KB | 表示 | |
| XML形式データ |  emd_1205_validation.xml.gz emd_1205_validation.xml.gz | 4.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1205 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1205 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1205 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1205 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1205.map.gz / 形式: CCP4 / 大きさ: 1.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1205.map.gz / 形式: CCP4 / 大きさ: 1.9 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | GSIII from Bacteroides fragilis (negative stain reconstruction) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 4.25 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
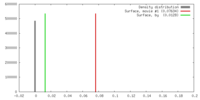
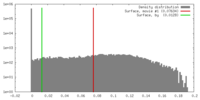
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : B.fragilis GlnN purified from E.coli
| 全体 | 名称: B.fragilis GlnN purified from E.coli |
|---|---|
| 要素 |
|
-超分子 #1000: B.fragilis GlnN purified from E.coli
| 超分子 | 名称: B.fragilis GlnN purified from E.coli / タイプ: sample / ID: 1000 / 集合状態: One dodecamer of GlnN / Number unique components: 1 |
|---|---|
| 分子量 | 実験値: 1.3 MDa / 理論値: 990 KDa / 手法: Calibrated gel-filtration |
-分子 #1: GlnN
| 分子 | 名称: GlnN / タイプ: protein_or_peptide / ID: 1 / Name.synonym: GSIII 詳細: Recombinant GlnN purified from GlnA deficient E.coli mutant; SwissProt P15623 コピー数: 12 / 集合状態: Dodecamer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  Bacteroides fragilis (バクテリア) / 株: B. fragilis BF-1 / 組織: E.coli cytoplasm / 細胞: E.coli Bacteroides fragilis (バクテリア) / 株: B. fragilis BF-1 / 組織: E.coli cytoplasm / 細胞: E.coli |
| 分子量 | 実験値: 990 KDa / 理論値: 1.3 MDa |
| 組換発現 | 生物種:  |
| 配列 | InterPro: Glutamine synthetase, N-terminal domain |
-実験情報
-構造解析
| 手法 | ネガティブ染色法, クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.25 mg/mL |
|---|---|
| 緩衝液 | pH: 7.15 / 詳細: 10 mM Imidazole-HCl, 10 mM MnCl2 |
| 染色 | タイプ: NEGATIVE 詳細: Aliquots (10ul) were applied to 300 mesh copper grids, which had been coated with thin carbon support film and previously glow discharged in air for 20 seconds, before being stained with 2% ...詳細: Aliquots (10ul) were applied to 300 mesh copper grids, which had been coated with thin carbon support film and previously glow discharged in air for 20 seconds, before being stained with 2% uranyl acetate solution using the droplet method. |
| グリッド | 詳細: 300 mesh copper grid |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TECNAI F20 |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: LEO OMEGA |
| 詳細 | Leo 912 TEM |
| 日付 | 2004年5月13日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: PROSCAN TEM-PIV (2k x 2k) デジタル化 - サンプリング間隔: 14 µm / 実像数: 160 詳細: Images were digitized using an Ilford Leafscan and downsized by a factor of 2 ビット/ピクセル: 16 |
| 電子線 | 加速電圧: 120 kV / 電子線源: TUNGSTEN HAIRPIN |
| 電子光学系 | 倍率(補正後): 65882 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 倍率(公称値): 50000 |
| 試料ステージ | 試料ホルダー: Eucentric / 試料ホルダーモデル: OTHER |
| 実験機器 |  モデル: Tecnai F20 / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 想定した対称性 - 点群: C6 (6回回転対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 21.0 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: SPIDER / 使用した粒子像数: 12587 |
|---|---|
| 最終 2次元分類 | クラス数: 166 |
-原子モデル構築 1
| ソフトウェア | 名称: Situs |
|---|---|
| 詳細 | Protocol: rigid body |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 当てはまり具合の基準: CC score |
 ムービー
ムービー コントローラー
コントローラー



 UCSF Chimera
UCSF Chimera







 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)