+Search query
-Structure paper
| Title | Dual BACH1 regulation by complementary SCF-type E3 ligases. |
|---|---|
| Journal, issue, pages | Cell, Vol. 187, Issue 26, Page 7585-7602.e25, Year 2024 |
| Publish date | Dec 26, 2024 |
 Authors Authors | Benedikt Goretzki / Maryam Khoshouei / Martin Schröder / Patrick Penner / Luca Egger / Christine Stephan / Dayana Argoti / Nele Dierlamm / Jimena Maria Rada / Sandra Kapps / Catrin Swantje Müller / Zacharias Thiel / Merve Mutlu / Claude Tschopp / David Furkert / Felix Freuler / Simon Haenni / Laurent Tenaillon / Britta Knapp / Alexandra Hinniger / Philipp Hoppe / Enrico Schmidt / Sascha Gutmann / Mario Iurlaro / Grigory Ryzhakov / César Fernández /   |
| PubMed Abstract | Broad-complex, tramtrack, and bric-à-brac domain (BTB) and CNC homolog 1 (BACH1) is a key regulator of the cellular oxidative stress response and an oncogene that undergoes tight post-translational ...Broad-complex, tramtrack, and bric-à-brac domain (BTB) and CNC homolog 1 (BACH1) is a key regulator of the cellular oxidative stress response and an oncogene that undergoes tight post-translational control by two distinct F-box ubiquitin ligases, SCF and SCF. However, how both ligases recognize BACH1 under oxidative stress is unclear. In our study, we elucidate the mechanism by which FBXO22 recognizes a quaternary degron in a domain-swapped β-sheet of the BACH1 BTB dimer. Cancer-associated mutations and cysteine modifications destabilize the degron and impair FBXO22 binding but simultaneously expose an otherwise shielded degron in the dimer interface, allowing FBXL17 to recognize BACH1 as a monomer. These findings shed light on a ligase switch mechanism that enables post-translational regulation of BACH1 by complementary ligases depending on the stability of its BTB domain. Our results provide mechanistic insights into the oxidative stress response and may spur therapeutic approaches for targeting oxidative stress-related disorders and cancer. |
 External links External links |  Cell / Cell /  PubMed:39657677 PubMed:39657677 |
| Methods | EM (single particle) / X-ray diffraction |
| Resolution | 1.47 - 3.4 Å |
| Structure data | EMDB-19766, PDB-8s7d: EMDB-19768, PDB-8s7e:  PDB-9gp5:  PDB-9gr9:  PDB-9gra: |
| Chemicals |  ChemComp-HOH: 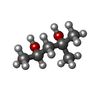 ChemComp-MRD: |
| Source |
|
 Keywords Keywords | LIGASE / SKP1-FBXO22 E3 ligase SCF F-box protein BACH1 BTB / SKP1-FBXO22 E3 ligase SCF F-box protein / DNA BINDING PROTEIN / BACH1 / back-to-back domain / BTB domain |
 Movie
Movie Controller
Controller Structure viewers
Structure viewers About Yorodumi Papers
About Yorodumi Papers







 homo sapiens (human)
homo sapiens (human)