+検索条件
-Structure paper
| タイトル | Structure of human mitochondrial pyruvate carrier MPC1 and MPC2 complex. |
|---|---|
| ジャーナル・号・ページ | Nat Commun, Vol. 16, Issue 1, Page 6700, Year 2025 |
| 掲載日 | 2025年7月21日 |
 著者 著者 | Yingyuan Sun / Yaru Wang / Zheng Xing / Dongyu Li / Rong Wang / Baozhi Chen / Ning Zhou / Alyssa Ayala / Benjamin P Tu / Xiaofeng Qi /  |
| PubMed 要旨 | The Mitochondrial Pyruvate Carrier (MPC) bridges cytosolic and mitochondrial metabolism by transporting pyruvate into mitochondria for ATP production and biosynthesis of various essential molecules. ...The Mitochondrial Pyruvate Carrier (MPC) bridges cytosolic and mitochondrial metabolism by transporting pyruvate into mitochondria for ATP production and biosynthesis of various essential molecules. MPC functions as a heterodimer composed of MPC1 and MPC2 in most mammalian cells. Here, we present the cryogenic electron microscopy (cryo-EM) structures of the human MPC1-2 complex in the mitochondrial intermembrane space (IMS)-open state and the inhibitor-bound in the mitochondrial matrix-open state. Structural analysis shows that the transport channel of MPC is formed by the interaction of transmembrane helix (TM) 1 and TM2 of MPC1 with TM2 and TM1 of MPC2, respectively. UK5099, a potent MPC inhibitor, shares the same binding site with pyruvate at the matrix side of the transport channel, stabilizing MPC in its matrix-open conformation. Notably, a functional W82F mutation in MPC2 leads to the complex in an IMS-open conformation. Structural comparisons across different conformations, combined with yeast rescue assays, reveal the mechanisms of substrate binding and asymmetric conformational changes in MPC during pyruvate transport across the inner mitochondrial membrane (IMM) as well as the inhibitory mechanisms of MPC inhibitors. |
 リンク リンク |  Nat Commun / Nat Commun /  PubMed:40691140 / PubMed:40691140 /  PubMed Central PubMed Central |
| 手法 | EM (単粒子) |
| 解像度 | 2.77 - 6.14 Å |
| 構造データ |  EMDB-70260: Human MPC1-2 Complex EMDB-70261, PDB-9o9s: EMDB-70262, PDB-9o9t:  EMDB-70348: Human MPC1-2 Complex matrix-open  EMDB-70349: Human MPC1-2 Complex matrix-open (TMs weighted)  EMDB-70350: Human MPC1-2 Complex IMS-open  EMDB-70351: Human MPC1-2 Complex IMS-open (TMs weighted) |
| 化合物 | 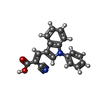 ChemComp-I2R: |
| 由来 |
|
 キーワード キーワード | MEMBRANE PROTEIN |
 ムービー
ムービー コントローラー
コントローラー 構造ビューア
構造ビューア 万見文献について
万見文献について







 homo sapiens (ヒト)
homo sapiens (ヒト)
