+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-5166 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
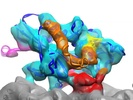
| タイトル | 3D reconstruction of a microtubule decorated with monomeric human kinesin (K349 construct) having AMPPNP bound in the nucleotide pocket. | |||||||||
 マップデータ マップデータ | 3D reconstruction of a microtubule decorated with monomeric human kinesin (K349 construct) with AMPPNP bound in the nucleotide pocket. | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  kinesin (キネシン) / kinesin (キネシン) /  microtubule (微小管) / microtubule (微小管) /  atpase (ATPアーゼ) / atpase (ATPアーゼ) /  molecular motor (分子モーター) / molecular motor (分子モーター) /  myosin (ミオシン) / mechanism / myosin (ミオシン) / mechanism /  motility (運動性) / motility (運動性) /  cytoskeleton (細胞骨格) cytoskeleton (細胞骨格) | |||||||||
| 生物種 | unidentified (未定義) | |||||||||
| 手法 | らせん対称体再構成法 /  クライオ電子顕微鏡法 / 解像度: 9.1 Å クライオ電子顕微鏡法 / 解像度: 9.1 Å | |||||||||
 データ登録者 データ登録者 | Sindelar CV / Downing KH | |||||||||
 引用 引用 |  ジャーナル: Proc Natl Acad Sci U S A / 年: 2010 ジャーナル: Proc Natl Acad Sci U S A / 年: 2010タイトル: An atomic-level mechanism for activation of the kinesin molecular motors. 著者: Charles V Sindelar / Kenneth H Downing /  要旨: Kinesin cytoskeletal motors convert the energy of ATP hydrolysis into stepping movement along microtubules. A partial model of this process has been derived from crystal structures, which show that ...Kinesin cytoskeletal motors convert the energy of ATP hydrolysis into stepping movement along microtubules. A partial model of this process has been derived from crystal structures, which show that movement of the motor domain relative to its major microtubule binding element, the switch II helix, is coupled to docking of kinesin's neck linker element along the motor domain. This docking would displace the cargo in the direction of travel and so contribute to a step. However, the crystal structures do not reveal how ATP binding and hydrolysis govern this series of events. We used cryoelectron microscopy to derive 8-9 A-resolution maps of four nucleotide states encompassing the microtubule-attached kinetic cycle of a kinesin motor. The exceptionally high quality of these maps allowed us to build in crystallographically determined conformations of kinesin's key subcomponents, yielding novel arrangements of kinesin's switch II helix and nucleotide-sensing switch loops. The resulting atomic models reveal a seesaw mechanism in which the switch loops, triggered by ATP binding, propel their side of the motor domain down and thereby elicit docking of the neck linker on the opposite side of the seesaw. Microtubules engage the seesaw mechanism by stabilizing the formation of extra turns at the N terminus of the switch II helix, which then serve as an anchor for the switch loops as they modulate the seesaw angle. These observations explain how microtubules activate kinesin's ATP-sensing machinery to promote cargo displacement and inform the mechanism of kinesin's ancestral relative, myosin. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_5166.map.gz emd_5166.map.gz | 154.9 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-5166-v30.xml emd-5166-v30.xml emd-5166.xml emd-5166.xml | 10 KB 10 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_5166.jpg emd_5166.jpg | 78.8 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-5166 http://ftp.pdbj.org/pub/emdb/structures/EMD-5166 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-5166 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-5166 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_5166.map.gz / 形式: CCP4 / 大きさ: 165 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_5166.map.gz / 形式: CCP4 / 大きさ: 165 KB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | 3D reconstruction of a microtubule decorated with monomeric human kinesin (K349 construct) with AMPPNP bound in the nucleotide pocket. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 2.1167 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Microtubule decorated with monomeric human kinesin (K349 construc...
| 全体 | 名称: Microtubule decorated with monomeric human kinesin (K349 construct) having AMPPNP bound in the nucleotide pocket. |
|---|---|
| 要素 |
|
-超分子 #1000: Microtubule decorated with monomeric human kinesin (K349 construc...
| 超分子 | 名称: Microtubule decorated with monomeric human kinesin (K349 construct) having AMPPNP bound in the nucleotide pocket. タイプ: sample / ID: 1000 / Number unique components: 2 |
|---|
-分子 #1: K349
| 分子 | 名称: K349 / タイプ: protein_or_peptide / ID: 1 / Name.synonym: Monomeric human kinesin construct / 組換発現: Yes / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種: unidentified (未定義) |
-分子 #2: Microtubule
| 分子 | 名称: Microtubule / タイプ: protein_or_peptide / ID: 2 / Name.synonym: Microtubule / 組換発現: Yes / データベース: NCBI |
|---|---|
| 由来(天然) | 生物種: unidentified (未定義) |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 緩衝液 | pH: 6.8 / 詳細: 25mM Pipes, 25mM NaCl, 2mM MgCl2, 1mM EGTA |
|---|---|
| グリッド | 詳細: 300 mesh copper grid with homemade holey carbon |
| 凍結 | 凍結剤: ETHANE / 装置: HOMEMADE PLUNGER / 詳細: Vitrification instrument: Homemade |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | JEOL 4000EX |
|---|---|
| 電子線 | 加速電圧: 400 kV / 電子線源: LAB6 |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 4.1 mm / 最大 デフォーカス(公称値): 1.6 µm / 最小 デフォーカス(公称値): 0.7 µm / 倍率(公称値): 60000 Bright-field microscopy / Cs: 4.1 mm / 最大 デフォーカス(公称値): 1.6 µm / 最小 デフォーカス(公称値): 0.7 µm / 倍率(公称値): 60000 |
| 試料ステージ | 試料ホルダー: Eucentric / 試料ホルダーモデル: GATAN LIQUID NITROGEN |
| 温度 | 平均: 105 K |
| 日付 | 2008年1月21日 |
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM デジタル化 - スキャナー: NIKON SUPER COOLSCAN 9000 デジタル化 - サンプリング間隔: 6.35 µm / 実像数: 98 / 平均電子線量: 15 e/Å2 / ビット/ピクセル: 16 |
- 画像解析
画像解析
| CTF補正 | 詳細: done within FREALIGN |
|---|---|
| 最終 再構成 | アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 9.1 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: SPIDER,FREALIGN 詳細: Approximately 190,000 asymmetric units were averaged in the final reconstruction. |
-原子モデル構築 1
| 初期モデル | PDB ID: |
|---|---|
| ソフトウェア | 名称:  UCSF Chimera UCSF Chimera |
| 詳細 | Protocol: Rigid Body. Regions in the crystal structure whose structure were found to differ from the EM map were excluded from the fitting procedure. These regions corresponded to the switch loops, helices alpha 3 and alpha 4 (switch II helix), and the neck linker. |
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT / 当てはまり具合の基準: Cross correlation |
 ムービー
ムービー コントローラー
コントローラー