+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4098 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM reconstruction of bacteriophage AP205 virus-like particles. | |||||||||
 マップデータ マップデータ | Bacteriophage AP205 cryo-EM map | |||||||||
 試料 試料 | AP205 != Acinetobacter phage AP205 AP205
| |||||||||
| 機能・相同性 |  カプシド / Coat protein カプシド / Coat protein 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   Acinetobacter phage AP205 (ファージ) Acinetobacter phage AP205 (ファージ) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 6.0 Å クライオ電子顕微鏡法 / 解像度: 6.0 Å | |||||||||
 データ登録者 データ登録者 | Diebolder CA / Rumnieks J / Tars K / Koning RI | |||||||||
 引用 引用 |  ジャーナル: J Mol Biol / 年: 2016 ジャーナル: J Mol Biol / 年: 2016タイトル: Structure of AP205 Coat Protein Reveals Circular Permutation in ssRNA Bacteriophages. 著者: Mihails Shishovs / Janis Rumnieks / Christoph Diebolder / Kristaps Jaudzems / Loren B Andreas / Jan Stanek / Andris Kazaks / Svetlana Kotelovica / Inara Akopjana / Guido Pintacuda / Roman I ...著者: Mihails Shishovs / Janis Rumnieks / Christoph Diebolder / Kristaps Jaudzems / Loren B Andreas / Jan Stanek / Andris Kazaks / Svetlana Kotelovica / Inara Akopjana / Guido Pintacuda / Roman I Koning / Kaspars Tars /    要旨: AP205 is a single-stranded RNA bacteriophage that has a coat protein sequence not similar to any other known single-stranded RNA phage. Here, we report an atomic-resolution model of the AP205 virus- ...AP205 is a single-stranded RNA bacteriophage that has a coat protein sequence not similar to any other known single-stranded RNA phage. Here, we report an atomic-resolution model of the AP205 virus-like particle based on a crystal structure of an unassembled coat protein dimer and a cryo-electron microscopy reconstruction of the assembled particle, together with secondary structure information from site-specific solid-state NMR data. The AP205 coat protein dimer adopts the conserved Leviviridae coat protein fold except for the N-terminal region, which forms a beta-hairpin in the other known single-stranded RNA phages. AP205 has a similar structure at the same location formed by N- and C-terminal beta-strands, making it a circular permutant compared to the other coat proteins. The permutation moves the coat protein termini to the most surface-exposed part of the assembled particle, which explains its increased tolerance to long N- and C-terminal fusions. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4098.map.gz emd_4098.map.gz | 226.4 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4098-v30.xml emd-4098-v30.xml emd-4098.xml emd-4098.xml | 12.6 KB 12.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
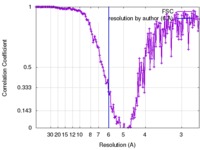
| FSC (解像度算出) |  emd_4098_fsc.xml emd_4098_fsc.xml | 16.4 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_4098.png emd_4098.png | 225.9 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4098 http://ftp.pdbj.org/pub/emdb/structures/EMD-4098 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4098 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4098 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4098.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4098.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Bacteriophage AP205 cryo-EM map | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.34 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : AP205
| 全体 | 名称: AP205 |
|---|---|
| 要素 |
|
-超分子 #1: Acinetobacter phage AP205
| 超分子 | 名称: Acinetobacter phage AP205 / タイプ: virus / ID: 1 / 親要素: 0 / 含まれる分子: all / NCBI-ID: 154784 / 生物種: Acinetobacter phage AP205 / ウイルスタイプ: VIRUS-LIKE PARTICLE / ウイルス・単離状態: SPECIES / ウイルス・エンベロープ: No / ウイルス・中空状態: No |
|---|
-分子 #1: Coat protein
| 分子 | 名称: Coat protein / タイプ: protein_or_peptide / ID: 1 / コピー数: 180 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Acinetobacter phage AP205 (ファージ) Acinetobacter phage AP205 (ファージ) |
| 分子量 | 理論値: 13.820569 KDa |
| 組換発現 | 生物種:   Escherichia coli (大腸菌) Escherichia coli (大腸菌) |
| 配列 | 文字列: ANKPMQPITS TANKIVWSDP TRLSTTFSAS LLRQRVKVGI AELNNVSGQY VSVYKRPAPK PEGCADACVI MPNENQSIRT VISGSAENL ATLKAEWETH KRNVDTLFAS GNAGLGFLDP TAAIVSSDTT |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 400 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 雰囲気: AIR |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 298 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 最大 デフォーカス(補正後): 2.5 µm / 最小 デフォーカス(補正後): 1.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 59000 Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.0 µm / 倍率(公称値): 59000 |
| 特殊光学系 | エネルギーフィルター - 名称: FEI SFEG |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 撮影 | フィルム・検出器のモデル: FEI FALCON II (4k x 4k) 検出モード: INTEGRATING / デジタル化 - 画像ごとのフレーム数: 1-7 / 平均電子線量: 8.0 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー