+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-8191 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of lactate dehydrogenase (LDH) in complex with GSK2837808A | |||||||||
 マップデータ マップデータ | Lactate dehydrogenase (LDH) in complex with GSK2837808A | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード |  lactate dehydrogenase (乳酸脱水素酵素) / small metabolic complex / small molecule inhibitor / lactate dehydrogenase (乳酸脱水素酵素) / small metabolic complex / small molecule inhibitor /  OXIDOREDUCTASE (酸化還元酵素) OXIDOREDUCTASE (酸化還元酵素) | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 ピルビン酸 / ピルビン酸 /  ピルビン酸 / ピルビン酸 /  乳酸脱水素酵素 / 乳酸脱水素酵素 /  L-lactate dehydrogenase activity / carboxylic acid metabolic process / carbohydrate metabolic process / L-lactate dehydrogenase activity / carboxylic acid metabolic process / carbohydrate metabolic process /  細胞質基質 細胞質基質類似検索 - 分子機能 | |||||||||
| 生物種 |   Gallus gallus (ニワトリ) Gallus gallus (ニワトリ) | |||||||||
| 手法 |  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 2.8 Å クライオ電子顕微鏡法 / 解像度: 2.8 Å | |||||||||
 データ登録者 データ登録者 | Merk A / Bartesaghi A | |||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2016 ジャーナル: Cell / 年: 2016タイトル: Breaking Cryo-EM Resolution Barriers to Facilitate Drug Discovery. 著者: Alan Merk / Alberto Bartesaghi / Soojay Banerjee / Veronica Falconieri / Prashant Rao / Mindy I Davis / Rajan Pragani / Matthew B Boxer / Lesley A Earl / Jacqueline L S Milne / Sriram Subramaniam /  要旨: Recent advances in single-particle cryoelecton microscopy (cryo-EM) are enabling generation of numerous near-atomic resolution structures for well-ordered protein complexes with sizes ≥ ∼200 kDa. ...Recent advances in single-particle cryoelecton microscopy (cryo-EM) are enabling generation of numerous near-atomic resolution structures for well-ordered protein complexes with sizes ≥ ∼200 kDa. Whether cryo-EM methods are equally useful for high-resolution structural analysis of smaller, dynamic protein complexes such as those involved in cellular metabolism remains an important question. Here, we present 3.8 Å resolution cryo-EM structures of the cancer target isocitrate dehydrogenase (93 kDa) and identify the nature of conformational changes induced by binding of the allosteric small-molecule inhibitor ML309. We also report 2.8-Å- and 1.8-Å-resolution structures of lactate dehydrogenase (145 kDa) and glutamate dehydrogenase (334 kDa), respectively. With these results, two perceived barriers in single-particle cryo-EM are overcome: (1) crossing 2 Å resolution and (2) obtaining structures of proteins with sizes < 100 kDa, demonstrating that cryo-EM can be used to investigate a broad spectrum of drug-target interactions and dynamic conformational states. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_8191.map.gz emd_8191.map.gz | 19.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-8191-v30.xml emd-8191-v30.xml emd-8191.xml emd-8191.xml | 16.6 KB 16.6 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_8191.png emd_8191.png | 169.7 KB | ||
| Filedesc metadata |  emd-8191.cif.gz emd-8191.cif.gz | 6.1 KB | ||
| その他 |  emd_8191_additional.map.gz emd_8191_additional.map.gz | 19.9 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-8191 http://ftp.pdbj.org/pub/emdb/structures/EMD-8191 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8191 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-8191 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_8191.map.gz / 形式: CCP4 / 大きさ: 22.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_8191.map.gz / 形式: CCP4 / 大きさ: 22.2 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Lactate dehydrogenase (LDH) in complex with GSK2837808A | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.495 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
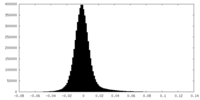
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
-追加マップ: Map sharpened using a B-factor of -150
| ファイル | emd_8191_additional.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Map sharpened using a B-factor of -150 | ||||||||||||
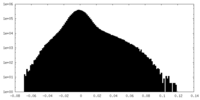
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Lactate dehydrogenase (LDH) in complex with GSK2837808A
| 全体 | 名称: Lactate dehydrogenase (LDH) in complex with GSK2837808A |
|---|---|
| 要素 |
|
-超分子 #1: Lactate dehydrogenase (LDH) in complex with GSK2837808A
| 超分子 | 名称: Lactate dehydrogenase (LDH) in complex with GSK2837808A タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Gallus gallus (ニワトリ) Gallus gallus (ニワトリ) |
| 分子量 | 理論値: 145 KDa |
-分子 #1: L-lactate dehydrogenase B chain
| 分子 | 名称: L-lactate dehydrogenase B chain / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO / EC番号:  乳酸脱水素酵素 乳酸脱水素酵素 |
|---|---|
| 由来(天然) | 生物種:   Gallus gallus (ニワトリ) Gallus gallus (ニワトリ) |
| 分子量 | 理論値: 36.115656 KDa |
| 組換発現 | 生物種:  Bacteria (細菌) Bacteria (細菌) |
| 配列 | 文字列: ATLKEKLITP VAAGSTVPSN KITVVGVGQV GMACAISILG KGLCDELALV DVLEDKLKGE MMDLQHGSLF LQTHKIVADK DYAVTANSK IVVVTAGVRQ QEGESRLNLV QRNVNVFKFI IPQIVKYSPN CTILVVSNPV DILTYVTWKL SGLPKHRVIG S GCNLDTAR ...文字列: ATLKEKLITP VAAGSTVPSN KITVVGVGQV GMACAISILG KGLCDELALV DVLEDKLKGE MMDLQHGSLF LQTHKIVADK DYAVTANSK IVVVTAGVRQ QEGESRLNLV QRNVNVFKFI IPQIVKYSPN CTILVVSNPV DILTYVTWKL SGLPKHRVIG S GCNLDTAR FRYLMAERLG IHPTSCHGWI LGEHGDSSVA VWSGVNVAGV SLQELNPAMG TDKDSENWKE VHKQVVESAY EV IRLKGYT NWAIGLSVAE LCETMLKNLY RVHSVSTLVK GTYGIENDVF LSLPCVLSAS GLTSVINQKL KDDEVAQLKK SAD TLWSIQ KDLKD UniProtKB: L-lactate dehydrogenase B chain |
-分子 #2: water
| 分子 | 名称: water / タイプ: ligand / ID: 2 / コピー数: 41 / 式: HOH |
|---|---|
| 分子量 | 理論値: 18.015 Da |
| Chemical component information |  ChemComp-HOH: |
-実験情報
-構造解析
| 手法 |  クライオ電子顕微鏡法 クライオ電子顕微鏡法 |
|---|---|
 解析 解析 |  単粒子再構成法 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.5 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 / 構成要素 - 名称: PBS / 詳細: Phosphate-buffered saline |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: PLASMA CLEANING |
| 凍結 | 凍結剤: ETHANE / 装置: LEICA EM GP / 詳細: Plunged into liquid ethane (LEICE EM GP). |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 倍率(補正後): 101000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 270000 Bright-field microscopy / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.2 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 270000 |
| 特殊光学系 | エネルギーフィルター - 名称: GIF Quantum エネルギーフィルター - エネルギー下限: 0 eV エネルギーフィルター - エネルギー上限: 20 eV |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 温度 | 最低: 79.6 K / 最高: 79.8 K |
| 撮影 | フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 検出モード: SUPER-RESOLUTION / デジタル化 - 画像ごとのフレーム数: 0-29 / 実像数: 1707 / 平均露光時間: 0.2 sec. / 平均電子線量: 60.0 e/Å2 |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 粒子像選択 | 選択した数: 508402 |
|---|---|
| 初期モデル | モデルのタイプ: OTHER |
| 初期 角度割当 | タイプ: PROJECTION MATCHING / ソフトウェア - 名称: FREALIGN (ver. 9.10) |
| 最終 角度割当 | タイプ: PROJECTION MATCHING / ソフトウェア - 名称: FREALIGN (ver. 9.10) |
| 最終 再構成 | 想定した対称性 - 点群: D2 (2回x2回 2面回転対称 ) )アルゴリズム: FOURIER SPACE / 解像度のタイプ: BY AUTHOR / 解像度: 2.8 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: FREALIGN (ver. 9.10) 詳細: The primary map in this entry corresponds to the uncorrected reconstruction. A version sharpened using a B-factor of -150 is provided as additional volume data. 使用した粒子像数: 50865 |
 ムービー
ムービー コントローラー
コントローラー























 Z
Z Y
Y X
X