[English] 日本語
 Yorodumi
Yorodumi- PDB-1rg0: Monoclinic crystal form of the truncated K122-4 pilin from Pseudo... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 1rg0 | ||||||
|---|---|---|---|---|---|---|---|
| Title | Monoclinic crystal form of the truncated K122-4 pilin from Pseudomonas aeruginosa | ||||||
 Components Components | Fimbrial protein | ||||||
 Keywords Keywords |  CELL ADHESION / Type IV Pilin / CELL ADHESION / Type IV Pilin /  Lectin / Adhesin / Lectin / Adhesin /  Pseudomonas Pseudomonas | ||||||
| Function / homology |  Function and homology information Function and homology information glycosphingolipid binding / biological process involved in interaction with host / glycosphingolipid binding / biological process involved in interaction with host /  pilus / pilus /  periplasmic space / periplasmic space /  cell adhesion / cell adhesion /  membrane membraneSimilarity search - Function | ||||||
| Biological species |   Pseudomonas aeruginosa (bacteria) Pseudomonas aeruginosa (bacteria) | ||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 1.8 Å MOLECULAR REPLACEMENT / Resolution: 1.8 Å | ||||||
 Authors Authors | Audette, G.F. / Irvin, R.T. / Hazes, B. | ||||||
 Citation Citation |  Journal: Biochemistry / Year: 2004 Journal: Biochemistry / Year: 2004Title: Crystallographic Analysis of the Pseudomonas aeruginosa Strain K122-4 Monomeric Pilin Reveals a Conserved Receptor-Binding Architecture Authors: Audette, G.F. / Irvin, R.T. / Hazes, B. #1:  Journal: Acta Crystallogr.,Sect.D / Year: 2003 Journal: Acta Crystallogr.,Sect.D / Year: 2003Title: Purification, crystallization and preliminary diffraction studies of the Pseudomonas aeruginosa strain K122-4 monomeric pilin Authors: Audette, G.F. / Irvin, R.T. / Hazes, B. | ||||||
| History |
| ||||||
| Remark 300 | BIOMOLECULE: THIS ENTRY CONTAINS THE CRYSTALLOGRAPHIC ASYMMETRIC UNIT WHICH CONSISTS OF 2 CHAIN(S). ...BIOMOLECULE: THIS ENTRY CONTAINS THE CRYSTALLOGRAPHIC ASYMMETRIC UNIT WHICH CONSISTS OF 2 CHAIN(S). FOR AN EXPLANATION OF THE BIOLOGICAL UNIT, PLEASE REFER TO THE FOLLOWING REFERENCES: Parge, H.E., Forest, K.T., Hickey, M.J., Christensen, D.A., Getzoff, E.D., Tainer, J.A.: Structure of the fibre-forming protein pilin at 2.6 A resolution. Nature 378 pp. 32 (1995). Keizer, D.W., Slupsky, C.M., Kalisiak, M., Campbell, A.P., Crump, M.P., Sastry, P.A., Hazes, B., Irvin, R.T., Sykes, B.D.: Structure of a Pilin Monomer from Pseudomonas Aeruginosa. Implications for the Assembly of Pili. J.Biol.Chem. 276 pp. 24186 (2001). | ||||||
| Remark 999 | SEQUENCE THE AUTHORS STATE THE PROTEIN SEQUENCE AT RESIDUE 36 IS IS PROBABLY A SEQUENCING ERROR. |
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  1rg0.cif.gz 1rg0.cif.gz | 61.6 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb1rg0.ent.gz pdb1rg0.ent.gz | 44.6 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  1rg0.json.gz 1rg0.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/rg/1rg0 https://data.pdbj.org/pub/pdb/validation_reports/rg/1rg0 ftp://data.pdbj.org/pub/pdb/validation_reports/rg/1rg0 ftp://data.pdbj.org/pub/pdb/validation_reports/rg/1rg0 | HTTPS FTP |
|---|
-Related structure data
| Related structure data |  1qveSC S: Starting model for refinement C: citing same article ( |
|---|---|
| Similar structure data |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||||||||||||
| Unit cell |
| ||||||||||||||||||
| Noncrystallographic symmetry (NCS) | NCS domain:
NCS domain segments: Component-ID: 1 / Ens-ID: 1 / Beg auth comp-ID: GLN / Beg label comp-ID: GLN / End auth comp-ID: CYS / End label comp-ID: CYS / Refine code: 6 / Auth seq-ID: 32 - 142 / Label seq-ID: 8 - 118
| ||||||||||||||||||
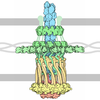
| Details | The type IV pilins are initially produced as integral inner membrane proteins that are subsequently assembled into a helical fiber. This entry contains the crystallographic asymmetric unit which consists of 2 chain(s). For an explanation of the biological unit, please refer to the following references: Parge, H.E., Forest, K.T., Hickey, M.J., Christensen, D.A., Getzoff, E.D., Tainer, J.A.: Structure of the Fibre-Forming Protein Pilin at 2.6 A Resolution. Nature 378 PP. 32 (1995). Keizer, D.W., Slupsky, C.M., Kalisiak, M., Campbell, A.P., Crump, M.P., Sastry, P.A., Hazes, B., Irvin, R.T., Sykes, B.D.: Structure of a Pillin Monomer from Pseudomonas aeruginosa. Implications for the Assembly of Pili. J. Biol. Chem. 276, PP 2418 (2001). |
- Components
Components
| #1: Protein | Mass: 12845.372 Da / Num. of mol.: 2 Source method: isolated from a genetically manipulated source Source: (gene. exp.)   Pseudomonas aeruginosa (bacteria) / Strain: K122-4 / Gene: PILA, FIMA / Plasmid: pMAL-p2X / Production host: Pseudomonas aeruginosa (bacteria) / Strain: K122-4 / Gene: PILA, FIMA / Plasmid: pMAL-p2X / Production host:   Escherichia coli (E. coli) / Strain (production host): ER2507 / References: UniProt: P17838 Escherichia coli (E. coli) / Strain (production host): ER2507 / References: UniProt: P17838#2: Water | ChemComp-HOH / |  Water Water |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.1 Å3/Da / Density % sol: 41.56 % |
|---|---|
Crystal grow | Temperature: 295 K / Method: vapor diffusion, hanging drop / pH: 5.8 Details: PEG 4000, Potassium Phosphate Monobasic, Sodium Cacodylate, Tris HCl, pH 5.8, VAPOR DIFFUSION, HANGING DROP, temperature 295K |
-Data collection
| Diffraction | Mean temperature: 100 K |
|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  ALS ALS  / Beamline: 8.3.1 / Wavelength: 1.1 Å / Beamline: 8.3.1 / Wavelength: 1.1 Å |
| Detector | Type: ADSC QUANTUM 315 / Detector: CCD / Date: Jul 20, 2003 |
| Radiation | Monochromator: Double Crystal Monochromator / Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray |
| Radiation wavelength | Wavelength : 1.1 Å / Relative weight: 1 : 1.1 Å / Relative weight: 1 |
| Reflection | Resolution: 1.51→40.49 Å / Num. obs: 25475 / % possible obs: 78.5 % / Observed criterion σ(F): 0 / Observed criterion σ(I): 0 / Redundancy: 2.8 % / Biso Wilson estimate: 22.1 Å2 / Rsym value: 0.195 / Net I/σ(I): 9.3 |
| Reflection shell | Resolution: 1.51→1.63 Å / Redundancy: 1.7 % / Mean I/σ(I) obs: 0.6 / Num. unique all: 2771 / Rsym value: 0.01068 / % possible all: 68 |
- Processing
Processing
| Software |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure : :  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: PDB Entry 1QVE Resolution: 1.8→40.49 Å / Cor.coef. Fo:Fc: 0.912 / Cor.coef. Fo:Fc free: 0.9 / SU B: 6.062 / SU ML: 0.184 / TLS residual ADP flag: LIKELY RESIDUAL / Isotropic thermal model: Isotropic / Cross valid method: THROUGHOUT / σ(F): 0 / ESU R: 0.209 / ESU R Free: 0.162 / Stereochemistry target values: MAXIMUM LIKELIHOOD / Details: HYDROGENS HAVE BEEN ADDED IN THE RIDING POSITIONS
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Ion probe radii: 0.8 Å / Shrinkage radii: 0.8 Å / VDW probe radii: 1.4 Å / Solvent model: BABINET MODEL WITH MASK | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso mean: 12.106 Å2
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine analyze | Luzzati coordinate error obs: 0.27 Å | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: LAST / Resolution: 1.8→40.49 Å
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints NCS | Dom-ID: 1 / Auth asym-ID: A / Ens-ID: 1 / Number: 1480 / Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Resolution: 1.8→1.847 Å / Total num. of bins used: 20
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS params. | Method: refined / Refine-ID: X-RAY DIFFRACTION
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement TLS group |
|
 Movie
Movie Controller
Controller

















 PDBj
PDBj