+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8qa4 | ||||||
|---|---|---|---|---|---|---|---|
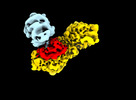
| タイトル | MTHFR + SAH symmetric dis-inhibited state | ||||||
 要素 要素 | Methylenetetrahydrofolate reductase (NADPH) | ||||||
 キーワード キーワード |  FLAVOPROTEIN (フラボタンパク質) / Dis-inhibited / FLAVOPROTEIN (フラボタンパク質) / Dis-inhibited /  allosteric (アロステリック効果) / allosteric (アロステリック効果) /  folate (葉酸) / folate (葉酸) /  S-adenosylhomocysteine (S-アデノシル-L-ホモシステイン) S-adenosylhomocysteine (S-アデノシル-L-ホモシステイン) | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報methylenetetrahydrofolate reductase (NADPH) / response to vitamin B2 / methylenetetrahydrofolate reductase (NADPH) activity /  methylenetetrahydrofolate reductase (NAD(P)H) activity / methionine metabolic process / modified amino acid binding / homocysteine metabolic process / S-adenosylmethionine metabolic process / methionine biosynthetic process / Metabolism of folate and pterines ...methylenetetrahydrofolate reductase (NADPH) / response to vitamin B2 / methylenetetrahydrofolate reductase (NADPH) activity / methylenetetrahydrofolate reductase (NAD(P)H) activity / methionine metabolic process / modified amino acid binding / homocysteine metabolic process / S-adenosylmethionine metabolic process / methionine biosynthetic process / Metabolism of folate and pterines ...methylenetetrahydrofolate reductase (NADPH) / response to vitamin B2 / methylenetetrahydrofolate reductase (NADPH) activity /  methylenetetrahydrofolate reductase (NAD(P)H) activity / methionine metabolic process / modified amino acid binding / homocysteine metabolic process / S-adenosylmethionine metabolic process / methionine biosynthetic process / Metabolism of folate and pterines / response to folic acid / tetrahydrofolate interconversion / heterochromatin organization / response to amino acid / FAD binding / response to interleukin-1 / neural tube closure / methylenetetrahydrofolate reductase (NAD(P)H) activity / methionine metabolic process / modified amino acid binding / homocysteine metabolic process / S-adenosylmethionine metabolic process / methionine biosynthetic process / Metabolism of folate and pterines / response to folic acid / tetrahydrofolate interconversion / heterochromatin organization / response to amino acid / FAD binding / response to interleukin-1 / neural tube closure /  NADP binding / NADP binding /  flavin adenine dinucleotide binding / response to hypoxia / response to xenobiotic stimulus / protein-containing complex binding / flavin adenine dinucleotide binding / response to hypoxia / response to xenobiotic stimulus / protein-containing complex binding /  細胞質基質 細胞質基質類似検索 - 分子機能 | ||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 2.8 Å クライオ電子顕微鏡法 / 解像度: 2.8 Å | ||||||
 データ登録者 データ登録者 | Blomgren, L.K.M. / Yue, W.W. / Froese, D.S. / McCorvie, T.J. | ||||||
| 資金援助 |  スイス, 1件 スイス, 1件
| ||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Dynamic inter-domain transformations mediate the allosteric regulation of human 5, 10-methylenetetrahydrofolate reductase. 著者: Linnea K M Blomgren / Melanie Huber / Sabrina R Mackinnon / Céline Bürer / Arnaud Baslé / Wyatt W Yue / D Sean Froese / Thomas J McCorvie /   要旨: 5,10-methylenetetrahydrofolate reductase (MTHFR) commits folate-derived one-carbon units to generate the methyl-donor S-adenosyl-L-methionine (SAM). Eukaryotic MTHFR appends to the well-conserved ...5,10-methylenetetrahydrofolate reductase (MTHFR) commits folate-derived one-carbon units to generate the methyl-donor S-adenosyl-L-methionine (SAM). Eukaryotic MTHFR appends to the well-conserved catalytic domain (CD) a unique regulatory domain (RD) that confers feedback inhibition by SAM. Here we determine the cryo-electron microscopy structures of human MTHFR bound to SAM and its demethylated product S-adenosyl-L-homocysteine (SAH). In the active state, with the RD bound to a single SAH, the CD is flexible and exposes its active site for catalysis. However, in the inhibited state the RD pocket is remodelled, exposing a second SAM-binding site that was previously occluded. Dual-SAM bound MTHFR demonstrates a substantially rearranged inter-domain linker that reorients the CD, inserts a loop into the active site, positions Tyr404 to bind the cofactor FAD, and blocks substrate access. Our data therefore explain the long-distance regulatory mechanism of MTHFR inhibition, underpinned by the transition between dual-SAM and single-SAH binding in response to cellular methylation status. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8qa4.cif.gz 8qa4.cif.gz | 199.9 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8qa4.ent.gz pdb8qa4.ent.gz | 153.4 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8qa4.json.gz 8qa4.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/qa/8qa4 https://data.pdbj.org/pub/pdb/validation_reports/qa/8qa4 ftp://data.pdbj.org/pub/pdb/validation_reports/qa/8qa4 ftp://data.pdbj.org/pub/pdb/validation_reports/qa/8qa4 | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  18298MC  8qa5C  8qa6C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 75461.195 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: MTHFR Homo sapiens (ヒト) / 遺伝子: MTHFR発現宿主:   Spodoptera frugiperda (ツマジロクサヨトウ) Spodoptera frugiperda (ツマジロクサヨトウ)参照: UniProt: P42898 #2: 化合物 |  S-アデノシル-L-ホモシステイン S-アデノシル-L-ホモシステイン#3: 水 | ChemComp-HOH / |  水 水研究の焦点であるリガンドがあるか | Y | |
|---|
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: Human 5,10-methylenetetrahydrofolate reductase in complex with S-Adenosyl-L-homocysteine, regulatory domains タイプ: COMPLEX / Entity ID: #1 / 由来: RECOMBINANT |
|---|---|
| 分子量 | 値: 0.15 MDa / 実験値: NO |
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 由来(組換発現) | 生物種:   Spodoptera frugiperda (ツマジロクサヨトウ) Spodoptera frugiperda (ツマジロクサヨトウ) |
| 緩衝液 | pH: 7.5 詳細: 20 mM HEPES, pH 7.5, 150 mM NaCl, 0.0025% Tween20, 1 mM S-Adenosyl-L-homocysteine, filter sterilised |
| 試料 | 濃度: 2 mg/ml / 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES |
| 試料支持 | グリッドの材料: GOLD / グリッドのサイズ: 300 divisions/in. / グリッドのタイプ: UltrAuFoil R1.2/1.3 |
急速凍結 | 装置: FEI VITROBOT MARK III / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 295 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 顕微鏡 | モデル: TFS GLACIOS |
|---|---|
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 200 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 200 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 倍率(公称値): 240000 X / 最大 デフォーカス(公称値): 2100 nm / 最小 デフォーカス(公称値): 900 nm / Cs Bright-field microscopy / 倍率(公称値): 240000 X / 最大 デフォーカス(公称値): 2100 nm / 最小 デフォーカス(公称値): 900 nm / Cs : 2.7 mm / C2レンズ絞り径: 100 µm : 2.7 mm / C2レンズ絞り径: 100 µm |
| 試料ホルダ | 凍結剤: NITROGEN |
| 撮影 | 平均露光時間: 5.18 sec. / 電子線照射量: 50 e/Å2 フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 撮影したグリッド数: 2 / 実像数: 5606 |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 1900000 | ||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性 : C2 (2回回転対称 : C2 (2回回転対称 ) ) | ||||||||||||||||||||||||||||||||||||||||
3次元再構成 | 解像度: 2.8 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 105879 / アルゴリズム: FOURIER SPACE / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | B value: 90.1 / プロトコル: FLEXIBLE FIT / 空間: REAL / Target criteria: Cross-correlation coeficient | ||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 6fcx PDB chain-ID: A / Accession code: 6fcx / Source name: PDB / タイプ: experimental model | ||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー




 PDBj
PDBj




