+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7xd0 | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
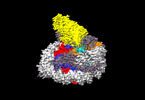
| タイトル | cryo-EM structure of H2BK34ub nucleosome | ||||||||||||||||||||||||
 要素 要素 |
| ||||||||||||||||||||||||
 キーワード キーワード |  NUCLEAR PROTEIN / H2BK34ub nucleosome NUCLEAR PROTEIN / H2BK34ub nucleosome | ||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 nucleosome assembly / structural constituent of chromatin / nucleosome assembly / structural constituent of chromatin /  ヌクレオソーム / ヌクレオソーム /  リボソーム / structural constituent of ribosome / リボソーム / structural constituent of ribosome /  翻訳 (生物学) / protein heterodimerization activity / 翻訳 (生物学) / protein heterodimerization activity /  DNA binding / DNA binding /  細胞核 / 細胞核 /  細胞質 細胞質類似検索 - 分子機能 | ||||||||||||||||||||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト)synthetic construct (人工物) | ||||||||||||||||||||||||
| 手法 |  電子顕微鏡法 / 電子顕微鏡法 /  単粒子再構成法 / 単粒子再構成法 /  クライオ電子顕微鏡法 / 解像度: 3.48 Å クライオ電子顕微鏡法 / 解像度: 3.48 Å | ||||||||||||||||||||||||
 データ登録者 データ登録者 | Ai, H.S. / Liu, A.J. / Lou, Z.Y. / Liu, L. | ||||||||||||||||||||||||
| 資金援助 |  中国, 7件 中国, 7件
| ||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Chem Biol / 年: 2022 ジャーナル: Nat Chem Biol / 年: 2022タイトル: H2B Lys34 Ubiquitination Induces Nucleosome Distortion to Stimulate Dot1L Activity. 著者: Huasong Ai / Maoshen Sun / Aijun Liu / Zixian Sun / Tingting Liu / Lin Cao / Lujun Liang / Qian Qu / Zichen Li / Zhiheng Deng / Zebin Tong / Guochao Chu / Xiaolin Tian / Haiteng Deng / Suwen ...著者: Huasong Ai / Maoshen Sun / Aijun Liu / Zixian Sun / Tingting Liu / Lin Cao / Lujun Liang / Qian Qu / Zichen Li / Zhiheng Deng / Zebin Tong / Guochao Chu / Xiaolin Tian / Haiteng Deng / Suwen Zhao / Jia-Bin Li / Zhiyong Lou / Lei Liu /  要旨: Ubiquitination-dependent histone crosstalk plays critical roles in chromatin-associated processes and is highly associated with human diseases. Mechanism studies of the crosstalk have been of the ...Ubiquitination-dependent histone crosstalk plays critical roles in chromatin-associated processes and is highly associated with human diseases. Mechanism studies of the crosstalk have been of the central focus. Here our study on the crosstalk between H2BK34ub and Dot1L-catalyzed H3K79me suggests a novel mechanism of ubiquitination-induced nucleosome distortion to stimulate the activity of an enzyme. We determined the cryo-electron microscopy structures of Dot1L-H2BK34ub nucleosome complex and the H2BK34ub nucleosome alone. The structures reveal that H2BK34ub induces an almost identical orientation and binding pattern of Dot1L on nucleosome as H2BK120ub, which positions Dot1L for the productive conformation through direct ubiquitin-enzyme contacts. However, H2BK34-anchored ubiquitin does not directly interact with Dot1L as occurs in the case of H2BK120ub, but rather induces DNA and histone distortion around the modified site. Our findings establish the structural framework for understanding the H2BK34ub-H3K79me trans-crosstalk and highlight the diversity of mechanisms for histone ubiquitination to activate chromatin-modifying enzymes. | ||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7xd0.cif.gz 7xd0.cif.gz | 346 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7xd0.ent.gz pdb7xd0.ent.gz | 266.5 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7xd0.json.gz 7xd0.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/xd/7xd0 https://data.pdbj.org/pub/pdb/validation_reports/xd/7xd0 ftp://data.pdbj.org/pub/pdb/validation_reports/xd/7xd0 ftp://data.pdbj.org/pub/pdb/validation_reports/xd/7xd0 | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-タンパク質 , 5種, 10分子 FBGCHDEALK
| #1: タンパク質 |  ヒストンH4 ヒストンH4分子量: 9409.056 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 発現宿主: Homo sapiens (ヒト) / 発現宿主:   Escherichia coli BL21(DE3) (大腸菌) / 参照: UniProt: A0A672PXK1 Escherichia coli BL21(DE3) (大腸菌) / 参照: UniProt: A0A672PXK1#2: タンパク質 |  ヒストンH2A ヒストンH2A分子量: 11865.871 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: HIST1H2AB, HIST1H2AE, hCG_1640984, hCG_1787383 / 発現宿主: Homo sapiens (ヒト) / 遺伝子: HIST1H2AB, HIST1H2AE, hCG_1640984, hCG_1787383 / 発現宿主:   Escherichia coli BL21(DE3) (大腸菌) / 参照: UniProt: Q08AJ9 Escherichia coli BL21(DE3) (大腸菌) / 参照: UniProt: Q08AJ9#3: タンパク質 | 分子量: 10233.723 Da / 分子数: 2 / 由来タイプ: 合成 / 由来: (合成) synthetic construct (人工物) / 参照: UniProt: Q2M2T1 #4: タンパク質 | 分子量: 11631.616 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 発現宿主: Homo sapiens (ヒト) / 発現宿主:   Escherichia coli BL21(DE3) (大腸菌) / 参照: UniProt: S4RAZ3 Escherichia coli BL21(DE3) (大腸菌) / 参照: UniProt: S4RAZ3#7: タンパク質 | 分子量: 8576.831 Da / 分子数: 2 / 由来タイプ: 合成 / 由来: (合成) synthetic construct (人工物) / 参照: UniProt: A0A2H6N1E9 |
|---|
-DNA鎖 , 2種, 2分子 IJ
| #5: DNA鎖 | 分子量: 44825.559 Da / 分子数: 1 / 由来タイプ: 合成 / 由来: (合成) synthetic construct (人工物) |
|---|---|
| #6: DNA鎖 | 分子量: 45305.852 Da / 分子数: 1 / 由来タイプ: 合成 / 由来: (合成) synthetic construct (人工物) |
-実験情報
-実験
| 実験 | 手法:  電子顕微鏡法 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法:  単粒子再構成法 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: H2BK34ub nucleosome / タイプ: COMPLEX / Entity ID: all / 由来: RECOMBINANT |
|---|---|
| 由来(天然) | 生物種:   Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 由来(組換発現) | 生物種:   Escherichia coli BL21(DE3) (大腸菌) Escherichia coli BL21(DE3) (大腸菌) |
| 緩衝液 | pH: 7.5 |
| 試料 | 包埋: NO / シャドウイング: NO / 染色 : NO / 凍結 : NO / 凍結 : YES : YES |
急速凍結 | 凍結剤: ETHANE |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源 : :  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: OTHER FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: OTHER |
| 電子レンズ | モード: BRIGHT FIELD Bright-field microscopy / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 1000 nm Bright-field microscopy / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 1000 nm |
| 撮影 | 電子線照射量: 50 e/Å2 / フィルム・検出器のモデル: GATAN K3 (6k x 4k) |
- 解析
解析
CTF補正 | タイプ: PHASE FLIPPING ONLY |
|---|---|
3次元再構成 | 解像度: 3.48 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 85558 / 対称性のタイプ: POINT |
 ムービー
ムービー コントローラー
コントローラー









 PDBj
PDBj








































