+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1twr | ||||||
|---|---|---|---|---|---|---|---|
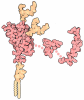
| タイトル | Crystal structures of ferrous and ferrous-NO forms of verdoheme in a complex with human heme oxygenase-1: catalytic implications for heme cleavage | ||||||
 要素 要素 | Heme oxygenase 1 HMOX1 HMOX1 | ||||||
 キーワード キーワード |  OXIDOREDUCTASE (酸化還元酵素) / OXIDOREDUCTASE (酸化還元酵素) /  heme oxygenase-1 (ヘム酸素添加酵素) / heme degredation heme oxygenase-1 (ヘム酸素添加酵素) / heme degredation | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報Regulation of HMOX1 expression and activity / heme oxygenase (biliverdin-producing) / low-density lipoprotein particle clearance / cellular response to cisplatin / heme oxidation / smooth muscle hyperplasia / negative regulation of leukocyte migration /  heme oxygenase (decyclizing) activity / wound healing involved in inflammatory response / positive regulation of blood vessel endothelial cell proliferation involved in sprouting angiogenesis ...Regulation of HMOX1 expression and activity / heme oxygenase (biliverdin-producing) / low-density lipoprotein particle clearance / cellular response to cisplatin / heme oxidation / smooth muscle hyperplasia / negative regulation of leukocyte migration / heme oxygenase (decyclizing) activity / wound healing involved in inflammatory response / positive regulation of blood vessel endothelial cell proliferation involved in sprouting angiogenesis ...Regulation of HMOX1 expression and activity / heme oxygenase (biliverdin-producing) / low-density lipoprotein particle clearance / cellular response to cisplatin / heme oxidation / smooth muscle hyperplasia / negative regulation of leukocyte migration /  heme oxygenase (decyclizing) activity / wound healing involved in inflammatory response / positive regulation of blood vessel endothelial cell proliferation involved in sprouting angiogenesis / heme catabolic process / cellular response to arsenic-containing substance / endothelial cell proliferation / erythrocyte homeostasis / positive regulation of epithelial cell apoptotic process / Heme degradation / epithelial cell apoptotic process / NFE2L2 regulating anti-oxidant/detoxification enzymes / negative regulation of macroautophagy / Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / positive regulation of cell migration involved in sprouting angiogenesis / positive regulation of macroautophagy / The NLRP3 inflammasome / heme oxygenase (decyclizing) activity / wound healing involved in inflammatory response / positive regulation of blood vessel endothelial cell proliferation involved in sprouting angiogenesis / heme catabolic process / cellular response to arsenic-containing substance / endothelial cell proliferation / erythrocyte homeostasis / positive regulation of epithelial cell apoptotic process / Heme degradation / epithelial cell apoptotic process / NFE2L2 regulating anti-oxidant/detoxification enzymes / negative regulation of macroautophagy / Insertion of tail-anchored proteins into the endoplasmic reticulum membrane / positive regulation of cell migration involved in sprouting angiogenesis / positive regulation of macroautophagy / The NLRP3 inflammasome /  regulation of angiogenesis / regulation of angiogenesis /  Purinergic signaling in leishmaniasis infection / negative regulation of extrinsic apoptotic signaling pathway via death domain receptors / positive regulation of chemokine production / cellular response to cadmium ion / response to nicotine / negative regulation of smooth muscle cell proliferation / Purinergic signaling in leishmaniasis infection / negative regulation of extrinsic apoptotic signaling pathway via death domain receptors / positive regulation of chemokine production / cellular response to cadmium ion / response to nicotine / negative regulation of smooth muscle cell proliferation /  オートファジー / Iron uptake and transport / positive regulation of smooth muscle cell proliferation / Heme signaling / response to hydrogen peroxide / Cytoprotection by HMOX1 / multicellular organismal-level iron ion homeostasis / positive regulation of angiogenesis / cellular response to heat / cellular response to hypoxia / オートファジー / Iron uptake and transport / positive regulation of smooth muscle cell proliferation / Heme signaling / response to hydrogen peroxide / Cytoprotection by HMOX1 / multicellular organismal-level iron ion homeostasis / positive regulation of angiogenesis / cellular response to heat / cellular response to hypoxia /  血管新生 / Interleukin-4 and Interleukin-13 signaling / positive regulation of canonical NF-kappaB signal transduction / response to oxidative stress / intracellular iron ion homeostasis / mitochondrial outer membrane / intracellular signal transduction / 血管新生 / Interleukin-4 and Interleukin-13 signaling / positive regulation of canonical NF-kappaB signal transduction / response to oxidative stress / intracellular iron ion homeostasis / mitochondrial outer membrane / intracellular signal transduction /  heme binding / endoplasmic reticulum membrane / regulation of transcription by RNA polymerase II / perinuclear region of cytoplasm / structural molecule activity / heme binding / endoplasmic reticulum membrane / regulation of transcription by RNA polymerase II / perinuclear region of cytoplasm / structural molecule activity /  enzyme binding / enzyme binding /  小胞体 / protein homodimerization activity / 小胞体 / protein homodimerization activity /  extracellular space / extracellular space /  核質 / 核質 /  生体膜 / identical protein binding / 生体膜 / identical protein binding /  metal ion binding / metal ion binding /  細胞核 / 細胞核 /  細胞質基質 細胞質基質類似検索 - 分子機能 | ||||||
| 生物種 |   Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.1 Å 分子置換 / 解像度: 2.1 Å | ||||||
 データ登録者 データ登録者 | Lad, L. / Ortiz de Montellano, P.R. / Poulos, T.L. | ||||||
 引用 引用 |  ジャーナル: J.Inorg.Biochem. / 年: 2004 ジャーナル: J.Inorg.Biochem. / 年: 2004タイトル: Crystal structures of ferrous and ferrous-NO forms of verdoheme in a complex with human heme oxygenase-1: catalytic implications for heme cleavage. 著者: Lad, L. / Ortiz de Montellano, P.R. / Poulos, T.L. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1twr.cif.gz 1twr.cif.gz | 104.3 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1twr.ent.gz pdb1twr.ent.gz | 79.8 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1twr.json.gz 1twr.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/tw/1twr https://data.pdbj.org/pub/pdb/validation_reports/tw/1twr ftp://data.pdbj.org/pub/pdb/validation_reports/tw/1twr ftp://data.pdbj.org/pub/pdb/validation_reports/tw/1twr | HTTPS FTP |
|---|
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 |
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 |  HMOX1 / HO-1 HMOX1 / HO-1分子量: 26898.615 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)   Homo sapiens (ヒト) / 遺伝子: HMOX1, HO1, HO / プラスミド: pCWORI / 発現宿主: Homo sapiens (ヒト) / 遺伝子: HMOX1, HO1, HO / プラスミド: pCWORI / 発現宿主:   Escherichia coli (大腸菌) / 株 (発現宿主): dh5alpha Escherichia coli (大腸菌) / 株 (発現宿主): dh5alpha参照: UniProt: P09601, heme oxygenase (biliverdin-producing) #2: 化合物 | #3: 化合物 |  一酸化窒素 一酸化窒素#4: 水 | ChemComp-HOH / |  水 水 |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 2 Å3/Da / 溶媒含有率: 23 % |
|---|---|
結晶化 | 温度: 301 K / 手法: liquid diffusion / pH: 8 詳細: NH4SO4, Hepes, NaCl, pH 8.0, LIQUID DIFFUSION, temperature 301K |
-データ収集
| 回折 | 平均測定温度: 119 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  ALS ALS  / ビームライン: 5.0.2 / ビームライン: 5.0.2 |
| 検出器 | タイプ: ADSC QUANTUM 4 / 検出器: CCD |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 相対比: 1 |
| 反射 | 解像度: 2.1→50 Å / Num. all: 64321 / Num. obs: 59654 / % possible obs: 93.1 % / Observed criterion σ(F): 2 / Observed criterion σ(I): 2 / 冗長度: 8.1 % / Rmerge(I) obs: 0.097 / Rsym value: 0.025 / Net I/σ(I): 10.3 |
| 反射 シェル | 解像度: 2.1→2.18 Å / 冗長度: 5.1 % / Rmerge(I) obs: 0.082 / Mean I/σ(I) obs: 2 / Num. unique all: 5476 / Rsym value: 0.25 / % possible all: 94.3 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法 : :  分子置換 分子置換開始モデル: pdb entry 1qq8  1qq8 最高解像度: 2.1 Å / Isotropic thermal model: isotropic / 交差検証法: THROUGHOUT / σ(I): 2 / 立体化学のターゲット値: Engh & Huber
| ||||||||||||||||
| 精密化ステップ | サイクル: LAST / 最高解像度: 2.1 Å
| ||||||||||||||||
| 拘束条件 |
| ||||||||||||||||
| LS精密化 シェル | 解像度: 2.1→2.18 Å
|
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj