+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8pkz | ||||||
|---|---|---|---|---|---|---|---|
| タイトル | NMR solution structure of PilF-GSPIIB in the c-di-GMP bound state | ||||||
 要素 要素 | ATP-binding motif-containing protein pilF | ||||||
 キーワード キーワード | MOTOR PROTEIN / PilT class / NMR-structure / ligand binding / GSPII | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報 | ||||||
| 生物種 |   Thermus thermophilus HB27 (バクテリア) Thermus thermophilus HB27 (バクテリア) | ||||||
| 手法 | 溶液NMR / distance geometry / simulated annealing / torsion angle dynamics | ||||||
 データ登録者 データ登録者 | Neissner, K. / Woehnert, J. | ||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| ||||||
 引用 引用 |  ジャーナル: To Be Published ジャーナル: To Be Publishedタイトル: NMR solution structure of GSPIIB of Thermus thermophilus in the c-di-GMP bound state 著者: Neissner, K. / Woehnert, J. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8pkz.cif.gz 8pkz.cif.gz | 1.1 MB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8pkz.ent.gz pdb8pkz.ent.gz | 910.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8pkz.json.gz 8pkz.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  8pkz_validation.pdf.gz 8pkz_validation.pdf.gz | 679.4 KB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  8pkz_full_validation.pdf.gz 8pkz_full_validation.pdf.gz | 868.2 KB | 表示 | |
| XML形式データ |  8pkz_validation.xml.gz 8pkz_validation.xml.gz | 75.9 KB | 表示 | |
| CIF形式データ |  8pkz_validation.cif.gz 8pkz_validation.cif.gz | 83.8 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/pk/8pkz https://data.pdbj.org/pub/pdb/validation_reports/pk/8pkz ftp://data.pdbj.org/pub/pdb/validation_reports/pk/8pkz ftp://data.pdbj.org/pub/pdb/validation_reports/pk/8pkz | HTTPS FTP |
-関連構造データ
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
|---|---|
| その他のデータベース |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 1 |
| |||||||||
| NMR アンサンブル |
|
- 要素
要素
| #1: タンパク質 | 分子量: 16269.562 Da / 分子数: 1 / 由来タイプ: 組換発現 詳細: Each molecule consists of the protein bound to c-di-GMP (residues 147-148). 由来: (組換発現)   Thermus thermophilus HB27 (バクテリア) Thermus thermophilus HB27 (バクテリア)遺伝子: pilF, TT_C1622 / 発現宿主:  | ||
|---|---|---|---|
| #2: 化合物 | | 研究の焦点であるリガンドがあるか | Y | |
-実験情報
-実験
| 実験 | 手法: 溶液NMR | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| NMR実験 |
|
- 試料調製
試料調製
| 詳細 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 試料 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 試料状態 | イオン強度: 200 mM NaCl mM / Label: conditions_1 / pH: 5.8 / 圧: ambient atm / 温度: 318 K |
-NMR測定
| NMRスペクトロメーター |
|
|---|
- 解析
解析
| NMR software |
| |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 |
| |||||||||||||||||||||
| 代表構造 | 選択基準: target function | |||||||||||||||||||||
| NMRアンサンブル | コンフォーマー選択の基準: target function / 計算したコンフォーマーの数: 100 / 登録したコンフォーマーの数: 20 |
 ムービー
ムービー コントローラー
コントローラー



 PDBj
PDBj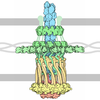



 HSQC
HSQC