[English] 日本語
 Yorodumi
Yorodumi- PDB-8de2: TEM-1 beta-lactamase A237Y mutant covalently bound to avibactam, ... -
+ Open data
Open data
- Basic information
Basic information
| Entry | Database: PDB / ID: 8de2 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
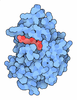
| Title | TEM-1 beta-lactamase A237Y mutant covalently bound to avibactam, a room temperature structure | |||||||||
 Components Components | Beta-lactamase TEM | |||||||||
 Keywords Keywords | HYDROLASE/INHIBITOR / Hydrolase / Beta-lactamase / TEM / avibactam / room-temperature / HYDROLASE-INHIBITOR complex | |||||||||
| Function / homology |  Function and homology information Function and homology informationbeta-lactam antibiotic catabolic process / beta-lactamase activity / beta-lactamase / response to antibiotic Similarity search - Function | |||||||||
| Biological species |  | |||||||||
| Method |  X-RAY DIFFRACTION / X-RAY DIFFRACTION /  SYNCHROTRON / SYNCHROTRON /  MOLECULAR REPLACEMENT / Resolution: 2.45 Å MOLECULAR REPLACEMENT / Resolution: 2.45 Å | |||||||||
 Authors Authors | Ji, Z. / Boxer, S.G. / Mathews, I.I. | |||||||||
| Funding support |  United States, 2items United States, 2items
| |||||||||
 Citation Citation |  Journal: J.Am.Chem.Soc. / Year: 2022 Journal: J.Am.Chem.Soc. / Year: 2022Title: Protein Electric Fields Enable Faster and Longer-Lasting Covalent Inhibition of beta-Lactamases. Authors: Ji, Z. / Kozuch, J. / Mathews, I.I. / Diercks, C.S. / Shamsudin, Y. / Schulz, M.A. / Boxer, S.G. | |||||||||
| History |
|
- Structure visualization
Structure visualization
| Structure viewer | Molecule:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- Downloads & links
Downloads & links
- Download
Download
| PDBx/mmCIF format |  8de2.cif.gz 8de2.cif.gz | 212.1 KB | Display |  PDBx/mmCIF format PDBx/mmCIF format |
|---|---|---|---|---|
| PDB format |  pdb8de2.ent.gz pdb8de2.ent.gz | 169.1 KB | Display |  PDB format PDB format |
| PDBx/mmJSON format |  8de2.json.gz 8de2.json.gz | Tree view |  PDBx/mmJSON format PDBx/mmJSON format | |
| Others |  Other downloads Other downloads |
-Validation report
| Summary document |  8de2_validation.pdf.gz 8de2_validation.pdf.gz | 1.6 MB | Display |  wwPDB validaton report wwPDB validaton report |
|---|---|---|---|---|
| Full document |  8de2_full_validation.pdf.gz 8de2_full_validation.pdf.gz | 1.6 MB | Display | |
| Data in XML |  8de2_validation.xml.gz 8de2_validation.xml.gz | 40.2 KB | Display | |
| Data in CIF |  8de2_validation.cif.gz 8de2_validation.cif.gz | 53.6 KB | Display | |
| Arichive directory |  https://data.pdbj.org/pub/pdb/validation_reports/de/8de2 https://data.pdbj.org/pub/pdb/validation_reports/de/8de2 ftp://data.pdbj.org/pub/pdb/validation_reports/de/8de2 ftp://data.pdbj.org/pub/pdb/validation_reports/de/8de2 | HTTPS FTP |
-Related structure data
| Related structure data |  7u6qC  8ddzC  8de0C  8de1C  1ermS S: Starting model for refinement C: citing same article ( |
|---|---|
| Similar structure data | Similarity search - Function & homology  F&H Search F&H Search |
- Links
Links
- Assembly
Assembly
| Deposited unit | 
| |||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| |||||||||||||||||||||||||||||||||||
| 2 | 
| |||||||||||||||||||||||||||||||||||
| 3 | 
| |||||||||||||||||||||||||||||||||||
| 4 | 
| |||||||||||||||||||||||||||||||||||
| Unit cell |
| |||||||||||||||||||||||||||||||||||
| Noncrystallographic symmetry (NCS) | NCS domain:
NCS domain segments: Component-ID: 1 / Ens-ID: 1 / Beg auth comp-ID: HIS / Beg label comp-ID: HIS / End auth comp-ID: TRP / End label comp-ID: TRP / Auth seq-ID: 26 - 288 / Label seq-ID: 2 - 264
|
- Components
Components
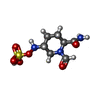
| #1: Protein | Mass: 29061.053 Da / Num. of mol.: 4 / Mutation: M182T, A237Y Source method: isolated from a genetically manipulated source Details: An extra glycine at the N-terminus / Source: (gene. exp.)   #2: Chemical | ChemComp-NXL / ( #3: Water | ChemComp-HOH / | Has ligand of interest | Y | Has protein modification | Y | |
|---|
-Experimental details
-Experiment
| Experiment | Method:  X-RAY DIFFRACTION / Number of used crystals: 1 X-RAY DIFFRACTION / Number of used crystals: 1 |
|---|
- Sample preparation
Sample preparation
| Crystal | Density Matthews: 2.19 Å3/Da / Density % sol: 43.75 % |
|---|---|
| Crystal grow | Temperature: 296 K / Method: vapor diffusion, hanging drop / pH: 7 Details: PEG3350, HEPES(4-(2-hydroxyethyl)-1-piperazineethanesulfonic acid) |
-Data collection
| Diffraction | Mean temperature: 297 K / Serial crystal experiment: N | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Diffraction source | Source:  SYNCHROTRON / Site: SYNCHROTRON / Site:  SSRL SSRL  / Beamline: BL12-1 / Wavelength: 0.97946 Å / Beamline: BL12-1 / Wavelength: 0.97946 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Detector | Type: DECTRIS PILATUS 6M / Detector: PIXEL / Date: May 13, 2022 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation | Protocol: SINGLE WAVELENGTH / Monochromatic (M) / Laue (L): M / Scattering type: x-ray | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radiation wavelength | Wavelength: 0.97946 Å / Relative weight: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection twin | Operator: -h,-k,l / Fraction: 0.52 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection | Resolution: 2.45→39.33 Å / Num. obs: 35092 / % possible obs: 94.9 % / Redundancy: 6.025 % / CC1/2: 0.998 / Rmerge(I) obs: 0.152 / Rrim(I) all: 0.167 / Χ2: 0.816 / Net I/σ(I): 8.54 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Reflection shell | Diffraction-ID: 1
|
- Processing
Processing
| Software |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Refinement | Method to determine structure:  MOLECULAR REPLACEMENT MOLECULAR REPLACEMENTStarting model: 1ERM Resolution: 2.45→39.33 Å / Cross valid method: THROUGHOUT / σ(F): 1.95 / Phase error: 38.09 / Stereochemistry target values: TWIN_LSQ_F
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solvent computation | Shrinkage radii: 0.9 Å / VDW probe radii: 1.11 Å / Solvent model: FLAT BULK SOLVENT MODEL | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Displacement parameters | Biso max: 141.07 Å2 / Biso mean: 43.5318 Å2 / Biso min: 24.83 Å2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refinement step | Cycle: final / Resolution: 2.45→39.33 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Refine LS restraints NCS |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LS refinement shell | Refine-ID: X-RAY DIFFRACTION / Rfactor Rfree error: 0 / Total num. of bins used: 13
|
 Movie
Movie Controller
Controller


 PDBj
PDBj