| 登録情報 | データベース: PDB / ID: 7rjq
|
|---|
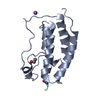
| タイトル | Crystal structure of human Bromodomain containing protein 4 (BRD4) in complex with ILF3 |
|---|
 要素 要素 | - Bromodomain-containing protein 4
- Interleukin enhancer-binding factor 3
|
|---|
 キーワード キーワード | SIGNALING PROTEIN / Brd4 / ILF3 / acetyllysine |
|---|
| 機能・相同性 |  機能・相同性情報 機能・相同性情報
spliceosome-depend formation of circular RNA / Regulation of CDH11 gene transcription / mRNA 3'-UTR AU-rich region binding / negative regulation of viral genome replication / RNA polymerase II C-terminal domain binding / P-TEFb complex binding / negative regulation of DNA damage checkpoint / histone H4 reader activity / host-mediated suppression of viral transcription / positive regulation of G2/M transition of mitotic cell cycle ...spliceosome-depend formation of circular RNA / Regulation of CDH11 gene transcription / mRNA 3'-UTR AU-rich region binding / negative regulation of viral genome replication / RNA polymerase II C-terminal domain binding / P-TEFb complex binding / negative regulation of DNA damage checkpoint / histone H4 reader activity / host-mediated suppression of viral transcription / positive regulation of G2/M transition of mitotic cell cycle / positive regulation of T-helper 17 cell lineage commitment / : / RNA polymerase II CTD heptapeptide repeat kinase activity / condensed nuclear chromosome / transcription coregulator activity / positive regulation of transcription elongation by RNA polymerase II / PKR-mediated signaling / p53 binding / double-stranded RNA binding / chromosome / virus receptor activity / regulation of inflammatory response / histone binding / defense response to virus / Potential therapeutics for SARS / transcription coactivator activity / single-stranded RNA binding / protein phosphorylation / positive regulation of canonical NF-kappaB signal transduction / transcription cis-regulatory region binding / negative regulation of translation / chromatin remodeling / ribonucleoprotein complex / negative regulation of DNA-templated transcription / protein serine/threonine kinase activity / DNA damage response / chromatin binding / regulation of transcription by RNA polymerase II / chromatin / positive regulation of DNA-templated transcription / nucleolus / enzyme binding / positive regulation of transcription by RNA polymerase II / mitochondrion / DNA binding / RNA binding / extracellular region / nucleoplasm / nucleus / membrane / cytosol / cytoplasm類似検索 - 分子機能 Interleukin enhancer-binding factor 3 / DZF domain / : / : / DZF N-terminal domain / DZF C-terminal domain / DZF domain profile. / domain in DSRM or ZnF_C2H2 domain containing proteins / Double-stranded RNA binding motif / Double-stranded RNA binding motif ...Interleukin enhancer-binding factor 3 / DZF domain / : / : / DZF N-terminal domain / DZF C-terminal domain / DZF domain profile. / domain in DSRM or ZnF_C2H2 domain containing proteins / Double-stranded RNA binding motif / Double-stranded RNA binding motif / Double stranded RNA-binding domain (dsRBD) profile. / Double-stranded RNA-binding domain / Bromodomain protein 4, C-terminal / C-terminal domain of bromodomain protein 4 / Brdt, bromodomain, repeat I / Brdt, bromodomain, repeat II / NET domain superfamily / NET domain profile. / : / NET domain / Bromodomain extra-terminal - transcription regulation / Nucleotidyltransferase superfamily / Bromodomain, conserved site / Bromodomain signature. / Bromodomain / bromo domain / Bromodomain / Bromodomain (BrD) profile. / Bromodomain-like superfamily類似検索 - ドメイン・相同性 Bromodomain-containing protein 4 / Interleukin enhancer-binding factor 3類似検索 - 構成要素 |
|---|
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) |
|---|
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 1.72 Å 分子置換 / 解像度: 1.72 Å |
|---|
 データ登録者 データ登録者 | Fedorov, E. / Islam, K. / Ghosh, A. |
|---|
| 資金援助 |  米国, 3件 米国, 3件 | 組織 | 認可番号 | 国 |
|---|
| National Institutes of Health/National Institute of General Medical Sciences (NIH/NIGMS) | R01GM123234 |  米国 米国 | | National Institutes of Health/National Institute of General Medical Sciences (NIH/NIGMS) | R01GM130752 |  米国 米国 | | National Institutes of Health/National Institute of General Medical Sciences (NIH/NIGMS) | P01GM118303 |  米国 米国 |
|
|---|
 引用 引用 |  ジャーナル: To Be Published ジャーナル: To Be Published
タイトル: Uncovering the Bromodomain Interactome using Site-Specific Azide-Acetyllysine Photochemistry, Proteomic Profiling and Structural Characterization
著者: Wagner, S. / Fedorov, E. / Sudhamalla, B. / Jnawali, H.N. / Debiec, R. / Ghosh, A. / Islam, K. |
|---|
| 履歴 | | 登録 | 2021年7月21日 | 登録サイト: RCSB / 処理サイト: RCSB |
|---|
| 改定 1.0 | 2022年8月3日 | Provider: repository / タイプ: Initial release |
|---|
| 改定 1.1 | 2023年10月18日 | Group: Data collection / Refinement description
カテゴリ: chem_comp_atom / chem_comp_bond / pdbx_initial_refinement_model |
|---|
| 改定 1.2 | 2023年11月15日 | Group: Data collection / カテゴリ: chem_comp_atom / chem_comp_bond / Item: _chem_comp_atom.atom_id / _chem_comp_bond.atom_id_2 |
|---|
| 改定 1.3 | 2024年11月20日 | Group: Structure summary
カテゴリ: pdbx_entry_details / pdbx_modification_feature
Item: _pdbx_entry_details.has_protein_modification |
|---|
|
|---|
 データを開く
データを開く 基本情報
基本情報 要素
要素 キーワード
キーワード 機能・相同性情報
機能・相同性情報 Homo sapiens (ヒト)
Homo sapiens (ヒト) X線回折 /
X線回折 /  シンクロトロン /
シンクロトロン /  分子置換 / 解像度: 1.72 Å
分子置換 / 解像度: 1.72 Å  データ登録者
データ登録者 米国, 3件
米国, 3件  引用
引用 ジャーナル: To Be Published
ジャーナル: To Be Published 構造の表示
構造の表示 Molmil
Molmil Jmol/JSmol
Jmol/JSmol ダウンロードとリンク
ダウンロードとリンク ダウンロード
ダウンロード 7rjq.cif.gz
7rjq.cif.gz PDBx/mmCIF形式
PDBx/mmCIF形式 pdb7rjq.ent.gz
pdb7rjq.ent.gz PDB形式
PDB形式 7rjq.json.gz
7rjq.json.gz PDBx/mmJSON形式
PDBx/mmJSON形式 その他のダウンロード
その他のダウンロード 7rjq_validation.pdf.gz
7rjq_validation.pdf.gz wwPDB検証レポート
wwPDB検証レポート 7rjq_full_validation.pdf.gz
7rjq_full_validation.pdf.gz 7rjq_validation.xml.gz
7rjq_validation.xml.gz 7rjq_validation.cif.gz
7rjq_validation.cif.gz https://data.pdbj.org/pub/pdb/validation_reports/rj/7rjq
https://data.pdbj.org/pub/pdb/validation_reports/rj/7rjq ftp://data.pdbj.org/pub/pdb/validation_reports/rj/7rjq
ftp://data.pdbj.org/pub/pdb/validation_reports/rj/7rjq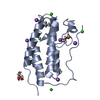

 F&H 検索
F&H 検索 リンク
リンク 集合体
集合体
 要素
要素 Homo sapiens (ヒト) / 遺伝子: BRD4, HUNK1 / 発現宿主:
Homo sapiens (ヒト) / 遺伝子: BRD4, HUNK1 / 発現宿主: 
 Homo sapiens (ヒト) / 参照: UniProt: Q12906
Homo sapiens (ヒト) / 参照: UniProt: Q12906






 X線回折 / 使用した結晶の数: 1
X線回折 / 使用した結晶の数: 1  試料調製
試料調製 シンクロトロン / サイト:
シンクロトロン / サイト:  APS
APS  / ビームライン: 31-ID / 波長: 0.98 Å
/ ビームライン: 31-ID / 波長: 0.98 Å 分子置換
分子置換 解析
解析 分子置換
分子置換 ムービー
ムービー コントローラー
コントローラー



 PDBj
PDBj



