+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 2scu | ||||||
|---|---|---|---|---|---|---|---|
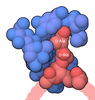
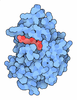
| タイトル | A detailed description of the structure of Succinyl-COA synthetase from Escherichia coli | ||||||
 要素 要素 | (PROTEIN (SUCCINYL-COA LIGASE)) x 2 | ||||||
 キーワード キーワード | LIGASE / CITRIC ACID CYCLE / HETEROTETRAMER | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報succinate-CoA ligase (GDP-forming) activity / succinate-CoA ligase complex (ADP-forming) / succinate-CoA ligase (ADP-forming) / succinate-CoA ligase complex / succinate-CoA ligase (ADP-forming) activity / succinyl-CoA metabolic process / tricarboxylic acid cycle / nucleotide binding / magnesium ion binding / ATP binding ...succinate-CoA ligase (GDP-forming) activity / succinate-CoA ligase complex (ADP-forming) / succinate-CoA ligase (ADP-forming) / succinate-CoA ligase complex / succinate-CoA ligase (ADP-forming) activity / succinyl-CoA metabolic process / tricarboxylic acid cycle / nucleotide binding / magnesium ion binding / ATP binding / cytoplasm / cytosol 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  多重同系置換 / 解像度: 2.3 Å 多重同系置換 / 解像度: 2.3 Å | ||||||
 データ登録者 データ登録者 | Fraser, M.E. / Wolodko, W.T. / James, M.N.G. / Bridger, W.A. | ||||||
 引用 引用 |  ジャーナル: J.Mol.Biol. / 年: 1999 ジャーナル: J.Mol.Biol. / 年: 1999タイトル: A detailed structural description of Escherichia coli succinyl-CoA synthetase. 著者: Fraser, M.E. / James, M.N. / Bridger, W.A. / Wolodko, W.T. #1:  ジャーナル: J.Biol.Chem. / 年: 1994 ジャーナル: J.Biol.Chem. / 年: 1994タイトル: The Crystal Structure of Succinyl-Coa Synthetase from Escherichia Coli at 2.5 Angstroms Resolution 著者: Wolodko, W.T. / Fraser, M.E. / James, M.N.G. / Bridger, W.A. #2:  ジャーナル: J.Biol.Chem. / 年: 1984 ジャーナル: J.Biol.Chem. / 年: 1984タイトル: Crystallization of Succinyl-Coa Synthetase from Escherichia Coli 著者: Wolodko, W.T. / James, M.N.G. / Bridger, W.A. #3:  ジャーナル: J.Mol.Biol. / 年: 1999 ジャーナル: J.Mol.Biol. / 年: 1999タイトル: A Dimeric Form of Escherichia Coli Succinyl-Coa Synthetase Produced by Site- Directed Mutagenesis 著者: Bailey, D.L. / Fraser, M.E. / Bridger, W.A. / James, M.N.G. / Wolodko, W.T. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  2scu.cif.gz 2scu.cif.gz | 269.2 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb2scu.ent.gz pdb2scu.ent.gz | 216.3 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  2scu.json.gz 2scu.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/sc/2scu https://data.pdbj.org/pub/pdb/validation_reports/sc/2scu ftp://data.pdbj.org/pub/pdb/validation_reports/sc/2scu ftp://data.pdbj.org/pub/pdb/validation_reports/sc/2scu | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ | |
|---|---|
| 類似構造データ |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||||||||||||||
| 2 | 
| ||||||||||||||||||||
| 単位格子 |
| ||||||||||||||||||||
| Components on special symmetry positions |
| ||||||||||||||||||||
| 非結晶学的対称性 (NCS) | NCS oper:
|
- 要素
要素
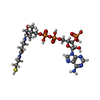
| #1: タンパク質 | 分子量: 29758.213 Da / 分子数: 2 / 由来タイプ: 組換発現 / 詳細: RESIDUES A246 AND D246 ARE PHOSPHOHISTIDINES / 由来: (組換発現)   参照: UniProt: P07459, UniProt: P0AGE9*PLUS, succinate-CoA ligase (ADP-forming) #2: タンパク質 | 分子量: 41438.496 Da / 分子数: 2 / 由来タイプ: 組換発現 / 詳細: RESIDUES A246 AND D246 ARE PHOSPHOHISTIDINES / 由来: (組換発現)   参照: UniProt: P07460, UniProt: P0A836*PLUS, succinate-CoA ligase (ADP-forming) #3: 化合物 | #4: 化合物 | #5: 水 | ChemComp-HOH / | 非ポリマーの詳細 | SO4 400 IS ASSOCIATED | 配列の詳細 | AMINO-TERMINAL ANALYSIS OF THE ALPHA SUBUNIT INDICATES THAT THE FIRST RESIDUE IS A SERINE (W. A. ...AMINO-TERMINAL ANALYSIS OF THE ALPHA SUBUNIT INDICATES THAT THE FIRST RESIDUE IS A SERINE (W. A. BRIDGE, ENZYMES, 1974, 3RD ED. 10, 581-606). IN THE GENE SEQUENCING | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 23 X線回折 / 使用した結晶の数: 23 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 3.45 Å3/Da / 溶媒含有率: 64.35 % / 解説: DATA WERE COLLECTED USING THE WEISSENBERG METHOD. | |||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶化 | pH: 7.2 / 詳細: pH 7.2 | |||||||||||||||||||||||||||||||||||
| 結晶化 | *PLUS 温度: 21 ℃ / pH: 7.3 / 手法: microdialysis / 詳細: Wolodko, W.T., (1984) J. Biol. Chem., 259, 5316. | |||||||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 283 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  Photon Factory Photon Factory  / ビームライン: BL-6A / 波長: 1 / ビームライン: BL-6A / 波長: 1 |
| 検出器 | 検出器: IMAGE PLATE / 日付: 1995年3月1日 |
| 放射 | プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 1 Å / 相対比: 1 |
| 反射 | 解像度: 2.3→100 Å / Num. obs: 417950 / % possible obs: 92.7 % / Observed criterion σ(I): 0 / 冗長度: 5 % / Biso Wilson estimate: 32 Å2 / Rmerge(I) obs: 0.095 |
| 反射 シェル | 解像度: 2.3→2.5 Å / Rmerge(I) obs: 0.45 |
| 反射 | *PLUS Num. obs: 83411 / Num. measured all: 417950 |
- 解析
解析
| ソフトウェア |
| ||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  多重同系置換 / 解像度: 2.3→8 Å / σ(F): 0 多重同系置換 / 解像度: 2.3→8 Å / σ(F): 0
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.3→8 Å
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||
| ソフトウェア | *PLUS 名称: TNT / バージョン: 5EB / 分類: refinement | ||||||||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | *PLUS Rfactor all: 0.195 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS | ||||||||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 | *PLUS
|
 ムービー
ムービー コントローラー
コントローラー














 PDBj
PDBj