+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 1pk8 | ||||||
|---|---|---|---|---|---|---|---|
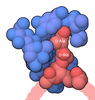
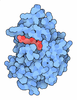
| タイトル | Crystal Structure of Rat Synapsin I C Domain Complexed to Ca.ATP | ||||||
 要素 要素 | rat synapsin I | ||||||
 キーワード キーワード | MEMBRANE PROTEIN / ATP binding / ATP grasp / calcium (II) ion | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報synaptic vesicle cycle / synaptic vesicle clustering / Serotonin Neurotransmitter Release Cycle / Dopamine Neurotransmitter Release Cycle / extrinsic component of synaptic vesicle membrane / synaptonemal complex / neurotransmitter secretion / regulation of synaptic vesicle cycle / presynaptic active zone / regulation of synaptic vesicle exocytosis ...synaptic vesicle cycle / synaptic vesicle clustering / Serotonin Neurotransmitter Release Cycle / Dopamine Neurotransmitter Release Cycle / extrinsic component of synaptic vesicle membrane / synaptonemal complex / neurotransmitter secretion / regulation of synaptic vesicle cycle / presynaptic active zone / regulation of synaptic vesicle exocytosis / neuron development / synapse organization / Schaffer collateral - CA1 synapse / terminal bouton / calcium-dependent protein binding / synaptic vesicle / synaptic vesicle membrane / presynapse / actin binding / cell body / cytoskeleton / postsynaptic density / axon / synapse / dendrite / protein kinase binding / Golgi apparatus / ATP binding / identical protein binding 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 |  X線回折 / X線回折 /  シンクロトロン / シンクロトロン /  分子置換 / 解像度: 2.1 Å 分子置換 / 解像度: 2.1 Å | ||||||
 データ登録者 データ登録者 | Brautigam, C.A. / Chelliah, Y. / Deisenhofer, J. | ||||||
 引用 引用 |  ジャーナル: J.Biol.Chem. / 年: 2004 ジャーナル: J.Biol.Chem. / 年: 2004タイトル: Tetramerization and ATP binding by a protein comprising the A, B, and C domains of rat synapsin I. 著者: Brautigam, C.A. / Chelliah, Y. / Deisenhofer, J. #1:  ジャーナル: Embo J. / 年: 1998 ジャーナル: Embo J. / 年: 1998タイトル: Synapsin I is structurally similar to ATP-utilizing enzymes 著者: Esser, L. / Wang, C.R. / Hosaka, M. / Smagula, C.S. / Sudhof, T.C. / Deisenhofer, J. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  1pk8.cif.gz 1pk8.cif.gz | 501.1 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb1pk8.ent.gz pdb1pk8.ent.gz | 404.2 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  1pk8.json.gz 1pk8.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  1pk8_validation.pdf.gz 1pk8_validation.pdf.gz | 5 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  1pk8_full_validation.pdf.gz 1pk8_full_validation.pdf.gz | 5 MB | 表示 | |
| XML形式データ |  1pk8_validation.xml.gz 1pk8_validation.xml.gz | 90.6 KB | 表示 | |
| CIF形式データ |  1pk8_validation.cif.gz 1pk8_validation.cif.gz | 122.4 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/pk/1pk8 https://data.pdbj.org/pub/pdb/validation_reports/pk/1pk8 ftp://data.pdbj.org/pub/pdb/validation_reports/pk/1pk8 ftp://data.pdbj.org/pub/pdb/validation_reports/pk/1pk8 | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
| ||||||||
|---|---|---|---|---|---|---|---|---|---|
| 1 | 
| ||||||||
| 2 | 
| ||||||||
| 単位格子 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 45539.398 Da / 分子数: 8 / 断片: A, B & C domains / 由来タイプ: 組換発現 / 由来: (組換発現)   #2: 化合物 | ChemComp-CA / #3: 化合物 | ChemComp-ATP / #4: 化合物 | #5: 水 | ChemComp-HOH / | |
|---|
-実験情報
-実験
| 実験 | 手法:  X線回折 / 使用した結晶の数: 1 X線回折 / 使用した結晶の数: 1 |
|---|
- 試料調製
試料調製
| 結晶 | マシュー密度: 1.89 Å3/Da / 溶媒含有率: 34.82 % | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 結晶化 | 温度: 299 K / 手法: 蒸気拡散法, ハンギングドロップ法 / pH: 7.5 詳細: PEGMME 5000, Tris, NaCl, Ca.ATP, EDTA, DTT, pH 7.5, VAPOR DIFFUSION, HANGING DROP, temperature 299K | ||||||||||||||||||||||||||||||||||||||||||
| 結晶化 | *PLUS 手法: 蒸気拡散法, ハンギングドロップ法 | ||||||||||||||||||||||||||||||||||||||||||
| 溶液の組成 | *PLUS
|
-データ収集
| 回折 | 平均測定温度: 100 K |
|---|---|
| 放射光源 | 由来:  シンクロトロン / サイト: シンクロトロン / サイト:  APS APS  / ビームライン: 19-ID / 波長: 1.008 Å / ビームライン: 19-ID / 波長: 1.008 Å |
| 検出器 | タイプ: CUSTOM-MADE / 検出器: CCD / 日付: 2000年3月17日 |
| 放射 | モノクロメーター: Double crystal monochromator, Si-111 プロトコル: SINGLE WAVELENGTH / 単色(M)・ラウエ(L): M / 散乱光タイプ: x-ray |
| 放射波長 | 波長: 1.008 Å / 相対比: 1 |
| 反射 | 解像度: 2.1→40 Å / Num. obs: 150398 / % possible obs: 96.3 % / 冗長度: 3.7 % / Biso Wilson estimate: 19 Å2 / Rsym value: 0.058 / Net I/σ(I): 20.9 |
| 反射 シェル | 解像度: 2.1→2.18 Å / 冗長度: 3.6 % / Mean I/σ(I) obs: 2.8 / Num. unique all: 14381 / Rsym value: 0.373 / % possible all: 92 |
| 反射 | *PLUS 最低解像度: 20 Å / Num. obs: 144586 / Num. measured all: 522852 / Rmerge(I) obs: 0.058 |
| 反射 シェル | *PLUS % possible obs: 92 % / Rmerge(I) obs: 0.373 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 精密化 | 構造決定の手法:  分子置換 分子置換開始モデル: PDB ENTRY 1AUX, ATPgammaS and Ca2+ removed 解像度: 2.1→20 Å / Isotropic thermal model: restrained / 交差検証法: THROUGHOUT / σ(F): 0 / 立体化学のターゲット値: MODIFIED ENGH & HUBER 詳細: Although the A, B, and C domains of rat Synapsin I were included in crystallization, only the C domain was observed. Some side chain atoms were set to an occupancy of 0.00 because of disorder. ...詳細: Although the A, B, and C domains of rat Synapsin I were included in crystallization, only the C domain was observed. Some side chain atoms were set to an occupancy of 0.00 because of disorder. Two conformations of ATP were modeled and refined due to ample evidence in the electron density maps. The differing phosphate positions would probably necessitate a movement in the associated Ca2+ ions, but only one Ca2+ was modeled per pair of ATP conformations
| |||||||||||||||||||||||||
| 溶媒の処理 | 溶媒モデル: flat model / Bsol: 37.4817 Å2 / ksol: 0.341215 e/Å3 | |||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 34.2 Å2
| |||||||||||||||||||||||||
| Refine analyze |
| |||||||||||||||||||||||||
| 精密化ステップ | サイクル: LAST / 解像度: 2.1→20 Å
| |||||||||||||||||||||||||
| 拘束条件 |
| |||||||||||||||||||||||||
| LS精密化 シェル | 解像度: 2.1→2.23 Å / Rfactor Rfree error: 0.007
| |||||||||||||||||||||||||
| 精密化 | *PLUS % reflection Rfree: 10 % | |||||||||||||||||||||||||
| 溶媒の処理 | *PLUS | |||||||||||||||||||||||||
| 原子変位パラメータ | *PLUS | |||||||||||||||||||||||||
| 拘束条件 | *PLUS
|
 ムービー
ムービー コントローラー
コントローラー















 PDBj
PDBj