+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-4908 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the E. coli cytochrome bd-I oxidase at 2.68 A resolution | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Oxidoreductase Cytochrome bd oxidase bd oxidase Oxidase / MEMBRANE PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報quinol oxidase (electrogenic, proton-motive force generating) / oxidoreductase activity, acting on diphenols and related substances as donors / cytochrome complex / aerobic electron transport chain / outer membrane / oxidoreductase activity, acting on diphenols and related substances as donors, oxygen as acceptor / oxidative phosphorylation / cellular response to hypoxia / electron transfer activity / heme binding ...quinol oxidase (electrogenic, proton-motive force generating) / oxidoreductase activity, acting on diphenols and related substances as donors / cytochrome complex / aerobic electron transport chain / outer membrane / oxidoreductase activity, acting on diphenols and related substances as donors, oxygen as acceptor / oxidative phosphorylation / cellular response to hypoxia / electron transfer activity / heme binding / membrane / metal ion binding / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |   | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.68 Å | |||||||||
 データ登録者 データ登録者 | Safarian S / Hahn A | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Science / 年: 2019 ジャーナル: Science / 年: 2019タイトル: Active site rearrangement and structural divergence in prokaryotic respiratory oxidases. 著者: S Safarian / A Hahn / D J Mills / M Radloff / M L Eisinger / A Nikolaev / J Meier-Credo / F Melin / H Miyoshi / R B Gennis / J Sakamoto / J D Langer / P Hellwig / W Kühlbrandt / H Michel /     要旨: Cytochrome bd-type quinol oxidases catalyze the reduction of molecular oxygen to water in the respiratory chain of many human-pathogenic bacteria. They are structurally unrelated to mitochondrial ...Cytochrome bd-type quinol oxidases catalyze the reduction of molecular oxygen to water in the respiratory chain of many human-pathogenic bacteria. They are structurally unrelated to mitochondrial cytochrome c oxidases and are therefore a prime target for the development of antimicrobial drugs. We determined the structure of the cytochrome bd-I oxidase by single-particle cryo-electron microscopy to a resolution of 2.7 angstroms. Our structure contains a previously unknown accessory subunit CydH, the L-subfamily-specific Q-loop domain, a structural ubiquinone-8 cofactor, an active-site density interpreted as dioxygen, distinct water-filled proton channels, and an oxygen-conducting pathway. Comparison with another cytochrome bd oxidase reveals structural divergence in the family, including rearrangement of high-spin hemes and conformational adaption of a transmembrane helix to generate a distinct oxygen-binding site. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_4908.map.gz emd_4908.map.gz | 7.9 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-4908-v30.xml emd-4908-v30.xml emd-4908.xml emd-4908.xml | 20.5 KB 20.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
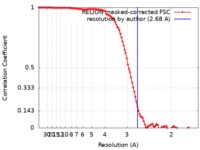
| FSC (解像度算出) |  emd_4908_fsc.xml emd_4908_fsc.xml | 10.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_4908.png emd_4908.png | 118.5 KB | ||
| Filedesc metadata |  emd-4908.cif.gz emd-4908.cif.gz | 7 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-4908 http://ftp.pdbj.org/pub/emdb/structures/EMD-4908 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4908 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-4908 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_4908.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_4908.map.gz / 形式: CCP4 / 大きさ: 103 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.832 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
+全体 : Cytochrome bd-I oxidase from E. coli
+超分子 #1: Cytochrome bd-I oxidase from E. coli
+分子 #1: Cytochrome bd-I ubiquinol oxidase subunit 2
+分子 #2: Cytochrome bd-I ubiquinol oxidase subunit 1
+分子 #3: Uncharacterized protein YnhF
+分子 #4: Cytochrome bd-I ubiquinol oxidase subunit X
+分子 #5: Ubiquinone-8
+分子 #6: (2S)-3-(hexadecanoyloxy)-2-[(9Z)-octadec-9-enoyloxy]propyl 2-(tri...
+分子 #7: CIS-HEME D HYDROXYCHLORIN GAMMA-SPIROLACTONE
+分子 #8: HEME B/C
+分子 #9: OXYGEN MOLECULE
+分子 #10: water
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 7 mg/mL | ||||||
|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
| ||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 200 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 45 sec. / 前処理 - 雰囲気: AIR | ||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 温度 | 最低: 70.0 K / 最高: 70.0 K |
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / 撮影したグリッド数: 1 / 実像数: 5463 / 平均露光時間: 2.0 sec. / 平均電子線量: 40.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 最大 デフォーカス(補正後): 2.5 µm / 最小 デフォーカス(補正後): 0.5 µm / 倍率(補正後): 96000 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 96000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL / 温度因子: 120 当てはまり具合の基準: Cross-correlation coefficient |
|---|---|
| 得られたモデル |  PDB-6rko: |
 ムービー
ムービー コントローラー
コントローラー














 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)