+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of doubly-bound SNF2h-nucleosome complex | |||||||||||||||
 マップデータ マップデータ | Double-bound SNF2h-nucleosome structure (cryoSPARC local refinement) | |||||||||||||||
 試料 試料 |
| |||||||||||||||
 キーワード キーワード | nucleosome / chromatin remodeler / ISWI / SNF2h / DNA BINDING PROTEIN-DNA complex | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報RSF complex / histone octamer slider activity / ACF complex / WICH complex / negative regulation of mitotic chromosome condensation / CERF complex / CHRAC / NoRC complex / NURF complex / nucleosome array spacer activity ...RSF complex / histone octamer slider activity / ACF complex / WICH complex / negative regulation of mitotic chromosome condensation / CERF complex / CHRAC / NoRC complex / NURF complex / nucleosome array spacer activity / B-WICH complex / rDNA heterochromatin formation / ATP-dependent chromatin remodeler activity / chromatin silencing complex / negative regulation of transcription by RNA polymerase I / positive regulation of transcription by RNA polymerase III / DNA methylation-dependent constitutive heterochromatin formation / positive regulation of transcription by RNA polymerase I / regulation of DNA replication / pericentric heterochromatin / nucleosome binding / condensed chromosome / antiviral innate immune response / Deposition of new CENPA-containing nucleosomes at the centromere / cellular response to leukemia inhibitory factor / positive regulation of DNA replication / DNA-templated transcription initiation / helicase activity / NoRC negatively regulates rRNA expression / B-WICH complex positively regulates rRNA expression / 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 / fibrillar center / structural constituent of chromatin / nucleosome / heterochromatin formation / nucleosome assembly / Recruitment and ATM-mediated phosphorylation of repair and signaling proteins at DNA double strand breaks / site of double-strand break / chromatin organization / chromatin remodeling / protein heterodimerization activity / DNA repair / DNA damage response / chromatin binding / regulation of DNA-templated transcription / regulation of transcription by RNA polymerase II / chromatin / nucleolus / positive regulation of transcription by RNA polymerase II / ATP hydrolysis activity / DNA binding / nucleoplasm / ATP binding / nucleus 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |  Homo sapiens (ヒト) / Homo sapiens (ヒト) / | |||||||||||||||
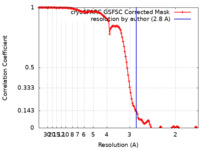
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.8 Å | |||||||||||||||
 データ登録者 データ登録者 | Chio US / Palovcak E / Armache JP / Narlikar GJ / Cheng Y | |||||||||||||||
| 資金援助 |  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Functionalized graphene-oxide grids enable high-resolution cryo-EM structures of the SNF2h-nucleosome complex without crosslinking. 著者: Un Seng Chio / Eugene Palovcak / Anton A A Smith / Henriette Autzen / Elise N Muñoz / Zanlin Yu / Feng Wang / David A Agard / Jean-Paul Armache / Geeta J Narlikar / Yifan Cheng /   要旨: Single-particle cryo-EM is widely used to determine enzyme-nucleosome complex structures. However, cryo-EM sample preparation remains challenging and inconsistent due to complex denaturation at the ...Single-particle cryo-EM is widely used to determine enzyme-nucleosome complex structures. However, cryo-EM sample preparation remains challenging and inconsistent due to complex denaturation at the air-water interface (AWI). Here, to address this issue, we develop graphene-oxide-coated EM grids functionalized with either single-stranded DNA (ssDNA) or thiol-poly(acrylic acid-co-styrene) (TAASTY) co-polymer. These grids protect complexes between the chromatin remodeler SNF2h and nucleosomes from the AWI and facilitate collection of high-quality micrographs of intact SNF2h-nucleosome complexes in the absence of crosslinking. The data yields maps ranging from 2.3 to 3 Å in resolution. 3D variability analysis reveals nucleotide-state linked conformational changes in SNF2h bound to a nucleosome. In addition, the analysis provides structural evidence for asymmetric coordination between two SNF2h protomers acting on the same nucleosome. We envision these grids will enable similar detailed structural analyses for other enzyme-nucleosome complexes and possibly other protein-nucleic acid complexes in general. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_43002.map.gz emd_43002.map.gz | 108.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-43002-v30.xml emd-43002-v30.xml emd-43002.xml emd-43002.xml | 30.8 KB 30.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_43002_fsc.xml emd_43002_fsc.xml | 12.7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_43002.png emd_43002.png | 106.9 KB | ||
| Filedesc metadata |  emd-43002.cif.gz emd-43002.cif.gz | 8.5 KB | ||
| その他 |  emd_43002_half_map_1.map.gz emd_43002_half_map_1.map.gz emd_43002_half_map_2.map.gz emd_43002_half_map_2.map.gz | 200.2 MB 200.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-43002 http://ftp.pdbj.org/pub/emdb/structures/EMD-43002 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43002 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-43002 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_43002_validation.pdf.gz emd_43002_validation.pdf.gz | 1.2 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_43002_full_validation.pdf.gz emd_43002_full_validation.pdf.gz | 1.2 MB | 表示 | |
| XML形式データ |  emd_43002_validation.xml.gz emd_43002_validation.xml.gz | 21.4 KB | 表示 | |
| CIF形式データ |  emd_43002_validation.cif.gz emd_43002_validation.cif.gz | 27.4 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43002 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43002 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43002 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-43002 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8v6vMC  8v4yC  8v7lC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_43002.map.gz / 形式: CCP4 / 大きさ: 216 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_43002.map.gz / 形式: CCP4 / 大きさ: 216 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Double-bound SNF2h-nucleosome structure (cryoSPARC local refinement) | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.8468 Å | ||||||||||||||||||||||||||||||||||||
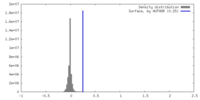
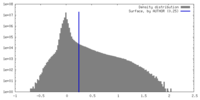
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half map A
| ファイル | emd_43002_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map A | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
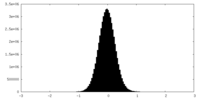
| 密度ヒストグラム |
-ハーフマップ: Half map B
| ファイル | emd_43002_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map B | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
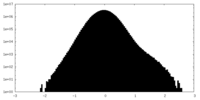
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
+全体 : ATP-dependent chromatin remodeler SNF2h in complex with nucleosome
+超分子 #1: ATP-dependent chromatin remodeler SNF2h in complex with nucleosome
+超分子 #2: Nucleosome with Xenopus laevis histones
+超分子 #3: SNF2h
+分子 #1: Histone H3.2
+分子 #2: Histone H4
+分子 #3: Histone H2A type 1
+分子 #4: Histone H2B
+分子 #7: SWI/SNF-related matrix-associated actin-dependent regulator of ch...
+分子 #5: Widom 601 DNA (147-mer) with 60 base pairs flanking DNA (reverse ...
+分子 #6: Widom 601 DNA (147-mer) with 60 base pairs flanking DNA (forward ...
+分子 #8: ADENOSINE-5'-DIPHOSPHATE
+分子 #9: MAGNESIUM ION
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 構成要素:
詳細: 12.5 mM HEPES-KOH, pH 7.5, 60 mM KCl, 5 mM MgCl2, 2 mM ADP, 2 mM BeSO4, 10 mM NaF, 1.5% glycerol | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - 材質: GRAPHENE OXIDE / 支持フィルム - トポロジー: CONTINUOUS / 支持フィルム - Film thickness: 1 | ||||||||||||||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV | ||||||||||||||||||||||||
| 詳細 | 100 nM nucleosome with 500 nM SNF2h |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 66.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.8 µm / 最小 デフォーカス(公称値): 0.5 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー














 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)