+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | CryoEM Structure of Computationally Designed Nanocage O32-ZL4 | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | O32-ZL4 / DE NOVO PROTEIN | |||||||||
| 機能・相同性 | D-galactonate catabolic process / 2-dehydro-3-deoxy-6-phosphogalactonate aldolase activity / KDPG/KHG aldolase / KDPG and KHG aldolase / Aldolase-type TIM barrel / 2-dehydro-3-deoxyphosphogluconate aldolase/4-hydroxy-2-oxoglutarate aldolase 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |   Thermotoga maritima (バクテリア) / synthetic construct (人工物) Thermotoga maritima (バクテリア) / synthetic construct (人工物) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.9 Å | |||||||||
 データ登録者 データ登録者 | Weidle C / Borst A | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Mater / 年: 2023 ジャーナル: Nat Mater / 年: 2023タイトル: Accurate computational design of three-dimensional protein crystals. 著者: Zhe Li / Shunzhi Wang / Una Nattermann / Asim K Bera / Andrew J Borst / Muammer Y Yaman / Matthew J Bick / Erin C Yang / William Sheffler / Byeongdu Lee / Soenke Seifert / Greg L Hura / ...著者: Zhe Li / Shunzhi Wang / Una Nattermann / Asim K Bera / Andrew J Borst / Muammer Y Yaman / Matthew J Bick / Erin C Yang / William Sheffler / Byeongdu Lee / Soenke Seifert / Greg L Hura / Hannah Nguyen / Alex Kang / Radhika Dalal / Joshua M Lubner / Yang Hsia / Hugh Haddox / Alexis Courbet / Quinton Dowling / Marcos Miranda / Andrew Favor / Ali Etemadi / Natasha I Edman / Wei Yang / Connor Weidle / Banumathi Sankaran / Babak Negahdari / Michael B Ross / David S Ginger / David Baker /   要旨: Protein crystallization plays a central role in structural biology. Despite this, the process of crystallization remains poorly understood and highly empirical, with crystal contacts, lattice packing ...Protein crystallization plays a central role in structural biology. Despite this, the process of crystallization remains poorly understood and highly empirical, with crystal contacts, lattice packing arrangements and space group preferences being largely unpredictable. Programming protein crystallization through precisely engineered side-chain-side-chain interactions across protein-protein interfaces is an outstanding challenge. Here we develop a general computational approach for designing three-dimensional protein crystals with prespecified lattice architectures at atomic accuracy that hierarchically constrains the overall number of degrees of freedom of the system. We design three pairs of oligomers that can be individually purified, and upon mixing, spontaneously self-assemble into >100 µm three-dimensional crystals. The structures of these crystals are nearly identical to the computational design models, closely corresponding in both overall architecture and the specific protein-protein interactions. The dimensions of the crystal unit cell can be systematically redesigned while retaining the space group symmetry and overall architecture, and the crystals are extremely porous and highly stable. Our approach enables the computational design of protein crystals with high accuracy, and the designed protein crystals, which have both structural and assembly information encoded in their primary sequences, provide a powerful platform for biological materials engineering. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_40926.map.gz emd_40926.map.gz | 266.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-40926-v30.xml emd-40926-v30.xml emd-40926.xml emd-40926.xml | 18.4 KB 18.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
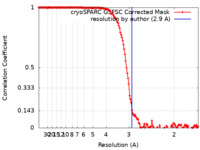
| FSC (解像度算出) |  emd_40926_fsc.xml emd_40926_fsc.xml | 13.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_40926.png emd_40926.png | 107.3 KB | ||
| Filedesc metadata |  emd-40926.cif.gz emd-40926.cif.gz | 6.4 KB | ||
| その他 |  emd_40926_half_map_1.map.gz emd_40926_half_map_1.map.gz emd_40926_half_map_2.map.gz emd_40926_half_map_2.map.gz | 261.6 MB 261.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-40926 http://ftp.pdbj.org/pub/emdb/structures/EMD-40926 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-40926 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-40926 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_40926_validation.pdf.gz emd_40926_validation.pdf.gz | 942.1 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_40926_full_validation.pdf.gz emd_40926_full_validation.pdf.gz | 941.6 KB | 表示 | |
| XML形式データ |  emd_40926_validation.xml.gz emd_40926_validation.xml.gz | 23 KB | 表示 | |
| CIF形式データ |  emd_40926_validation.cif.gz emd_40926_validation.cif.gz | 29.9 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-40926 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-40926 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-40926 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-40926 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8szzMC  8cusC  8cutC  8cuuC  8cuvC  8cuwC  8cuxC  8cwsC  8cwyC  8cwzC  8farC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_40926.map.gz / 形式: CCP4 / 大きさ: 282.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_40926.map.gz / 形式: CCP4 / 大きさ: 282.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.84 Å | ||||||||||||||||||||||||||||||||||||
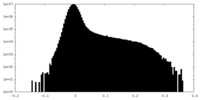
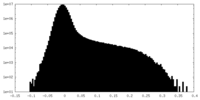
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_40926_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
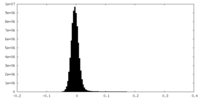
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_40926_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
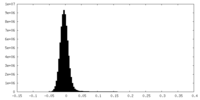
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : O32-ZL4
| 全体 | 名称: O32-ZL4 |
|---|---|
| 要素 |
|
-超分子 #1: O32-ZL4
| 超分子 | 名称: O32-ZL4 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 詳細: These two proteins were co expressed from the same plasmid and assembled inside E. coli into cages. O32-ZL4 was purified using the His tag on B component |
|---|---|
| 由来(天然) | 生物種:   Thermotoga maritima (バクテリア) Thermotoga maritima (バクテリア) |
| 分子量 | 理論値: 764.91792 KDa |
-分子 #1: O32-ZL4 Component A
| 分子 | 名称: O32-ZL4 Component A / タイプ: protein_or_peptide / ID: 1 / コピー数: 24 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
| 分子量 | 理論値: 8.766459 KDa |
| 配列 | 文字列: MTDELLRLAK EQAELLKEIK ILVELIAMLV KVIQKDPSDE ALKALAELVR KLKELVEDME RSMKEQLYII KGSWSG |
-分子 #2: O32-ZL4 Component B
| 分子 | 名称: O32-ZL4 Component B / タイプ: protein_or_peptide / ID: 2 / コピー数: 24 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:   Thermotoga maritima (バクテリア) Thermotoga maritima (バクテリア) |
| 分子量 | 理論値: 23.170152 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MKMEELFKKH KIVAVLRAND AQEAREKALA VFEGGVHLIE ITFTVPNAAA VILLLSFLKE KGAIIGAGTV TSEEQCALAV LSGAEFIVS PHLDEEISQF CKEKGVFYMP GVMTPTELVK AMKLGHTILK LFPGEVVGPQ FVKAMKGPFP NVKFVPTGGV N LDNVCEWF ...文字列: MKMEELFKKH KIVAVLRAND AQEAREKALA VFEGGVHLIE ITFTVPNAAA VILLLSFLKE KGAIIGAGTV TSEEQCALAV LSGAEFIVS PHLDEEISQF CKEKGVFYMP GVMTPTELVK AMKLGHTILK LFPGEVVGPQ FVKAMKGPFP NVKFVPTGGV N LDNVCEWF KAGVLAVGVG SALVKGTPDE VREKAKAFVE KIRGCTELEH HHHHH UniProtKB: 2-dehydro-3-deoxyphosphogluconate aldolase/4-hydroxy-2-oxoglutarate aldolase |
-分子 #3: SODIUM ION
| 分子 | 名称: SODIUM ION / タイプ: ligand / ID: 3 / コピー数: 24 |
|---|---|
| 分子量 | 理論値: 22.99 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 2.1 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
詳細: 25 mM Tris/HCl pH 7.5, 150 mM NaCl | |||||||||
| グリッド | モデル: Quantifoil R2/2 / 材質: COPPER / メッシュ: 300 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: CONTINUOUS / 支持フィルム - Film thickness: 2 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 30 sec. / 前処理 - 気圧: 0.0001 kPa | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV | |||||||||
| 詳細 | 25 mM Tris, 150 mM NaCl |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.8 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | Chain - Source name: Other / Chain - Initial model type: in silico model / 詳細: Computational model |
|---|---|
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL / 温度因子: 144.9 当てはまり具合の基準: Cross-correlation coefficient |
| 得られたモデル |  PDB-8szz: |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)