+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Composite map of the Rad51-ADP filament | |||||||||
 マップデータ マップデータ | This is a composite map with a high-resolution map (3.14 A) of the central part of the helix combined with the other part from a lower-resolution map (3.58A). | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Recombinase / ATPase / DNA repair protein / DNA binding / RECOMBINATION | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | らせん対称体再構成法 / クライオ電子顕微鏡法 / 解像度: 3.58 Å | |||||||||
 データ登録者 データ登録者 | Miki Y / Luo SC / Ho MC | |||||||||
| 資金援助 |  台湾, 1件 台湾, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2023 ジャーナル: Nat Commun / 年: 2023タイトル: A RAD51-ADP double filament structure unveils the mechanism of filament dynamics in homologous recombination. 著者: Shih-Chi Luo / Min-Chi Yeh / Yu-Hsiang Lien / Hsin-Yi Yeh / Huei-Lun Siao / I-Ping Tu / Peter Chi / Meng-Chiao Ho /  要旨: ATP-dependent RAD51 recombinases play an essential role in eukaryotic homologous recombination by catalyzing a four-step process: 1) formation of a RAD51 single-filament assembly on ssDNA in the ...ATP-dependent RAD51 recombinases play an essential role in eukaryotic homologous recombination by catalyzing a four-step process: 1) formation of a RAD51 single-filament assembly on ssDNA in the presence of ATP, 2) complementary DNA strand-exchange, 3) ATP hydrolysis transforming the RAD51 filament into an ADP-bound disassembly-competent state, and 4) RAD51 disassembly to provide access for DNA repairing enzymes. Of these steps, filament dynamics between the ATP- and ADP-bound states, and the RAD51 disassembly mechanism, are poorly understood due to the lack of near-atomic-resolution information of the ADP-bound RAD51-DNA filament structure. We report the cryo-EM structure of ADP-bound RAD51-DNA filaments at 3.1 Å resolution, revealing a unique RAD51 double-filament that wraps around ssDNA. Structural analysis, supported by ATP-chase and time-resolved cryo-EM experiments, reveals a collapsing mechanism involving two four-protomer movements along ssDNA for mechanical transition between RAD51 single- and double-filament without RAD51 dissociation. This mechanism enables elastic change of RAD51 filament length during structural transitions between ATP- and ADP-states. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_36040.map.gz emd_36040.map.gz | 194.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-36040-v30.xml emd-36040-v30.xml emd-36040.xml emd-36040.xml | 16.1 KB 16.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_36040.png emd_36040.png | 2.5 MB | ||
| その他 |  emd_36040_additional_1.map.gz emd_36040_additional_1.map.gz emd_36040_half_map_1.map.gz emd_36040_half_map_1.map.gz emd_36040_half_map_2.map.gz emd_36040_half_map_2.map.gz | 203.1 MB 199.2 MB 199.2 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-36040 http://ftp.pdbj.org/pub/emdb/structures/EMD-36040 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-36040 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-36040 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_36040_validation.pdf.gz emd_36040_validation.pdf.gz | 868 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_36040_full_validation.pdf.gz emd_36040_full_validation.pdf.gz | 867.6 KB | 表示 | |
| XML形式データ |  emd_36040_validation.xml.gz emd_36040_validation.xml.gz | 15.7 KB | 表示 | |
| CIF形式データ |  emd_36040_validation.cif.gz emd_36040_validation.cif.gz | 18.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-36040 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-36040 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-36040 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-36040 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_36040.map.gz / 形式: CCP4 / 大きさ: 216 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_36040.map.gz / 形式: CCP4 / 大きさ: 216 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | This is a composite map with a high-resolution map (3.14 A) of the central part of the helix combined with the other part from a lower-resolution map (3.58A). | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.83 Å | ||||||||||||||||||||||||||||||||||||
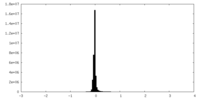
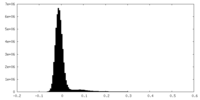
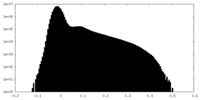
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: This is the consensus low-resolution density map (3.58...
| ファイル | emd_36040_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
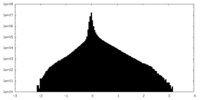
| 注釈 | This is the consensus low-resolution density map (3.58 A) used for composite map generation with a high-resolution map (3.14 A) locally refined in the central part of the helix. | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: This is half map A of the consensus map.
| ファイル | emd_36040_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
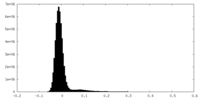
| 注釈 | This is half map A of the consensus map. | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: This is half map B of the consensus map.
| ファイル | emd_36040_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
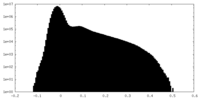
| 注釈 | This is half map B of the consensus map. | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : hRAD51-ADP filament intermediate
| 全体 | 名称: hRAD51-ADP filament intermediate |
|---|---|
| 要素 |
|
-超分子 #1: hRAD51-ADP filament intermediate
| 超分子 | 名称: hRAD51-ADP filament intermediate / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: hRAD51 protein filament assembled in the presence of ADP and single strand DNA |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: DNA repair protein RAD51 homolog 1
| 分子 | 名称: DNA repair protein RAD51 homolog 1 / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MAMQMQLEAN ADTSVEEESF GPQPISRLEQ CGINANDVKK LEEAGFHTVE AVAYAPKKEL INIKGISEAK ADKILAEAAK LVPMGFTTA TEFHQRRSEI IQITTGSKEL DKLLQGGIET GSITEMFGEF RTGKTQICHT LAVTCQLPID RGGGEGKAMY I DTEGTFRP ...文字列: MAMQMQLEAN ADTSVEEESF GPQPISRLEQ CGINANDVKK LEEAGFHTVE AVAYAPKKEL INIKGISEAK ADKILAEAAK LVPMGFTTA TEFHQRRSEI IQITTGSKEL DKLLQGGIET GSITEMFGEF RTGKTQICHT LAVTCQLPID RGGGEGKAMY I DTEGTFRP ERLLAVAERY GLSGSDVLDN VAYARAFNTD HQTQLLYQAS AMMVESRYAL LIVDSATALY RTDYSGRGEL SA RQMHLAR FLRMLLRLAD EFGVAVVITN QVVAQVDGAA MFAADPKKPI GGNIIAHAST TRLYLRKGRG ETRICKIYDS PCL PEAEAM FAINADGVGD AKD |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 緩衝液 | pH: 7.4 |
|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK III |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 1.0 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 想定した対称性 - らせんパラメータ - Δz: 9.8 Å 想定した対称性 - らせんパラメータ - ΔΦ: 155.6 ° 想定した対称性 - らせんパラメータ - 軸対称性: C1 (非対称) 解像度のタイプ: BY AUTHOR / 解像度: 3.58 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 2622222 |
|---|---|
| 初期モデル | モデルのタイプ: INSILICO MODEL |
| 最終 角度割当 | タイプ: NOT APPLICABLE |
 ムービー
ムービー コントローラー
コントローラー






 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)