+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of p97:UBXD1 PUB-in state | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | AAA+ / chaperone / hydrolase | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報: / flavin adenine dinucleotide catabolic process / VCP-NSFL1C complex / endosome to lysosome transport via multivesicular body sorting pathway / endoplasmic reticulum stress-induced pre-emptive quality control / BAT3 complex binding / cellular response to arsenite ion / protein-DNA covalent cross-linking repair / cytoplasm protein quality control / Derlin-1 retrotranslocation complex ...: / flavin adenine dinucleotide catabolic process / VCP-NSFL1C complex / endosome to lysosome transport via multivesicular body sorting pathway / endoplasmic reticulum stress-induced pre-emptive quality control / BAT3 complex binding / cellular response to arsenite ion / protein-DNA covalent cross-linking repair / cytoplasm protein quality control / Derlin-1 retrotranslocation complex / positive regulation of protein K63-linked deubiquitination / positive regulation of oxidative phosphorylation / : / aggresome assembly / deubiquitinase activator activity / regulation of protein localization to chromatin / ubiquitin-modified protein reader activity / mitotic spindle disassembly / VCP-NPL4-UFD1 AAA ATPase complex / cellular response to misfolded protein / negative regulation of protein localization to chromatin / vesicle-fusing ATPase / positive regulation of mitochondrial membrane potential / K48-linked polyubiquitin modification-dependent protein binding / regulation of aerobic respiration / retrograde protein transport, ER to cytosol / stress granule disassembly / regulation of synapse organization / ATPase complex / ubiquitin-specific protease binding / MHC class I protein binding / positive regulation of ATP biosynthetic process / ubiquitin-like protein ligase binding / RHOH GTPase cycle / polyubiquitin modification-dependent protein binding / autophagosome maturation / endoplasmic reticulum to Golgi vesicle-mediated transport / negative regulation of hippo signaling / HSF1 activation / translesion synthesis / interstrand cross-link repair / proteasomal protein catabolic process / ATP metabolic process / endoplasmic reticulum unfolded protein response / Protein methylation / Attachment and Entry / Josephin domain DUBs / ERAD pathway / lipid droplet / N-glycan trimming in the ER and Calnexin/Calreticulin cycle / proteasome complex / viral genome replication / Hh mutants are degraded by ERAD / Hedgehog ligand biogenesis / Defective CFTR causes cystic fibrosis / Translesion Synthesis by POLH / negative regulation of smoothened signaling pathway / macroautophagy / positive regulation of protein-containing complex assembly / ABC-family proteins mediated transport / establishment of protein localization / positive regulation of non-canonical NF-kappaB signal transduction / ADP binding / autophagy / Aggrephagy / Ovarian tumor domain proteases / KEAP1-NFE2L2 pathway / cytoplasmic stress granule / positive regulation of protein catabolic process / azurophil granule lumen / late endosome membrane / positive regulation of canonical Wnt signaling pathway / E3 ubiquitin ligases ubiquitinate target proteins / positive regulation of proteasomal ubiquitin-dependent protein catabolic process / site of double-strand break / double-strand break repair / Neddylation / cellular response to heat / ATPase binding / ubiquitin-dependent protein catabolic process / early endosome membrane / protein phosphatase binding / secretory granule lumen / regulation of apoptotic process / proteasome-mediated ubiquitin-dependent protein catabolic process / ficolin-1-rich granule lumen / Attachment and Entry / protein ubiquitination / endosome / ciliary basal body / protein domain specific binding / lysosomal membrane / DNA repair / intracellular membrane-bounded organelle / ubiquitin protein ligase binding / lipid binding / centrosome / DNA damage response / endoplasmic reticulum membrane / Neutrophil degranulation 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.93 Å | |||||||||
 データ登録者 データ登録者 | Braxton JR / Tucker MR / Tse E / Southworth DR | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 | ジャーナル: bioRxiv / 年: 2023 タイトル: The p97/VCP adapter UBXD1 drives AAA+ remodeling and ring opening through multi-domain tethered interactions. 著者: Julian R Braxton / Chad R Altobelli / Maxwell R Tucker / Eric Tse / Aye C Thwin / Michelle R Arkin / Daniel R Southworth /  要旨: p97/VCP is an essential cytosolic AAA+ ATPase hexamer that extracts and unfolds substrate polypeptides during protein homeostasis and degradation. Distinct sets of p97 adapters guide cellular ...p97/VCP is an essential cytosolic AAA+ ATPase hexamer that extracts and unfolds substrate polypeptides during protein homeostasis and degradation. Distinct sets of p97 adapters guide cellular functions but their roles in direct control of the hexamer are unclear. The UBXD1 adapter localizes with p97 in critical mitochondria and lysosome clearance pathways and contains multiple p97-interacting domains. We identify UBXD1 as a potent p97 ATPase inhibitor and report structures of intact p97:UBXD1 complexes that reveal extensive UBXD1 contacts across p97 and an asymmetric remodeling of the hexamer. Conserved VIM, UBX, and PUB domains tether adjacent protomers while a connecting strand forms an N-terminal domain lariat with a helix wedged at the interprotomer interface. An additional VIM-connecting helix binds along the second AAA+ domain. Together these contacts split the hexamer into a ring-open conformation. Structures, mutagenesis, and comparisons to other adapters further reveal how adapters containing conserved p97-remodeling motifs regulate p97 ATPase activity and structure. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_28990.map.gz emd_28990.map.gz | 230.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-28990-v30.xml emd-28990-v30.xml emd-28990.xml emd-28990.xml | 24.1 KB 24.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_28990.png emd_28990.png | 241.6 KB | ||
| Filedesc metadata |  emd-28990.cif.gz emd-28990.cif.gz | 6.9 KB | ||
| その他 |  emd_28990_additional_1.map.gz emd_28990_additional_1.map.gz emd_28990_half_map_1.map.gz emd_28990_half_map_1.map.gz emd_28990_half_map_2.map.gz emd_28990_half_map_2.map.gz | 120.6 MB 226.5 MB 226.5 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-28990 http://ftp.pdbj.org/pub/emdb/structures/EMD-28990 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28990 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-28990 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_28990_validation.pdf.gz emd_28990_validation.pdf.gz | 1.3 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_28990_full_validation.pdf.gz emd_28990_full_validation.pdf.gz | 1.3 MB | 表示 | |
| XML形式データ |  emd_28990_validation.xml.gz emd_28990_validation.xml.gz | 15.7 KB | 表示 | |
| CIF形式データ |  emd_28990_validation.cif.gz emd_28990_validation.cif.gz | 18.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28990 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28990 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28990 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-28990 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8fcqMC  8fclC  8fcmC  8fcnC  8fcoC  8fcpC  8fcrC  8fctC C: 同じ文献を引用 ( M: このマップから作成された原子モデル |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_28990.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_28990.map.gz / 形式: CCP4 / 大きさ: 244.1 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.834 Å | ||||||||||||||||||||||||||||||||||||
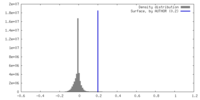
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: Unsharpened map
| ファイル | emd_28990_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Unsharpened map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
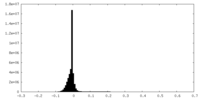
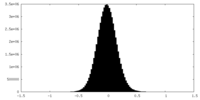
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_28990_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
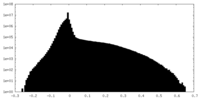
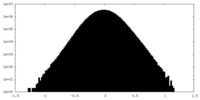
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_28990_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
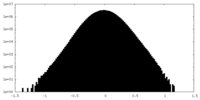
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Complex of p97 and UBXD1
| 全体 | 名称: Complex of p97 and UBXD1 |
|---|---|
| 要素 |
|
-超分子 #1: Complex of p97 and UBXD1
| 超分子 | 名称: Complex of p97 and UBXD1 / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: Transitional endoplasmic reticulum ATPase
| 分子 | 名称: Transitional endoplasmic reticulum ATPase / タイプ: protein_or_peptide / ID: 1 / コピー数: 6 / 光学異性体: LEVO / EC番号: vesicle-fusing ATPase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 89.43682 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MASGADSKGD DLSTAILKQK NRPNRLIVDE AINEDNSVVS LSQPKMDELQ LFRGDTVLLK GKKRREAVCI VLSDDTCSDE KIRMNRVVR NNLRVRLGDV ISIQPCPDVK YGKRIHVLPI DDTVEGITGN LFEVYLKPYF LEAYRPIRKG DIFLVRGGMR A VEFKVVET ...文字列: MASGADSKGD DLSTAILKQK NRPNRLIVDE AINEDNSVVS LSQPKMDELQ LFRGDTVLLK GKKRREAVCI VLSDDTCSDE KIRMNRVVR NNLRVRLGDV ISIQPCPDVK YGKRIHVLPI DDTVEGITGN LFEVYLKPYF LEAYRPIRKG DIFLVRGGMR A VEFKVVET DPSPYCIVAP DTVIHCEGEP IKREDEEESL NEVGYDDIGG CRKQLAQIKE MVELPLRHPA LFKAIGVKPP RG ILLYGPP GTGKTLIARA VANETGAFFF LINGPEIMSK LAGESESNLR KAFEEAEKNA PAIIFIDELD AIAPKREKTH GEV ERRIVS QLLTLMDGLK QRAHVIVMAA TNRPNSIDPA LRRFGRFDRE VDIGIPDATG RLEILQIHTK NMKLADDVDL EQVA NETHG HVGADLAALC SEAALQAIRK KMDLIDLEDE TIDAEVMNSL AVTMDDFRWA LSQSNPSALR ETVVEVPQVT WEDIG GLED VKRELQELVQ YPVEHPDKFL KFGMTPSKGV LFYGPPGCGK TLLAKAIANE CQANFISIKG PELLTMWFGE SEANVR EIF DKARQAAPCV LFFDELDSIA KARGGNIGDG GGAADRVINQ ILTEMDGMST KKNVFIIGAT NRPDIIDPAI LRPGRLD QL IYIPLPDEKS RVAILKANLR KSPVAKDVDL EFLAKMTNGF SGADLTEICQ RACKLAIRES IESEIRRERE RQTNPSAM E VEEDDPVPEI RRDHFEEAMR FARRSVSDND IRKYEMFAQT LQQSRGFGSF RFPSGNQGGA GPSQGSGGGT GGSVYTEDN DDDLYG UniProtKB: Transitional endoplasmic reticulum ATPase |
-分子 #2: UBX domain-containing protein 6
| 分子 | 名称: UBX domain-containing protein 6 / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 49.823656 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MKKFFQEFKA DIKFKSAGPG QKLKESVGEK AHKEKPNQPA PRPPRQGPTN EAQMAAAAAL ARLEQKQSRA WGPTSQDTIR NQVRKELQA EATVSGSPEA PGTNVVSEPR EEGSAHLAVP GVYFTCPLTG ATLRKDQRDA CIKEAILLHF STDPVAASIM K IYTFNKDQ ...文字列: MKKFFQEFKA DIKFKSAGPG QKLKESVGEK AHKEKPNQPA PRPPRQGPTN EAQMAAAAAL ARLEQKQSRA WGPTSQDTIR NQVRKELQA EATVSGSPEA PGTNVVSEPR EEGSAHLAVP GVYFTCPLTG ATLRKDQRDA CIKEAILLHF STDPVAASIM K IYTFNKDQ DRVKLGVDTI AKYLDNIHLH PEEEKYRKIK LQNKVFQERI NCLEGTHEFF EAIGFQKVLL PAQDQEDPEE FY VLSETTL AQPQSLERHK EQLLAAEPVR AKLDRQRRVF QPSPLASQFE LPGDFFNLTA EEIKREQRLR SEAVERLSVL RTK AMREKE EQRGLRKYNY TLLRVRLPDG CLLQGTFYAR ERLGAVYGFV REALQSDWLP FELLASGGQK LSEDENLALN ECGL VPSAL LTFSWDMAVL EDIKAAGAEP DSILKPELLS AIEKLL UniProtKB: UBX domain-containing protein 6 |
-分子 #3: ADENOSINE-5'-DIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 3 / コピー数: 12 / 式: ADP |
|---|---|
| 分子量 | 理論値: 427.201 Da |
| Chemical component information |  ChemComp-ADP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 1.89 mg/mL |
|---|---|
| 緩衝液 | pH: 7.4 |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: GOLD / メッシュ: 200 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 120 sec. / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.03 kPa / 詳細: Pelco easiGlow, 15 mA |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 277 K / 装置: FEI VITROBOT MARK IV / 詳細: Wait time 10 sec, blot time 3 sec, blot force 0. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 特殊光学系 | エネルギーフィルター - 名称: GIF Bioquantum / エネルギーフィルター - スリット幅: 20 eV |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 撮影したグリッド数: 1 / 実像数: 22536 / 平均露光時間: 2.024 sec. / 平均電子線量: 43.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 70.0 µm / 倍率(補正後): 59952 / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.8 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 105000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: OTHER / 詳細: Ab initio reconstruction from cryoSPARC |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / 解像度のタイプ: BY AUTHOR / 解像度: 3.93 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: cryoSPARC / 使用した粒子像数: 59126 |
| 初期 角度割当 | タイプ: RANDOM ASSIGNMENT / ソフトウェア - 名称: cryoSPARC |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD / ソフトウェア - 名称: cryoSPARC |
-原子モデル構築 1
| 精密化 | プロトコル: FLEXIBLE FIT |
|---|---|
| 得られたモデル |  PDB-8fcq: |
 ムービー
ムービー コントローラー
コントローラー




























 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)