+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-2600 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM study of the chromatin fiber reveals a double helix twisted by tetra-nucleosomal units | |||||||||
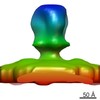
 マップデータ マップデータ | Reconstruction of 12x177 bp chromatin | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | In vitro reconstituted 12x177 bp chromatin | |||||||||
| 生物種 |  Homo sapiens (ヒト) / unidentified (未定義) Homo sapiens (ヒト) / unidentified (未定義) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 11.0 Å | |||||||||
 データ登録者 データ登録者 | Song F / Chen P / Sun D / Wang M / Dong L / Liang D / Xu RM / Zhu P / Li G | |||||||||
 引用 引用 |  ジャーナル: Science / 年: 2014 ジャーナル: Science / 年: 2014タイトル: Cryo-EM study of the chromatin fiber reveals a double helix twisted by tetranucleosomal units. 著者: Feng Song / Ping Chen / Dapeng Sun / Mingzhu Wang / Liping Dong / Dan Liang / Rui-Ming Xu / Ping Zhu / Guohong Li /  要旨: The hierarchical packaging of eukaryotic chromatin plays a central role in transcriptional regulation and other DNA-related biological processes. Here, we report the 11-angstrom-resolution cryogenic ...The hierarchical packaging of eukaryotic chromatin plays a central role in transcriptional regulation and other DNA-related biological processes. Here, we report the 11-angstrom-resolution cryogenic electron microscopy (cryo-EM) structures of 30-nanometer chromatin fibers reconstituted in the presence of linker histone H1 and with different nucleosome repeat lengths. The structures show a histone H1-dependent left-handed twist of the repeating tetranucleosomal structural units, within which the four nucleosomes zigzag back and forth with a straight linker DNA. The asymmetric binding and the location of histone H1 in chromatin play a role in the formation of the 30-nanometer fiber. Our results provide mechanistic insights into how nucleosomes compact into higher-order chromatin fibers. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_2600.map.gz emd_2600.map.gz | 10.8 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-2600-v30.xml emd-2600-v30.xml emd-2600.xml emd-2600.xml | 10.5 KB 10.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_2600.png emd_2600.png emd_2600_1.png emd_2600_1.png | 215 KB 205.5 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-2600 http://ftp.pdbj.org/pub/emdb/structures/EMD-2600 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2600 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-2600 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_2600.map.gz / 形式: CCP4 / 大きさ: 162.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_2600.map.gz / 形式: CCP4 / 大きさ: 162.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Reconstruction of 12x177 bp chromatin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.539 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : In vitro reconstituted 12x177 bp chromatin
| 全体 | 名称: In vitro reconstituted 12x177 bp chromatin |
|---|---|
| 要素 |
|
-超分子 #1000: In vitro reconstituted 12x177 bp chromatin
| 超分子 | 名称: In vitro reconstituted 12x177 bp chromatin / タイプ: sample / ID: 1000 / 集合状態: Dodecamer / Number unique components: 3 |
|---|
-分子 #1: Core histone
| 分子 | 名称: Core histone / タイプ: protein_or_peptide / ID: 1 詳細: Octameric nucleosome core histone contains 2 copies histone H2A, H2B, H3 and H4. 12 octamer units constitutes the dodecamer. コピー数: 2 / 集合状態: Octamer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種: |
| 組換発現 | 生物種:  |
-分子 #2: Histone H1.4
| 分子 | 名称: Histone H1.4 / タイプ: protein_or_peptide / ID: 2 / Name.synonym: HISTIHIE 詳細: Each octamer contains 1 copy linker histone, histone H1.4 コピー数: 12 / 集合状態: Monomer / 組換発現: Yes |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) / 別称: Human / 細胞中の位置: Nucleus Homo sapiens (ヒト) / 別称: Human / 細胞中の位置: Nucleus |
| 組換発現 | 生物種:  |
-分子 #3: 601 DNA
| 分子 | 名称: 601 DNA / タイプ: dna / ID: 3 / 詳細: 12 tandem repeats; full length 2124 bp / 分類: DNA / Structure: DOUBLE HELIX / Synthetic?: No |
|---|---|
| 由来(天然) | 生物種: unidentified (未定義) |
| 配列 | 文字列: GAGCATCCGG ATCCCCTGGA GAATCCCGGT GCCGAGGCCG CTCAATTGGT CGTAGACAGC TCTAGCACCG CTTAAACGCA CGTACGCGCT GTCCCCCGCG TTTTAACCGC CAAGGGGATT ACTCCCTAGT CTCCAGGCAC GTGTCACATA TATACATCCT GTTCCAGTGC CGGACCC |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 / 詳細: 10 mM HEPES, pH 8.0, 0.1 mM EDTA |
|---|---|
| グリッド | 詳細: 300 mesh R2.1 Quantifoil holey grid |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: FEI VITROBOT MARK IV 手法: Sample absorbed for 1 to 1.5 min, blotted for 4 seconds before plunging |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| アライメント法 | Legacy - 非点収差: Objective lens astigmatism was corrected at 155,000 times magnification |
| 詳細 | Parallel beam illumination |
| 日付 | 2012年3月1日 |
| 撮影 | カテゴリ: CCD フィルム・検出器のモデル: GATAN ULTRASCAN 4000 (4k x 4k) 実像数: 4424 / 平均電子線量: 18 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 3.95 µm / 最小 デフォーカス(公称値): 1.6 µm / 倍率(公称値): 59000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| CTF補正 | 詳細: CTF correction of each particle |
|---|---|
| 最終 再構成 | 想定した対称性 - 点群: C1 (非対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 11.0 Å / 解像度の算出法: OTHER / ソフトウェア - 名称: EMAN2 / 使用した粒子像数: 21000 |
 ムービー
ムービー コントローラー
コントローラー










 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)





















