[日本語] English
 万見
万見- EMDB-25837: Cryo-EM structure of transmembrane AAA+ protease FtsH in the ADP state -
+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of transmembrane AAA+ protease FtsH in the ADP state | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | AAA+ ATPase / protease / hexamer / ADP-bound state / HYDROLASE | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; その他のペプチターゼ / ATP-dependent peptidase activity / protein catabolic process / metalloendopeptidase activity / ATP hydrolysis activity / proteolysis / zinc ion binding / ATP binding / identical protein binding / plasma membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |   Thermotoga maritima (バクテリア) Thermotoga maritima (バクテリア) | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.15 Å | |||||||||
 データ登録者 データ登録者 | Liu W / Schoonen M | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Commun Biol / 年: 2022 ジャーナル: Commun Biol / 年: 2022タイトル: Cryo-EM structure of transmembrane AAA+ protease FtsH in the ADP state. 著者: Wu Liu / Martien Schoonen / Tong Wang / Sean McSweeney / Qun Liu /  要旨: AAA+ proteases regulate numerous physiological and cellular processes through tightly regulated proteolytic cleavage of protein substrates driven by ATP hydrolysis. FtsH is the only known family of ...AAA+ proteases regulate numerous physiological and cellular processes through tightly regulated proteolytic cleavage of protein substrates driven by ATP hydrolysis. FtsH is the only known family of membrane-anchored AAA+ proteases essential for membrane protein quality control. Although a spiral staircase rotation mechanism for substrate translocation across the FtsH pore has been proposed, the detailed conformational changes among various states have not been clear due to absence of FtsH structures in these states. We report here the cryo-EM structure for Thermotoga maritima FtsH (TmFtsH) in a fully ADP-bound symmetric state. Comparisons of the ADP-state structure with its apo-state and a substrate-engaged yeast YME1 structure show conformational changes in the ATPase domains, rather than the protease domains. A reconstruction of the full-length TmFtsH provides structural insights for the dynamic transmembrane and the periplasmic domains. Our structural analyses expand the understanding of conformational switches between different nucleotide states in ATP hydrolysis by FtsH. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_25837.map.gz emd_25837.map.gz | 15.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-25837-v30.xml emd-25837-v30.xml emd-25837.xml emd-25837.xml | 9.7 KB 9.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
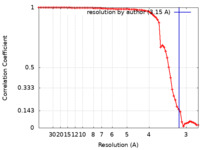
| FSC (解像度算出) |  emd_25837_fsc.xml emd_25837_fsc.xml | 7 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_25837.png emd_25837.png | 177.2 KB | ||
| Filedesc metadata |  emd-25837.cif.gz emd-25837.cif.gz | 5.3 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-25837 http://ftp.pdbj.org/pub/emdb/structures/EMD-25837 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-25837 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-25837 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_25837_validation.pdf.gz emd_25837_validation.pdf.gz | 500.7 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_25837_full_validation.pdf.gz emd_25837_full_validation.pdf.gz | 500.3 KB | 表示 | |
| XML形式データ |  emd_25837_validation.xml.gz emd_25837_validation.xml.gz | 9.7 KB | 表示 | |
| CIF形式データ |  emd_25837_validation.cif.gz emd_25837_validation.cif.gz | 12.5 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25837 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25837 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25837 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-25837 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7tdoMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_25837.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_25837.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.3684 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Hexameric FtsH in the ADP-bound state
| 全体 | 名称: Hexameric FtsH in the ADP-bound state |
|---|---|
| 要素 |
|
-超分子 #1: Hexameric FtsH in the ADP-bound state
| 超分子 | 名称: Hexameric FtsH in the ADP-bound state / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:   Thermotoga maritima (バクテリア) Thermotoga maritima (バクテリア) |
-分子 #1: ATP-dependent zinc metalloprotease FtsH
| 分子 | 名称: ATP-dependent zinc metalloprotease FtsH / タイプ: protein_or_peptide / ID: 1 / コピー数: 6 / 光学異性体: LEVO EC番号: 加水分解酵素; プロテアーゼ; ペプチド結合加水分解酵素; その他のペプチターゼ |
|---|---|
| 由来(天然) | 生物種:   Thermotoga maritima (バクテリア) Thermotoga maritima (バクテリア) |
| 分子量 | 理論値: 68.489664 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SNAMNRSNIW NLLFTILIIV TLFWLARFFY VENSPVSKLS YTSFVQMVED ERSVVSEVVI RDDGVLRVYT KDGRVYEVDA PWAVNDSQL IEKLVSKGIK VSGERSGSSS FWINVLGTLI PTILFIVVWL FIMRSLSGRN NQAFTFTKSR ATMYKPSGNK R VTFKDVGG ...文字列: SNAMNRSNIW NLLFTILIIV TLFWLARFFY VENSPVSKLS YTSFVQMVED ERSVVSEVVI RDDGVLRVYT KDGRVYEVDA PWAVNDSQL IEKLVSKGIK VSGERSGSSS FWINVLGTLI PTILFIVVWL FIMRSLSGRN NQAFTFTKSR ATMYKPSGNK R VTFKDVGG AEEAIEELKE VVEFLKDPSK FNRIGARMPK GILLVGPPGT GKTLLARAVA GEANVPFFHI SGSDFVELFV GV GAARVRD LFAQAKAHAP CIVFIDEIDA VGRHRGAGLG GGHDEREQTL NQLLVEMDGF DSKEGIIVMA ATNRPDILDP ALL RPGRFD KKIVVDPPDM LGRKKILEIH TRNKPLAEDV NLEIIAKRTP GFVGADLENL VNEAALLAAR EGRDKITMKD FEEA IDRVI AGPARKSKLI SPKEKRIIAY YEAGHAVVST VVPNGEPVHR ISIIPRGYKA LGYTLHLPEE DKYLVSRNEL LDKLT ALLG GRAAEEVVFG DVTSGAANDI ERATEIARNM VCQLGMSEEL GPLAWGKEEQ EVFLGKEITR LRNYSEEVAS KIDEEV KKI VTNCYERAKE IIRKYRKQLD NIVEILLEKE TIEGDELRRI LSEEFEKVVE UniProtKB: ATP-dependent zinc metalloprotease FtsH |
-分子 #2: ADENOSINE-5'-DIPHOSPHATE
| 分子 | 名称: ADENOSINE-5'-DIPHOSPHATE / タイプ: ligand / ID: 2 / コピー数: 6 / 式: ADP |
|---|---|
| 分子量 | 理論値: 427.201 Da |
| Chemical component information |  ChemComp-ADP: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.6 |
|---|---|
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 平均電子線量: 65.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm 最小 デフォーカス(公称値): 0.7000000000000001 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー






 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)