+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: EMDB / ID: EMD-1673 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM reconstruction of the E.Coli ClpA ATPase | |||||||||
 マップデータ マップデータ | ClpA ATPase cryo EM reconstruction | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Protease / ATPase / chaperone | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 12.6 Å | |||||||||
 データ登録者 データ登録者 | Effantin G / DeDonatis GM / Ishikawa T / Maurizi MR / Steven AC | |||||||||
 引用 引用 |  ジャーナル: Structure / 年: 2010 ジャーナル: Structure / 年: 2010タイトル: Local and global mobility in the ClpA AAA+ chaperone detected by cryo-electron microscopy: functional connotations. 著者: Grégory Effantin / Takashi Ishikawa / Gian Marco De Donatis / Michael R Maurizi / Alasdair C Steven /  要旨: The ClpA chaperone combines with the ClpP peptidase to perform targeted proteolysis in the bacterial cytoplasm. ClpA monomer has an N-terminal substrate-binding domain and two AAA+ ATPase domains (D1 ...The ClpA chaperone combines with the ClpP peptidase to perform targeted proteolysis in the bacterial cytoplasm. ClpA monomer has an N-terminal substrate-binding domain and two AAA+ ATPase domains (D1 and D2). ClpA hexamers stack axially on ClpP heptamers to form the symmetry-mismatched protease. We used cryo-electron microscopy to visualize the ClpA-ATPgammaS hexamer, in the context of ClpAP complexes. Two segments lining the axial channel show anomalously low density, indicating that these motifs, which have been implicated in substrate translocation, are mobile. We infer that ATP hydrolysis is accompanied by substantial structural changes in the D2 but not the D1 tier. The entire N domain is rendered invisible by large-scale fluctuations. When deletions of 10 and 15 residues were introduced into the linker, N domain mobility was reduced but not eliminated and changes were observed in enzymatic activities. Based on these observations, we present a pseudo-atomic model of ClpAP holoenzyme, a dynamic proteolytic nanomachine. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | EMマップ:  SurfView SurfView Molmil Molmil Jmol/JSmol Jmol/JSmol |
| 添付画像 |
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_1673.map.gz emd_1673.map.gz | 6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-1673-v30.xml emd-1673-v30.xml emd-1673.xml emd-1673.xml | 8.2 KB 8.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  1673.png 1673.png | 358.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-1673 http://ftp.pdbj.org/pub/emdb/structures/EMD-1673 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1673 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-1673 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_1673_validation.pdf.gz emd_1673_validation.pdf.gz | 219.3 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_1673_full_validation.pdf.gz emd_1673_full_validation.pdf.gz | 218.5 KB | 表示 | |
| XML形式データ |  emd_1673_validation.xml.gz emd_1673_validation.xml.gz | 5.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1673 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1673 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1673 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-1673 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_1673.map.gz / 形式: CCP4 / 大きさ: 6.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_1673.map.gz / 形式: CCP4 / 大きさ: 6.4 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | ClpA ATPase cryo EM reconstruction | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.84 Å | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
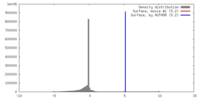
| 密度 |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
CCP4マップ ヘッダ情報:
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : E.Coli ClpA in complex with ClpP, both wild type
| 全体 | 名称: E.Coli ClpA in complex with ClpP, both wild type |
|---|---|
| 要素 |
|
-超分子 #1000: E.Coli ClpA in complex with ClpP, both wild type
| 超分子 | 名称: E.Coli ClpA in complex with ClpP, both wild type / タイプ: sample / ID: 1000 集合状態: One homohexamer of ClpA binds to one tetradecamer of ClpP Number unique components: 1 |
|---|---|
| 分子量 | 実験値: 800 KDa / 理論値: 800 KDa |
-分子 #1: clpA
| 分子 | 名称: clpA / タイプ: protein_or_peptide / ID: 1 / Name.synonym: clpA 詳細: ClpA is in complex with ClpP but only ClpA was reconstructed コピー数: 6 / 集合状態: Hexamer / 組換発現: No |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 実験値: 500 KDa / 理論値: 500 KDa |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.12 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 / 詳細: 150mM KCl, 50mM Tris-HCL,10mM MgCl2,1mM ATPgS |
| グリッド | 詳細: 300 mesh copper grid |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / 装置: OTHER / 詳細: Vitrification instrument: Vitrobot |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI/PHILIPS CM200FEG |
|---|---|
| 撮影 | カテゴリ: FILM / フィルム・検出器のモデル: KODAK SO-163 FILM / デジタル化 - スキャナー: ZEISS SCAI / デジタル化 - サンプリング間隔: 1.84 µm |
| 電子線 | 加速電圧: 120 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD / Cs: 2 mm / 倍率(公称値): 38000 |
| 試料ステージ | 試料ホルダー: Eucentric / 試料ホルダーモデル: GATAN LIQUID NITROGEN |
- 画像解析
画像解析
| 詳細 | Focal pairs were used |
|---|---|
| CTF補正 | 詳細: Each particle |
| 最終 再構成 | 想定した対称性 - 点群: C6 (6回回転対称) / アルゴリズム: OTHER / 解像度のタイプ: BY AUTHOR / 解像度: 12.6 Å / 解像度の算出法: FSC 0.5 CUT-OFF / ソフトウェア - 名称: Spider / 使用した粒子像数: 8260 |
 ムービー
ムービー コントローラー
コントローラー









 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)