+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | catalytic amyloid fibril formed by Ac-LHLHLRL-amide | |||||||||
 マップデータ マップデータ | electron density map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | catalytic amyloid fibril / protein fibril / zinc binding / prion | |||||||||
| 生物種 | synthetic construct (人工物) /  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
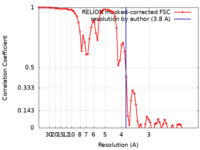
| 手法 | らせん対称体再構成法 / クライオ電子顕微鏡法 / 解像度: 3.8 Å | |||||||||
 データ登録者 データ登録者 | Heerde T / Schmidt M / Faendrich M | |||||||||
| 資金援助 |  ドイツ, 2件 ドイツ, 2件
| |||||||||
 引用 引用 |  ジャーナル: Sci Rep / 年: 2023 ジャーナル: Sci Rep / 年: 2023タイトル: Cryo-EM structure of a catalytic amyloid fibril. 著者: Thomas Heerde / Akanksha Bansal / Matthias Schmidt / Marcus Fändrich /  要旨: Catalytic amyloid fibrils are novel types of bioinspired, functional materials that combine the chemical and mechanical robustness of amyloids with the ability to catalyze a certain chemical reaction. ...Catalytic amyloid fibrils are novel types of bioinspired, functional materials that combine the chemical and mechanical robustness of amyloids with the ability to catalyze a certain chemical reaction. In this study we used cryo-electron microcopy to analyze the amyloid fibril structure and the catalytic center of amyloid fibrils that hydrolyze ester bonds. Our findings show that catalytic amyloid fibrils are polymorphic and consist of similarly structured, zipper-like building blocks that consist of mated cross-β sheets. These building blocks define the fibril core, which is decorated by a peripheral leaflet of peptide molecules. The observed structural arrangement differs from previously described catalytic amyloid fibrils and yielded a new model of the catalytic center. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_15824.map.gz emd_15824.map.gz | 694.9 KB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-15824-v30.xml emd-15824-v30.xml emd-15824.xml emd-15824.xml | 15 KB 15 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_15824_fsc.xml emd_15824_fsc.xml | 7.2 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_15824.png emd_15824.png | 34 KB | ||
| マスクデータ |  emd_15824_msk_1.map emd_15824_msk_1.map | 30.5 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-15824.cif.gz emd-15824.cif.gz | 4.9 KB | ||
| その他 |  emd_15824_half_map_1.map.gz emd_15824_half_map_1.map.gz emd_15824_half_map_2.map.gz emd_15824_half_map_2.map.gz | 22.5 MB 22.5 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-15824 http://ftp.pdbj.org/pub/emdb/structures/EMD-15824 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15824 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15824 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_15824_validation.pdf.gz emd_15824_validation.pdf.gz | 623.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_15824_full_validation.pdf.gz emd_15824_full_validation.pdf.gz | 623.2 KB | 表示 | |
| XML形式データ |  emd_15824_validation.xml.gz emd_15824_validation.xml.gz | 12.8 KB | 表示 | |
| CIF形式データ |  emd_15824_validation.cif.gz emd_15824_validation.cif.gz | 17.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15824 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15824 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15824 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-15824 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_15824.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_15824.map.gz / 形式: CCP4 / 大きさ: 30.5 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | electron density map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.04 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_15824_msk_1.map emd_15824_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: first half-map of the 3D refinement
| ファイル | emd_15824_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | first half-map of the 3D refinement | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: second half-map of the 3D refinement
| ファイル | emd_15824_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | second half-map of the 3D refinement | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : catalytic amyloid
| 全体 | 名称: catalytic amyloid |
|---|---|
| 要素 |
|
-超分子 #1: catalytic amyloid
| 超分子 | 名称: catalytic amyloid / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種: synthetic construct (人工物) |
-分子 #1: ACE-LEU-HIS-LEU-HIS-LEU-ARG-LEU-NH2
| 分子 | 名称: ACE-LEU-HIS-LEU-HIS-LEU-ARG-LEU-NH2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 30 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 928.179 Da |
| 配列 | 文字列: (ACE)LHLHLRL(NH2) |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | helical array |
- 試料調製
試料調製
| 濃度 | 0.0471 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 8 構成要素:
詳細: 25 mM Tris(hydroxymethyl)aminomethane (Tris), 1 mM Zincchloride | |||||||||
| グリッド | モデル: C-flat-1.2/1.3 / メッシュ: 400 | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 96 % / 装置: FEI VITROBOT MARK III |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 検出モード: COUNTING / 平均露光時間: 12.0 sec. / 平均電子線量: 40.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: BACKBONE TRACE / 当てはまり具合の基準: correlation coefficient |
|---|---|
| 得られたモデル |  PDB-8b3a: |
 ムービー
ムービー コントローラー
コントローラー




 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)