+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | myo-Inositol-1-Phosphate Synthase | |||||||||||||||||||||||||||
 マップデータ マップデータ | Full map of the reconstructed myo-inositol-1-phosphate synthase | |||||||||||||||||||||||||||
 試料 試料 |
| |||||||||||||||||||||||||||
| 生物種 |  Thermochaetoides thermophila (菌類) Thermochaetoides thermophila (菌類) | |||||||||||||||||||||||||||
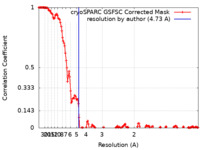
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 4.73 Å | |||||||||||||||||||||||||||
 データ登録者 データ登録者 | Janson K / Kyrilis FL / Tueting C / Alfes M / Das M / Traeger TK / Schmidt C / Hamdi F / Keller S / Meister A / Kastritis PL | |||||||||||||||||||||||||||
| 資金援助 |  ドイツ, European Union, ドイツ, European Union,  フランス, フランス,  オーストリア, 8件 オーストリア, 8件
| |||||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Biomacromolecules / 年: 2022 ジャーナル: Biomacromolecules / 年: 2022タイトル: Cryo-Electron Microscopy Snapshots of Eukaryotic Membrane Proteins in Native Lipid-Bilayer Nanodiscs. 著者: Kevin Janson / Fotis L Kyrilis / Christian Tüting / Marie Alfes / Manabendra Das / Toni K Träger / Carla Schmidt / Farzad Hamdi / Carolyn Vargas / Sandro Keller / Annette Meister / Panagiotis L Kastritis /   要旨: New technologies for purifying membrane-bound protein complexes in combination with cryo-electron microscopy (EM) have recently allowed the exploration of such complexes under near-native conditions. ...New technologies for purifying membrane-bound protein complexes in combination with cryo-electron microscopy (EM) have recently allowed the exploration of such complexes under near-native conditions. In particular, polymer-encapsulated nanodiscs enable the study of membrane proteins at high resolution while retaining protein-protein and protein-lipid interactions within a lipid bilayer. However, this powerful technology has not been exploited to address the important question of how endogenous─as opposed to overexpressed─membrane proteins are organized within a lipid environment. In this work, we demonstrate that biochemical enrichment protocols for native membrane-protein complexes from in combination with polymer-based lipid-bilayer nanodiscs provide a substantial improvement in the quality of recovered endogenous membrane-protein complexes. Mass spectrometry results revealed ∼1123 proteins, while multiple 2D class averages and two 3D reconstructions from cryo-EM data furnished prominent structural signatures. This integrated methodological approach to enriching endogenous membrane-protein complexes provides unprecedented opportunities for a deeper understanding of eukaryotic membrane proteomes. | |||||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_15517.map.gz emd_15517.map.gz | 323.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-15517-v30.xml emd-15517-v30.xml emd-15517.xml emd-15517.xml | 21.2 KB 21.2 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_15517_fsc.xml emd_15517_fsc.xml | 15 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_15517.png emd_15517.png | 54.1 KB | ||
| マスクデータ |  emd_15517_msk_1.map emd_15517_msk_1.map | 343 MB |  マスクマップ マスクマップ | |
| その他 |  emd_15517_half_map_1.map.gz emd_15517_half_map_1.map.gz emd_15517_half_map_2.map.gz emd_15517_half_map_2.map.gz | 318.7 MB 318.7 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-15517 http://ftp.pdbj.org/pub/emdb/structures/EMD-15517 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15517 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-15517 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_15517.map.gz / 形式: CCP4 / 大きさ: 343 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_15517.map.gz / 形式: CCP4 / 大きさ: 343 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Full map of the reconstructed myo-inositol-1-phosphate synthase | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.5918 Å | ||||||||||||||||||||||||||||||||||||
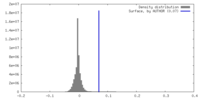
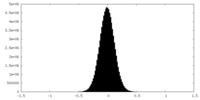
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_15517_msk_1.map emd_15517_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
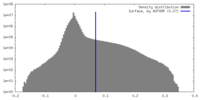
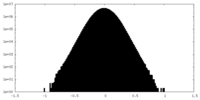
| 密度ヒストグラム |
-ハーフマップ: Half map of the reconstructed
| ファイル | emd_15517_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map of the reconstructed | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
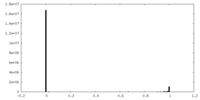
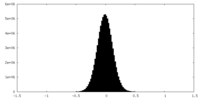
| 密度ヒストグラム |
-ハーフマップ: Half map of the reconstructed
| ファイル | emd_15517_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half map of the reconstructed | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
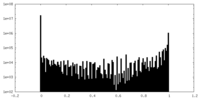
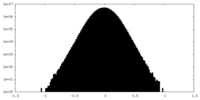
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : SB-DIBMA solubilized Chaetomium thermophilum membranes mMW fraction
| 全体 | 名称: SB-DIBMA solubilized Chaetomium thermophilum membranes mMW fraction |
|---|---|
| 要素 |
|
-超分子 #1: SB-DIBMA solubilized Chaetomium thermophilum membranes mMW fraction
| 超分子 | 名称: SB-DIBMA solubilized Chaetomium thermophilum membranes mMW fraction タイプ: complex / ID: 1 / キメラ: Yes / 親要素: 0 / 含まれる分子: all 詳細: Sample was created by solubilizing native chaetomium termophilum membranes with the aid of the copolymer SB-DIBMA |
|---|---|
| 由来(天然) | 生物種:  Thermochaetoides thermophila (菌類) Thermochaetoides thermophila (菌類) |
| 分子量 | 理論値: 120 KDa |
-分子 #1: myo-Inositol-1-Phosphate Synthase
| 分子 | 名称: myo-Inositol-1-Phosphate Synthase / タイプ: protein_or_peptide / ID: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Thermochaetoides thermophila (菌類) Thermochaetoides thermophila (菌類) |
| 配列 | 文字列: MAPHAEVDAG LANGGGQANG NGVAAAVAAP TVAPTTVSPI FKVNSPNVVY TDDEIRSKYV YRTTEVTTAE DGSLIATPRE TVYDFKVDRK LPKLGVMLVG WGGNNGSTIT AGIIANRRGL VWETRNGKQE ANYYGSVIMG STIKLGTDAK THKDINIPFH SVLPMVHPND ...文字列: MAPHAEVDAG LANGGGQANG NGVAAAVAAP TVAPTTVSPI FKVNSPNVVY TDDEIRSKYV YRTTEVTTAE DGSLIATPRE TVYDFKVDRK LPKLGVMLVG WGGNNGSTIT AGIIANRRGL VWETRNGKQE ANYYGSVIMG STIKLGTDAK THKDINIPFH SVLPMVHPND IVIGGWDISG LNLADAMDRA QVLEPSLKAL VRKEMASMKP LPSIYYPDFI AANQEDRADN ILPGNKACWE HVEEIRKNIR DFKAANGLDK VIVLWTANTE RYASIIEGVN DTADNLLNAI KNGHEEVSPS TVFAVSSILE GVPFINGSPQ NTFVPGCIEL AERHGAFIGG DDFKSGQTKM KSALVDFLIN AGIKLTSIAS YNHLGNNDGK NLSSQRQFRS KEISKSNVVD DMVEANTVLY KPGEHPDHIV VIKYVPAVGD SKRAMDEYHG EIFLGGHQTI SIANVCEDSL LASPLIIDLV IVAELMTRIQ WRLHKEDATE ADWKYFHSVL SILSYMLKAP MTPPGTPVVN ALAKQRAAMA NIFRACLGLD PENDMTLEHK LF |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.5 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.4 構成要素:
詳細: Solutions were freshly prepared, sterile filtrated, and sonicated before usage | |||||||||
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 25 sec. / 前処理 - 雰囲気: AIR / 前処理 - 気圧: 0.04 kPa 詳細: No special treatment The Grid was charged with 15 mA | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 95 % / チャンバー内温度: 277.15 K / 装置: FEI VITROBOT MARK IV / 詳細: Blotting time of 12 s Blotforce of 0. | |||||||||
| 詳細 | This sample was purified by size exclusion chromatography. Subsequently, multiple fractions in the medium molecular weight region were pooled together to obtain a higher protein concentration. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS GLACIOS |
|---|---|
| 温度 | 最低: 77.15 K / 最高: 103.15 K |
| アライメント法 | Coma free - Residual tilt: 14.7 mrad |
| 詳細 | Grid screening was performed manually until criteria for good acquisition areas was narrowed down. |
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 4048 pixel / デジタル化 - サイズ - 縦: 4048 pixel / 撮影したグリッド数: 1 / 実像数: 5912 / 平均電子線量: 64.72 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 倍率(補正後): 253464 / 照射モード: OTHER / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 240000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)