+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the NLRP3 PYD filament | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | NLRP3 / Pyrin domain / filament / IMMUNE SYSTEM | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報detection of biotic stimulus / molecular sensor activity / phosphatidylinositol phosphate binding / positive regulation of T-helper 2 cell differentiation / NLRP3 inflammasome complex assembly / positive regulation of T-helper 2 cell cytokine production / interphase microtubule organizing center / positive regulation of type 2 immune response / NLRP3 inflammasome complex / cysteine-type endopeptidase activator activity ...detection of biotic stimulus / molecular sensor activity / phosphatidylinositol phosphate binding / positive regulation of T-helper 2 cell differentiation / NLRP3 inflammasome complex assembly / positive regulation of T-helper 2 cell cytokine production / interphase microtubule organizing center / positive regulation of type 2 immune response / NLRP3 inflammasome complex / cysteine-type endopeptidase activator activity / peptidoglycan binding / osmosensory signaling pathway / phosphatidylinositol-4-phosphate binding / negative regulation of non-canonical NF-kappaB signal transduction / pattern recognition receptor signaling pathway / negative regulation of interleukin-1 beta production / pyroptotic inflammatory response / positive regulation of interleukin-4 production / microtubule organizing center / negative regulation of acute inflammatory response / The NLRP3 inflammasome / Purinergic signaling in leishmaniasis infection / signaling adaptor activity / protein maturation / positive regulation of interleukin-1 beta production / molecular condensate scaffold activity / positive regulation of non-canonical NF-kappaB signal transduction / defense response / positive regulation of NF-kappaB transcription factor activity / Cytoprotection by HMOX1 / Metalloprotease DUBs / ADP binding / protein homooligomerization / cellular response to virus / 加水分解酵素; 酸無水物に作用; 酸無水物に作用・細胞または細胞小器官の運動に関与 / negative regulation of inflammatory response / SARS-CoV-1 activates/modulates innate immune responses / positive regulation of inflammatory response / cellular response to lipopolysaccharide / regulation of inflammatory response / protein-macromolecule adaptor activity / molecular adaptor activity / DNA-binding transcription factor binding / sequence-specific DNA binding / inflammatory response / Golgi membrane / innate immune response / apoptotic process / SARS-CoV-2 activates/modulates innate and adaptive immune responses / endoplasmic reticulum / signal transduction / positive regulation of transcription by RNA polymerase II / ATP hydrolysis activity / mitochondrion / extracellular region / ATP binding / identical protein binding / nucleus / membrane / cytosol / cytoplasm 類似検索 - 分子機能 | |||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||
| 手法 | らせん対称体再構成法 / クライオ電子顕微鏡法 / 解像度: 3.6 Å | |||||||||
 データ登録者 データ登録者 | Hochheiser IV / Hagelueken G | |||||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| |||||||||
 引用 引用 |  ジャーナル: Sci Adv / 年: 2022 ジャーナル: Sci Adv / 年: 2022タイトル: Directionality of PYD filament growth determined by the transition of NLRP3 nucleation seeds to ASC elongation. 著者: Inga V Hochheiser / Heide Behrmann / Gregor Hagelueken / Juan F Rodríguez-Alcázar / Anja Kopp / Eicke Latz / Elmar Behrmann / Matthias Geyer /   要旨: Inflammasomes sense intrinsic and extrinsic danger signals to trigger inflammatory responses and pyroptotic cell death. Homotypic pyrin domain (PYD) interactions of inflammasome forming nucleotide- ...Inflammasomes sense intrinsic and extrinsic danger signals to trigger inflammatory responses and pyroptotic cell death. Homotypic pyrin domain (PYD) interactions of inflammasome forming nucleotide-binding oligomerization domain (NOD)-like receptors with the adaptor protein ASC (apoptosis-associated speck-like protein containing a CARD) mediate oligomerization into filamentous assemblies. We describe the cryo-electron microscopy (cryo-EM) structure of the human NLRP3 filament and identify a pattern of highly polar interface residues that form the homomeric interactions leading to characteristic filament ends designated as A- and B-ends. Coupling a titration polymerization assay to cryo-EM, we demonstrate that ASC adaptor protein elongation on NLRP3 nucleation seeds is unidirectional, associating exclusively to the B-end of the filament. Notably, NLRP3 and ASC PYD filaments exhibit the same symmetry in rotation and axial rise per subunit, allowing a continuous transition between NLRP3 and ASC. Integrating the directionality of filament growth, we present a molecular model of the ASC speck consisting of active NLRP3, ASC, and Caspase-1 proteins. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_13727.map.gz emd_13727.map.gz | 26.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-13727-v30.xml emd-13727-v30.xml emd-13727.xml emd-13727.xml | 10.4 KB 10.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_13727.png emd_13727.png | 77.3 KB | ||
| Filedesc metadata |  emd-13727.cif.gz emd-13727.cif.gz | 5.2 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-13727 http://ftp.pdbj.org/pub/emdb/structures/EMD-13727 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-13727 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-13727 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_13727_validation.pdf.gz emd_13727_validation.pdf.gz | 483.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_13727_full_validation.pdf.gz emd_13727_full_validation.pdf.gz | 482.8 KB | 表示 | |
| XML形式データ |  emd_13727_validation.xml.gz emd_13727_validation.xml.gz | 6 KB | 表示 | |
| CIF形式データ |  emd_13727_validation.cif.gz emd_13727_validation.cif.gz | 6.9 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13727 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13727 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13727 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-13727 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7pzdMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_13727.map.gz / 形式: CCP4 / 大きさ: 40.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_13727.map.gz / 形式: CCP4 / 大きさ: 40.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.067 Å | ||||||||||||||||||||||||||||||||||||
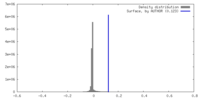
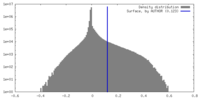
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : filament formed by the human NLRP3 Pyrin domain
| 全体 | 名称: filament formed by the human NLRP3 Pyrin domain |
|---|---|
| 要素 |
|
-超分子 #1: filament formed by the human NLRP3 Pyrin domain
| 超分子 | 名称: filament formed by the human NLRP3 Pyrin domain / タイプ: organelle_or_cellular_component / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
-分子 #1: NACHT, LRR and PYD domains-containing protein 3
| 分子 | 名称: NACHT, LRR and PYD domains-containing protein 3 / タイプ: protein_or_peptide / ID: 1 / コピー数: 18 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 12.486243 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MASTRCKLAR YLEDLEDVDL KKFKMHLEDY PPQKGCIPLP RGQTEKADHV DLATLMIDFN GEEKAWAMAV WIFAAINRRD LYEKAKRDE PKWGSDNARV SNPTVISQE UniProtKB: NACHT, LRR and PYD domains-containing protein 3 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | らせん対称体再構成法 |
| 試料の集合状態 | filament |
- 試料調製
試料調製
| 濃度 | 1.0 mg/mL |
|---|---|
| 緩衝液 | pH: 7.5 / 詳細: 20 mM HEPES (pH 7.5), 150 mM NaCl, 0.5 mM TCEP |
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 300 / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 45 sec. / 前処理 - 雰囲気: OTHER |
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 80 % / チャンバー内温度: 293 K / 装置: LEICA EM GP |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON II (4k x 4k) 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源: TUNGSTEN HAIRPIN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 最終 再構成 | 想定した対称性 - らせんパラメータ - Δz: 14.32 Å 想定した対称性 - らせんパラメータ - ΔΦ: 54.88 ° 想定した対称性 - らせんパラメータ - 軸対称性: C3 (3回回転対称) 解像度のタイプ: BY AUTHOR / 解像度: 3.6 Å / 解像度の算出法: FSC 0.143 CUT-OFF / ソフトウェア - 名称: RELION / 使用した粒子像数: 60333 |
|---|---|
| 初期モデル | モデルのタイプ: PDB ENTRY PDBモデル - PDB ID: |
| 最終 角度割当 | タイプ: NOT APPLICABLE |
 ムービー
ムービー コントローラー
コントローラー


















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)