+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of human exostosin-like 3 (EXTL3) | |||||||||||||||||||||||||||
 マップデータ マップデータ | ||||||||||||||||||||||||||||
 試料 試料 |
| |||||||||||||||||||||||||||
 キーワード キーワード | glycosyltransferase / heparan / n-acetylglucosaminyltransferase / TRANSFERASE | |||||||||||||||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報glucuronosyl-galactosyl-proteoglycan 4-alpha-N-acetylglucosaminyltransferase / glucuronyl-galactosyl-proteoglycan 4-alpha-N-acetylglucosaminyltransferase activity / positive regulation of detection of glucose / protein-hormone receptor activity / positive regulation of keratinocyte proliferation / negative regulation of keratinocyte differentiation / heparan sulfate proteoglycan biosynthetic process / negative regulation of inflammatory response to wounding / XBP1(S) activates chaperone genes / : ...glucuronosyl-galactosyl-proteoglycan 4-alpha-N-acetylglucosaminyltransferase / glucuronyl-galactosyl-proteoglycan 4-alpha-N-acetylglucosaminyltransferase activity / positive regulation of detection of glucose / protein-hormone receptor activity / positive regulation of keratinocyte proliferation / negative regulation of keratinocyte differentiation / heparan sulfate proteoglycan biosynthetic process / negative regulation of inflammatory response to wounding / XBP1(S) activates chaperone genes / : / glycosyltransferase activity / negative regulation of cytokine production involved in inflammatory response / negative regulation of inflammatory response / positive regulation of cell growth / positive regulation of phosphatidylinositol 3-kinase/protein kinase B signal transduction / endoplasmic reticulum membrane / magnesium ion binding / endoplasmic reticulum / Golgi apparatus / nucleus / plasma membrane 類似検索 - 分子機能 | |||||||||||||||||||||||||||
| 生物種 |  Homo sapiens (ヒト) Homo sapiens (ヒト) | |||||||||||||||||||||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.43 Å | |||||||||||||||||||||||||||
 データ登録者 データ登録者 | Wilson LFL / Dendooven T | |||||||||||||||||||||||||||
| 資金援助 |  英国, 英国,  スウェーデン, 8件 スウェーデン, 8件
| |||||||||||||||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2022 ジャーナル: Nat Commun / 年: 2022タイトル: The structure of EXTL3 helps to explain the different roles of bi-domain exostosins in heparan sulfate synthesis. 著者: L F L Wilson / T Dendooven / S W Hardwick / A Echevarría-Poza / T Tryfona / K B R M Krogh / D Y Chirgadze / B F Luisi / D T Logan / K Mani / P Dupree /     要旨: Heparan sulfate is a highly modified O-linked glycan that performs diverse physiological roles in animal tissues. Though quickly modified, it is initially synthesised as a polysaccharide of ...Heparan sulfate is a highly modified O-linked glycan that performs diverse physiological roles in animal tissues. Though quickly modified, it is initially synthesised as a polysaccharide of alternating β-D-glucuronosyl and N-acetyl-α-D-glucosaminyl residues by exostosins. These enzymes generally possess two glycosyltransferase domains (GT47 and GT64)-each thought to add one type of monosaccharide unit to the backbone. Although previous structures of murine exostosin-like 2 (EXTL2) provide insight into the GT64 domain, the rest of the bi-domain architecture is yet to be characterised; hence, how the two domains co-operate is unknown. Here, we report the structure of human exostosin-like 3 (EXTL3) in apo and UDP-bound forms. We explain the ineffectiveness of EXTL3's GT47 domain to transfer β-D-glucuronosyl units, and we observe that, in general, the bi-domain architecture would preclude a processive mechanism of backbone extension. We therefore propose that heparan sulfate backbone polymerisation occurs by a simple dissociative mechanism. | |||||||||||||||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_11923.map.gz emd_11923.map.gz | 264.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-11923-v30.xml emd-11923-v30.xml emd-11923.xml emd-11923.xml | 13.4 KB 13.4 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_11923_fsc.xml emd_11923_fsc.xml | 14.9 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_11923.png emd_11923.png | 216.6 KB | ||
| Filedesc metadata |  emd-11923.cif.gz emd-11923.cif.gz | 6.4 KB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-11923 http://ftp.pdbj.org/pub/emdb/structures/EMD-11923 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11923 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-11923 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_11923_validation.pdf.gz emd_11923_validation.pdf.gz | 622 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_11923_full_validation.pdf.gz emd_11923_full_validation.pdf.gz | 621.6 KB | 表示 | |
| XML形式データ |  emd_11923_validation.xml.gz emd_11923_validation.xml.gz | 14 KB | 表示 | |
| CIF形式データ |  emd_11923_validation.cif.gz emd_11923_validation.cif.gz | 19.1 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11923 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11923 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11923 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-11923 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  7au2MC  7auaC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_11923.map.gz / 形式: CCP4 / 大きさ: 282.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_11923.map.gz / 形式: CCP4 / 大きさ: 282.6 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.6667 Å | ||||||||||||||||||||||||||||||||||||
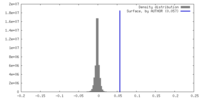
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
- 試料の構成要素
試料の構成要素
-全体 : Homodimer of EXTL3 globular domain
| 全体 | 名称: Homodimer of EXTL3 globular domain |
|---|---|
| 要素 |
|
-超分子 #1: Homodimer of EXTL3 globular domain
| 超分子 | 名称: Homodimer of EXTL3 globular domain / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 170 KDa |
-分子 #1: Exostosin-like 3
| 分子 | 名称: Exostosin-like 3 / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO EC番号: glucuronosyl-galactosyl-proteoglycan 4-alpha-N-acetylglucosaminyltransferase |
|---|---|
| 由来(天然) | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 分子量 | 理論値: 101.705117 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: APQLHHHHHH DLYENLYFQG KLTTLDEADE AGKRIFGPRV GNELCEVKHV LDLCRIRESV SEELLQLEAK RQELNSEIAK LNLKIEACK KSIENAKQDL LQLKNVISQT EHSYKELMAQ NQPKLSLPIR LLPEKDDAGL PPPKATRGCR LHNCFDYSRC P LTSGFPVY ...文字列: APQLHHHHHH DLYENLYFQG KLTTLDEADE AGKRIFGPRV GNELCEVKHV LDLCRIRESV SEELLQLEAK RQELNSEIAK LNLKIEACK KSIENAKQDL LQLKNVISQT EHSYKELMAQ NQPKLSLPIR LLPEKDDAGL PPPKATRGCR LHNCFDYSRC P LTSGFPVY VYDSDQFVFG SYLDPLVKQA FQATARANVY VTENADIACL YVILVGEMQE PVVLRPAELE KQLYSLPHWR TD GHNHVII NLSRKSDTQN LLYNVSTGRA MVAQSTFYTV QYRPGFDLVV SPLVHAMSEP NFMEIPPQVP VKRKYLFTFQ GEK IESLRS SLQEARSFEE EMEGDPPADY DDRIIATLKA VQDSKLDQVL VEFTCKNQPK PSLPTEWALC GEREDRLELL KLST FALII TPGDPRLVIS SGCATRLFEA LEVGAVPVVL GEQVQLPYQD MLQWNEAALV VPKPRVTEVH FLLRSLSDSD LLAMR RQGR FLWETYFSTA DSIFNTVLAM IRTRIQIPAA PIREEAAAEI PHRSGKAAGT DPNMADNGDL DLGPVETEPP YASPRY LRN FTLTVTDFYR SWNCAPGPFH LFPHTPFDPV LPSEAKFLGS GTGFRPIGGG AGGSGKEFQA ALGGNVPREQ FTVVMLT YE REEVLMNSLE RLNGLPYLNK VVVVWNSPKL PSEDLLWPDI GVPIMVVRTE KNSLNNRFLP WNEIETEAIL SIDDDAHL R HDEIMFGFRV WREARDRIVG FPGRYHAWDI PHQSWLYNSN YSCELSMVLT GAAFFHKYYA YLYSYVMPQA IRDMVDEYI NCEDIAMNFL VSHITRKPPI KVTSRWTFRC PGCPQALSHD DSHFHERHKC INFFVKVYGY MPLLYTQFRV DSVLFKTRLP HDKTKCFKF I UniProtKB: Exostosin-like 3 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| グリッド | モデル: Quantifoil / 材質: COPPER / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE |
| 凍結 | 凍結剤: ETHANE / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON III (4k x 4k) 検出モード: INTEGRATING / 平均電子線量: 71.4 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: SPOT SCAN / 撮影モード: BRIGHT FIELD |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 精密化 | プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-7au2: |
 ムービー
ムービー コントローラー
コントローラー







 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)