+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 8a1u | ||||||
|---|---|---|---|---|---|---|---|
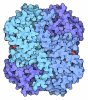
| タイトル | Sodium pumping NADH-quinone oxidoreductase with substrates NADH and Q2 | ||||||
 要素 要素 | (Na(+)-translocating NADH-quinone reductase subunit ...) x 6 | ||||||
 キーワード キーワード | MEMBRANE PROTEIN / NADH / quinone | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報NADH:ubiquinone reductase (Na+-transporting) / Gram-negative-bacterium-type cell wall / oxidoreductase activity, acting on NAD(P)H, quinone or similar compound as acceptor / sodium ion transport / FAD binding / respiratory electron transport chain / 2 iron, 2 sulfur cluster binding / transmembrane transport / FMN binding / electron transfer activity ...NADH:ubiquinone reductase (Na+-transporting) / Gram-negative-bacterium-type cell wall / oxidoreductase activity, acting on NAD(P)H, quinone or similar compound as acceptor / sodium ion transport / FAD binding / respiratory electron transport chain / 2 iron, 2 sulfur cluster binding / transmembrane transport / FMN binding / electron transfer activity / oxidoreductase activity / metal ion binding / plasma membrane 類似検索 - 分子機能 | ||||||
| 生物種 |  | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.86 Å | ||||||
 データ登録者 データ登録者 | Hau, J.-L. / Kaltwasser, S. / Vonck, J. / Fritz, G. / Steuber, J. | ||||||
| 資金援助 |  ドイツ, 1件 ドイツ, 1件
| ||||||
 引用 引用 |  ジャーナル: Nat Struct Mol Biol / 年: 2023 ジャーナル: Nat Struct Mol Biol / 年: 2023タイトル: Conformational coupling of redox-driven Na-translocation in Vibrio cholerae NADH:quinone oxidoreductase. 著者: Jann-Louis Hau / Susann Kaltwasser / Valentin Muras / Marco S Casutt / Georg Vohl / Björn Claußen / Wojtek Steffen / Alexander Leitner / Eckhard Bill / George E Cutsail / Serena DeBeer / ...著者: Jann-Louis Hau / Susann Kaltwasser / Valentin Muras / Marco S Casutt / Georg Vohl / Björn Claußen / Wojtek Steffen / Alexander Leitner / Eckhard Bill / George E Cutsail / Serena DeBeer / Janet Vonck / Julia Steuber / Günter Fritz /   要旨: In the respiratory chain, NADH oxidation is coupled to ion translocation across the membrane to build up an electrochemical gradient. In the human pathogen Vibrio cholerae, the sodium-pumping NADH: ...In the respiratory chain, NADH oxidation is coupled to ion translocation across the membrane to build up an electrochemical gradient. In the human pathogen Vibrio cholerae, the sodium-pumping NADH:quinone oxidoreductase (Na-NQR) generates a sodium gradient by a so far unknown mechanism. Here we show that ion pumping in Na-NQR is driven by large conformational changes coupling electron transfer to ion translocation. We have determined a series of cryo-EM and X-ray structures of the Na-NQR that represent snapshots of the catalytic cycle. The six subunits NqrA, B, C, D, E, and F of Na-NQR harbor a unique set of cofactors that shuttle the electrons from NADH twice across the membrane to quinone. The redox state of a unique intramembranous [2Fe-2S] cluster orchestrates the movements of subunit NqrC, which acts as an electron transfer switch. We propose that this switching movement controls the release of Na from a binding site localized in subunit NqrB. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
|---|
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  8a1u.cif.gz 8a1u.cif.gz | 733.6 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb8a1u.ent.gz pdb8a1u.ent.gz | 601.4 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  8a1u.json.gz 8a1u.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/a1/8a1u https://data.pdbj.org/pub/pdb/validation_reports/a1/8a1u ftp://data.pdbj.org/pub/pdb/validation_reports/a1/8a1u ftp://data.pdbj.org/pub/pdb/validation_reports/a1/8a1u | HTTPS FTP |
|---|
-関連構造データ
| 関連構造データ |  15089MC  8a1tC  8a1vC  8a1wC  8a1xC  8a1yC  8acwC  8acyC  8ad3C  8ad4C  8ad5C M: このデータのモデリングに利用したマップデータ C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
-Na(+)-translocating NADH-quinone reductase subunit ... , 6種, 6分子 ABCDEF
| #1: タンパク質 | 分子量: 51125.391 Da / 分子数: 1 / 由来タイプ: 組換発現 詳細: Subunit NqrA and N-terminal His6-tag and cleavage site for HRV-3C protease 由来: (組換発現)   参照: UniProt: Q9KPS1, NADH:ubiquinone reductase (Na+-transporting) |
|---|---|
| #2: タンパク質 | 分子量: 45390.883 Da / 分子数: 1 / 由来タイプ: 組換発現 / 詳細: N-terminal residues in model not resolved. / 由来: (組換発現)   参照: UniProt: Q9KPS2, NADH:ubiquinone reductase (Na+-transporting) |
| #3: タンパク質 | 分子量: 27652.270 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   参照: UniProt: P0C6E0, NADH:ubiquinone reductase (Na+-transporting) |
| #4: タンパク質 | 分子量: 22853.217 Da / 分子数: 1 / 由来タイプ: 組換発現 詳細: Residues at the N-terminus and at the C-terminus were not resolved in the density and are not part of the model. 由来: (組換発現)   参照: UniProt: Q9X4Q6, NADH:ubiquinone reductase (Na+-transporting) |
| #5: タンパク質 | 分子量: 21481.678 Da / 分子数: 1 / 由来タイプ: 組換発現 / 由来: (組換発現)   参照: UniProt: Q9X4Q7, NADH:ubiquinone reductase (Na+-transporting) |
| #6: タンパク質 | 分子量: 45113.492 Da / 分子数: 1 / 由来タイプ: 組換発現 詳細: N-terminal and C-terminal residues were not resolved in the density and are not part of the model. 由来: (組換発現)   参照: UniProt: Q9X4Q8, NADH:ubiquinone reductase (Na+-transporting) |
-糖 , 1種, 3分子 
| #9: 糖 |
|---|
-非ポリマー , 9種, 201分子 













| #7: 化合物 | | #8: 化合物 | ChemComp-RBF / | #10: 化合物 | ChemComp-3PE / #11: 化合物 | ChemComp-UQ2 / | #12: 化合物 | #13: 化合物 | #14: 化合物 | ChemComp-FAD / | #15: 化合物 | ChemComp-NAI / | #16: 水 | ChemComp-HOH / | |
|---|
-詳細
| 研究の焦点であるリガンドがあるか | N |
|---|---|
| Has protein modification | Y |
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 | 名称: NQR complex with substrates NADH and Q2 / タイプ: COMPLEX / Entity ID: #1-#6 / 由来: RECOMBINANT |
|---|---|
| 分子量 | 値: 0.22 MDa / 実験値: YES |
| 由来(天然) | 生物種:  |
| 由来(組換発現) | 生物種:  |
| 緩衝液 | pH: 7.6 |
| 試料 | 濃度: 4 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES |
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 400 divisions/in. / グリッドのタイプ: C-flat-1.2/1.3 |
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 276 K |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 215000 X / 倍率(補正後): 244328 X / 最大 デフォーカス(公称値): 2100 nm / 最小 デフォーカス(公称値): 800 nm / Cs: 2.7 mm / アライメント法: COMA FREE |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER |
| 撮影 | 平均露光時間: 4 sec. / 電子線照射量: 40 e/Å2 フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 撮影したグリッド数: 1 / 実像数: 9592 |
| 電子光学装置 | エネルギーフィルター名称: TFS Selectris X / エネルギーフィルタースリット幅: 7 eV |
- 解析
解析
| EMソフトウェア |
| ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | ||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 549586 | ||||||||||||||||||||||||||||
| 対称性 | 点対称性: C1 (非対称) | ||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 2.86 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 435715 / 対称性のタイプ: POINT | ||||||||||||||||||||||||||||
| 原子モデル構築 | プロトコル: RIGID BODY FIT / 空間: REAL | ||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 4P6V 4p6v Accession code: 4P6V / Source name: PDB / タイプ: experimental model |
 ムービー
ムービー コントローラー
コントローラー








 PDBj
PDBj