+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 | データベース: PDB / ID: 7kzz | ||||||
|---|---|---|---|---|---|---|---|
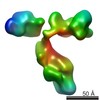
| タイトル | Cryo-EM structure of YiiP-Fab complex in Holo state | ||||||
 要素 要素 |
| ||||||
 キーワード キーワード | MEMBRANE PROTEIN / Zinc transport / cation diffusion facilitator / holo state / inward-facing state | ||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報zinc efflux active transmembrane transporter activity / cadmium ion transmembrane transporter activity / ferrous iron transmembrane transporter activity / intracellular zinc ion homeostasis / metal ion binding / plasma membrane 類似検索 - 分子機能 | ||||||
| 生物種 |  Shewanella oneidensis (バクテリア) Shewanella oneidensis (バクテリア) Homo sapiens (ヒト) Homo sapiens (ヒト) | ||||||
| 手法 | 電子顕微鏡法 / 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.42 Å | ||||||
 データ登録者 データ登録者 | Lopez-Redondo, M.L. / Fan, S. / Koide, A. / Koide, S. / Beckstein, O. / Stokes, D.L. | ||||||
| 資金援助 |  米国, 1件 米国, 1件
| ||||||
 引用 引用 |  ジャーナル: J Gen Physiol / 年: 2021 ジャーナル: J Gen Physiol / 年: 2021タイトル: Zinc binding alters the conformational dynamics and drives the transport cycle of the cation diffusion facilitator YiiP. 著者: Maria Lopez-Redondo / Shujie Fan / Akiko Koide / Shohei Koide / Oliver Beckstein / David L Stokes /  要旨: YiiP is a secondary transporter that couples Zn2+ transport to the proton motive force. Structural studies of YiiP from prokaryotes and Znt8 from humans have revealed three different Zn2+ sites and a ...YiiP is a secondary transporter that couples Zn2+ transport to the proton motive force. Structural studies of YiiP from prokaryotes and Znt8 from humans have revealed three different Zn2+ sites and a conserved homodimeric architecture. These structures define the inward-facing and outward-facing states that characterize the archetypal alternating access mechanism of transport. To study the effects of Zn2+ binding on the conformational transition, we use cryo-EM together with molecular dynamics simulation to compare structures of YiiP from Shewanella oneidensis in the presence and absence of Zn2+. To enable single-particle cryo-EM, we used a phage-display library to develop a Fab antibody fragment with high affinity for YiiP, thus producing a YiiP/Fab complex. To perform MD simulations, we developed a nonbonded dummy model for Zn2+ and validated its performance with known Zn2+-binding proteins. Using these tools, we find that, in the presence of Zn2+, YiiP adopts an inward-facing conformation consistent with that previously seen in tubular crystals. After removal of Zn2+ with high-affinity chelators, YiiP exhibits enhanced flexibility and adopts a novel conformation that appears to be intermediate between inward-facing and outward-facing states. This conformation involves closure of a hydrophobic gate that has been postulated to control access to the primary transport site. Comparison of several independent cryo-EM maps suggests that the transition from the inward-facing state is controlled by occupancy of a secondary Zn2+ site at the cytoplasmic membrane interface. This work enhances our understanding of individual Zn2+ binding sites and their role in the conformational dynamics that govern the transport cycle. | ||||||
| 履歴 |
|
- 構造の表示
構造の表示
| ムービー |
 ムービービューア ムービービューア |
|---|---|
| 構造ビューア | 分子:  Molmil Molmil Jmol/JSmol Jmol/JSmol |
- ダウンロードとリンク
ダウンロードとリンク
- ダウンロード
ダウンロード
| PDBx/mmCIF形式 |  7kzz.cif.gz 7kzz.cif.gz | 444.8 KB | 表示 |  PDBx/mmCIF形式 PDBx/mmCIF形式 |
|---|---|---|---|---|
| PDB形式 |  pdb7kzz.ent.gz pdb7kzz.ent.gz | 371.9 KB | 表示 |  PDB形式 PDB形式 |
| PDBx/mmJSON形式 |  7kzz.json.gz 7kzz.json.gz | ツリー表示 |  PDBx/mmJSON形式 PDBx/mmJSON形式 | |
| その他 |  その他のダウンロード その他のダウンロード |
-検証レポート
| 文書・要旨 |  7kzz_validation.pdf.gz 7kzz_validation.pdf.gz | 1.1 MB | 表示 |  wwPDB検証レポート wwPDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  7kzz_full_validation.pdf.gz 7kzz_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  7kzz_validation.xml.gz 7kzz_validation.xml.gz | 53.5 KB | 表示 | |
| CIF形式データ |  7kzz_validation.cif.gz 7kzz_validation.cif.gz | 80.7 KB | 表示 | |
| アーカイブディレクトリ |  https://data.pdbj.org/pub/pdb/validation_reports/kz/7kzz https://data.pdbj.org/pub/pdb/validation_reports/kz/7kzz ftp://data.pdbj.org/pub/pdb/validation_reports/kz/7kzz ftp://data.pdbj.org/pub/pdb/validation_reports/kz/7kzz | HTTPS FTP |
-関連構造データ
- リンク
リンク
- 集合体
集合体
| 登録構造単位 | 
|
|---|---|
| 1 |
|
- 要素
要素
| #1: タンパク質 | 分子量: 32485.211 Da / 分子数: 2 / 由来タイプ: 組換発現 由来: (組換発現)  Shewanella oneidensis (バクテリア) Shewanella oneidensis (バクテリア)遺伝子: fieF, SO_4475 / 発現宿主:  #2: 抗体 | 分子量: 23580.242 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 発現宿主: Homo sapiens (ヒト) / 発現宿主:  #3: 抗体 | 分子量: 25406.352 Da / 分子数: 2 / 由来タイプ: 組換発現 / 由来: (組換発現)  Homo sapiens (ヒト) / 発現宿主: Homo sapiens (ヒト) / 発現宿主:  #4: 化合物 | ChemComp-ZN / 研究の焦点であるリガンドがあるか | Y | |
|---|
-実験情報
-実験
| 実験 | 手法: 電子顕微鏡法 |
|---|---|
| EM実験 | 試料の集合状態: PARTICLE / 3次元再構成法: 単粒子再構成法 |
- 試料調製
試料調製
| 構成要素 |
| |||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 分子量 |
| |||||||||||||||||||||||||||||||||||
| 由来(天然) |
| |||||||||||||||||||||||||||||||||||
| 由来(組換発現) |
| |||||||||||||||||||||||||||||||||||
| 緩衝液 | pH: 7.5 | |||||||||||||||||||||||||||||||||||
| 緩衝液成分 |
| |||||||||||||||||||||||||||||||||||
| 試料 | 濃度: 3 mg/ml / 包埋: NO / シャドウイング: NO / 染色: NO / 凍結: YES 詳細: YiiP-Fab2R complex purified through SEC with DM, the same day as grid freezing. Main Peak fraction was used for freezing. | |||||||||||||||||||||||||||||||||||
| 試料支持 | グリッドの材料: COPPER / グリッドのサイズ: 400 divisions/in. / グリッドのタイプ: C-flat-1.2/1.3 | |||||||||||||||||||||||||||||||||||
| 急速凍結 | 装置: FEI VITROBOT MARK IV / 凍結剤: ETHANE / 湿度: 100 % / 凍結前の試料温度: 277 K 詳細: 3 uL of protein mixture applied to grid. Blot time 4 seconds, blot force 0. |
- 電子顕微鏡撮影
電子顕微鏡撮影
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
|---|---|
| 顕微鏡 | モデル: FEI TITAN KRIOS |
| 電子銃 | 電子線源:  FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM FIELD EMISSION GUN / 加速電圧: 300 kV / 照射モード: FLOOD BEAM |
| 電子レンズ | モード: BRIGHT FIELD / 倍率(公称値): 130000 X / 最大 デフォーカス(公称値): 2500 nm / 最小 デフォーカス(公称値): 1000 nm / Cs: 2.7 mm / C2レンズ絞り径: 70 µm / アライメント法: COMA FREE |
| 試料ホルダ | 凍結剤: NITROGEN 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER 最高温度: 77 K / 最低温度: 77 K |
| 撮影 | 平均露光時間: 9 sec. / 電子線照射量: 50 e/Å2 フィルム・検出器のモデル: GATAN K2 QUANTUM (4k x 4k) 撮影したグリッド数: 1 / 実像数: 3674 |
| 電子光学装置 | エネルギーフィルター名称: GIF Bioquantum / エネルギーフィルタースリット幅: 15 eV |
| 画像スキャン | サンプリングサイズ: 14 µm / 横: 3710 / 縦: 3838 / 動画フレーム数/画像: 45 |
- 解析
解析
| ソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| EMソフトウェア |
| |||||||||||||||||||||||||||||||||||||||||||||
| CTF補正 | タイプ: PHASE FLIPPING AND AMPLITUDE CORRECTION | |||||||||||||||||||||||||||||||||||||||||||||
| 粒子像の選択 | 選択した粒子像数: 1448191 | |||||||||||||||||||||||||||||||||||||||||||||
| 対称性 | 点対称性: C2 (2回回転対称) | |||||||||||||||||||||||||||||||||||||||||||||
| 3次元再構成 | 解像度: 3.42 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 粒子像の数: 151898 / アルゴリズム: FOURIER SPACE / クラス平均像の数: 1 / 対称性のタイプ: POINT | |||||||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | B value: 76 / プロトコル: BACKBONE TRACE / 空間: REAL / Target criteria: Correlation coefficient | |||||||||||||||||||||||||||||||||||||||||||||
| 原子モデル構築 | PDB-ID: 5VRF | |||||||||||||||||||||||||||||||||||||||||||||
| 精密化 | 交差検証法: NONE 立体化学のターゲット値: GeoStd + Monomer Library + CDL v1.2 | |||||||||||||||||||||||||||||||||||||||||||||
| 原子変位パラメータ | Biso mean: 81.71 Å2 | |||||||||||||||||||||||||||||||||||||||||||||
| 拘束条件 |
|
 ムービー
ムービー コントローラー
コントローラー








 PDBj
PDBj




