+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Assimilatory NADPH-dependent sulfite reductase minimal dimer | |||||||||
 マップデータ マップデータ | main map | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | sulfite reductase / hemoflavoprotein / oxidoreductase / cryo-EM / FLAVOPROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報sulfite reductase (ferredoxin) activity / assimilatory sulfite reductase (NADPH) / sulfite reductase (NADPH) activity / sulfite reductase complex (NADPH) / sulfate assimilation / hydrogen sulfide biosynthetic process / cysteine biosynthetic process / FMN binding / flavin adenine dinucleotide binding / NADP binding ...sulfite reductase (ferredoxin) activity / assimilatory sulfite reductase (NADPH) / sulfite reductase (NADPH) activity / sulfite reductase complex (NADPH) / sulfate assimilation / hydrogen sulfide biosynthetic process / cysteine biosynthetic process / FMN binding / flavin adenine dinucleotide binding / NADP binding / 4 iron, 4 sulfur cluster binding / heme binding / metal ion binding / cytosol 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.78 Å | |||||||||
 データ登録者 データ登録者 | Ghazi Esfahani B / Walia N / Neselu K / Aragon M / Askenasy I / Wei A / Mendez JH / Stroupe ME | |||||||||
| 資金援助 |  米国, 2件 米国, 2件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2025 ジャーナル: Nat Commun / 年: 2025タイトル: Structure of dimerized assimilatory NADPH-dependent sulfite reductase reveals the minimal interface for diflavin reductase binding. 著者: Behrouz Ghazi Esfahani / Nidhi Walia / Kasahun Neselu / Yashika Garg / Mahira Aragon / Isabel Askenasy / Hui Alex Wei / Joshua H Mendez / M Elizabeth Stroupe /   要旨: Escherichia coli NADPH-dependent assimilatory sulfite reductase (SiR) reduces sulfite by six electrons to make sulfide for incorporation into sulfur-containing biomolecules. SiR has two subunits: an ...Escherichia coli NADPH-dependent assimilatory sulfite reductase (SiR) reduces sulfite by six electrons to make sulfide for incorporation into sulfur-containing biomolecules. SiR has two subunits: an NADPH, FMN, and FAD-binding diflavin flavoprotein and a siroheme/FeS cluster-containing hemoprotein. The molecular interactions that govern subunit binding have been unknown since the discovery of SiR over 50 years ago because SiR is flexible, thus has been intransigent for traditional high-resolution structural analysis. We use a combination of the chameleon® plunging system with a fluorinated lipid to overcome the challenges of preserving a flexible molecule to determine a 2.78 Å-resolution cryo-EM structure of a minimal heterodimer complex. Chameleon®, combined with the fluorinated lipid, overcomes persistent denaturation at the air-water interface. Using a previously characterized minimal heterodimer reduces the heterogeneity of a structurally heterogeneous complex to a level that we analyze using multi-conformer cryo-EM image analysis algorithms. Here, we report the near-atomic resolution structure of the flavoprotein/hemoprotein complex, revealing how they interact in a minimal interface. Further, we determine the structural elements that discriminate between pairing a hemoprotein with a diflavin reductase, as in the E. coli homolog, or a ferredoxin partner, as in maize (Zea mays). | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_45359.map.gz emd_45359.map.gz | 168 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-45359-v30.xml emd-45359-v30.xml emd-45359.xml emd-45359.xml | 51 KB 51 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_45359_fsc.xml emd_45359_fsc.xml | 11.8 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_45359.png emd_45359.png | 70.9 KB | ||
| Filedesc metadata |  emd-45359.cif.gz emd-45359.cif.gz | 8 KB | ||
| その他 |  emd_45359_additional_1.map.gz emd_45359_additional_1.map.gz emd_45359_additional_10.map.gz emd_45359_additional_10.map.gz emd_45359_additional_11.map.gz emd_45359_additional_11.map.gz emd_45359_additional_12.map.gz emd_45359_additional_12.map.gz emd_45359_additional_2.map.gz emd_45359_additional_2.map.gz emd_45359_additional_3.map.gz emd_45359_additional_3.map.gz emd_45359_additional_4.map.gz emd_45359_additional_4.map.gz emd_45359_additional_5.map.gz emd_45359_additional_5.map.gz emd_45359_additional_6.map.gz emd_45359_additional_6.map.gz emd_45359_additional_7.map.gz emd_45359_additional_7.map.gz emd_45359_additional_8.map.gz emd_45359_additional_8.map.gz emd_45359_additional_9.map.gz emd_45359_additional_9.map.gz emd_45359_half_map_1.map.gz emd_45359_half_map_1.map.gz emd_45359_half_map_2.map.gz emd_45359_half_map_2.map.gz | 111.4 MB 48.5 MB 48.6 MB 48.6 MB 131.7 MB 48.7 MB 48.8 MB 48.8 MB 48.7 MB 48.7 MB 48.6 MB 48.5 MB 165.3 MB 165.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-45359 http://ftp.pdbj.org/pub/emdb/structures/EMD-45359 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-45359 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-45359 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_45359_validation.pdf.gz emd_45359_validation.pdf.gz | 863.5 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_45359_full_validation.pdf.gz emd_45359_full_validation.pdf.gz | 863.1 KB | 表示 | |
| XML形式データ |  emd_45359_validation.xml.gz emd_45359_validation.xml.gz | 20.6 KB | 表示 | |
| CIF形式データ |  emd_45359_validation.cif.gz emd_45359_validation.cif.gz | 26.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-45359 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-45359 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-45359 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-45359 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  9c91MC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_45359.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_45359.map.gz / 形式: CCP4 / 大きさ: 125 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | main map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.765 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
+追加マップ: map with the linker
+追加マップ: vol 7 gauss z.mrc
+追加マップ: vol 8 gauss z.mrc
+追加マップ: vol 9 gauss z.mrc
+追加マップ: dimer obtained from the SiRFPdelta-SiRHP dataset
+追加マップ: vol 0 gauss z.mrc
+追加マップ: vol 1 gauss z.mrc
+追加マップ: vol 2 gauss z.mrc
+追加マップ: vol 3 gauss z.mrc
+追加マップ: vol 4 gauss z.mrc
+追加マップ: vol 5 gauss z.mrc
+追加マップ: vol 6 gauss z.mrc
+ハーフマップ: half map A
+ハーフマップ: half map B
- 試料の構成要素
試料の構成要素
-全体 : sulfite reductase minimal dimer
| 全体 | 名称: sulfite reductase minimal dimer |
|---|---|
| 要素 |
|
-超分子 #1: sulfite reductase minimal dimer
| 超分子 | 名称: sulfite reductase minimal dimer / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 124 KDa |
-分子 #1: Sulfite reductase [NADPH] flavoprotein alpha-component
| 分子 | 名称: Sulfite reductase [NADPH] flavoprotein alpha-component タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO / EC番号: assimilatory sulfite reductase (NADPH) |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 64.093684 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGGSHHHHHH GMASMTGGNN MGRDLYDDDD KDRWGSELEI TIISASQTGN ARRVAEALRD DLLAAKLNVK LVNAGDYKFK QIASEKLLI VVTSTQGCGE PPEEAVALHK FLFSKKAPKL ENTAFAVFSL GDSSYEFFTQ SGKDFDSKLA ELGGERLLDR V DADVEYQA ...文字列: MGGSHHHHHH GMASMTGGNN MGRDLYDDDD KDRWGSELEI TIISASQTGN ARRVAEALRD DLLAAKLNVK LVNAGDYKFK QIASEKLLI VVTSTQGCGE PPEEAVALHK FLFSKKAPKL ENTAFAVFSL GDSSYEFFTQ SGKDFDSKLA ELGGERLLDR V DADVEYQA AASEWRARVV DALKSRAPVA APSQSVATGA VNEIHTSPYS KDAPLVASLS VNQKITGRNS EKDVRHIEID LG DSGLRYQ PGDALGVWYQ NDPALVKELV ELLWLKGDEP VTVEGKTLPL NEALQWHFEL TVNTANIVEN YATLTRSETL LPL VGDKAK LQHYAATTPI VDMVRFSPAQ LDAEALINLL RPLTPRLYSI ASSQAEVENE VHVTVGVVRY DVEGRARAGG ASSF LADRV EEEGEVRVFI EHNDNFRLPA NPETPVIMIG PGTGIAPFRA FMQQRAADEA PGKNWLFFGN PHFTEDFLYQ VEWQR YVKE GVLTRIDLAW SRDQKEKVYV QDKLREQGAE LWRWINDGAH IYVSGDACRM AKDVEQALLE VIAEFGGMDT EAADEF LSE LRVERRYQRD VY UniProtKB: Sulfite reductase [NADPH] flavoprotein alpha-component |
-分子 #2: Sulfite reductase [NADPH] hemoprotein beta-component
| 分子 | 名称: Sulfite reductase [NADPH] hemoprotein beta-component タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO / EC番号: assimilatory sulfite reductase (NADPH) |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 64.091102 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MSEKHPGPLV VEGKLTDAER MKHESNYLRG TIAEDLNDGL TGGFKGDNFL LIRFHGMYQQ DDRDIRAERA EQKLEPRHAM LLRCRLPGG VITTKQWQAI DKFAGENTIY GSIRLTNRQT FQFHGILKKN VKPVHQMLHS VGLDALATAN DMNRNVLCTS N PYESQLHA ...文字列: MSEKHPGPLV VEGKLTDAER MKHESNYLRG TIAEDLNDGL TGGFKGDNFL LIRFHGMYQQ DDRDIRAERA EQKLEPRHAM LLRCRLPGG VITTKQWQAI DKFAGENTIY GSIRLTNRQT FQFHGILKKN VKPVHQMLHS VGLDALATAN DMNRNVLCTS N PYESQLHA EAYEWAKKIS EHLLPRTRAY AEIWLDQEKV ATTDEEPILG QTYLPRKFKT TVVIPPQNDI DLHANDMNFV AI AENGKLV GFNLLVGGGL SIEHGNKKTY ARTASEFGYL PLEHTLAVAE AVVTTQRDWG NRTDRKNAKT KYTLERVGVE TFK AEVERR AGIKFEPIRP YEFTGRGDRI GWVKGIDDNW HLTLFIENGR ILDYPARPLK TGLLEIAKIH KGDFRITANQ NLII AGVPE SEKAKIEKIA KESGLMNAVT PQRENSMACV SFPTCPLAMA EAERFLPSFI DNIDNLMAKH GVSDEHIVMR VTGCP NGCG RAMLAEVGLV GKAPGRYNLH LGGNRIGTRI PRMYKENITE PEILASLDEL IGRWAKEREA GEGFGDFTVR AGIIRP VLD PARDLWD UniProtKB: Sulfite reductase [NADPH] hemoprotein beta-component |
-分子 #3: FLAVIN-ADENINE DINUCLEOTIDE
| 分子 | 名称: FLAVIN-ADENINE DINUCLEOTIDE / タイプ: ligand / ID: 3 / コピー数: 1 / 式: FAD |
|---|---|
| 分子量 | 理論値: 785.55 Da |
| Chemical component information |  ChemComp-FAD: |
-分子 #4: FLAVIN MONONUCLEOTIDE
| 分子 | 名称: FLAVIN MONONUCLEOTIDE / タイプ: ligand / ID: 4 / コピー数: 1 / 式: FMN |
|---|---|
| 分子量 | 理論値: 456.344 Da |
| Chemical component information |  ChemComp-FMN: |
-分子 #5: PHOSPHATE ION
| 分子 | 名称: PHOSPHATE ION / タイプ: ligand / ID: 5 / コピー数: 1 / 式: PO4 |
|---|---|
| 分子量 | 理論値: 94.971 Da |
| Chemical component information |  ChemComp-PO4: |
-分子 #6: POTASSIUM ION
| 分子 | 名称: POTASSIUM ION / タイプ: ligand / ID: 6 / コピー数: 1 / 式: K |
|---|---|
| 分子量 | 理論値: 39.098 Da |
-分子 #7: IRON/SULFUR CLUSTER
| 分子 | 名称: IRON/SULFUR CLUSTER / タイプ: ligand / ID: 7 / コピー数: 1 / 式: SF4 |
|---|---|
| 分子量 | 理論値: 351.64 Da |
| Chemical component information | 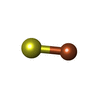 ChemComp-FS1: |
-分子 #8: SIROHEME
| 分子 | 名称: SIROHEME / タイプ: ligand / ID: 8 / コピー数: 1 / 式: SRM |
|---|---|
| 分子量 | 理論値: 916.661 Da |
| Chemical component information |  ChemComp-SRM: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 10 mg/mL |
|---|---|
| 緩衝液 | pH: 6.8 |
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: DIRECT ELECTRON APOLLO (4k x 4k) 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 3.0 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー






 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)





































































































































