+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM structure of the mammalian peptide transporter PepT2 bound to cefadroxil | |||||||||||||||
 マップデータ マップデータ | unsharpened map | |||||||||||||||
 試料 試料 |
| |||||||||||||||
 キーワード キーワード | protein-coupled peptide transporter / peptide transport / antibiotics / MEMBRANE PROTEIN | |||||||||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報high-affinity oligopeptide transmembrane transporter activity / tripeptide import across plasma membrane / dipeptide transport / peptidoglycan transport / tripeptide transmembrane transporter activity / dipeptide import across plasma membrane / oligopeptide transport / peptide:proton symporter activity / metanephric proximal tubule development / dipeptide transmembrane transporter activity ...high-affinity oligopeptide transmembrane transporter activity / tripeptide import across plasma membrane / dipeptide transport / peptidoglycan transport / tripeptide transmembrane transporter activity / dipeptide import across plasma membrane / oligopeptide transport / peptide:proton symporter activity / metanephric proximal tubule development / dipeptide transmembrane transporter activity / antibacterial innate immune response / regulation of nucleotide-binding domain, leucine rich repeat containing receptor signaling pathway / xenobiotic transport / renal absorption / phagocytic vesicle membrane / protein transport / apical plasma membrane / membrane / plasma membrane 類似検索 - 分子機能 | |||||||||||||||
| 生物種 |   | |||||||||||||||
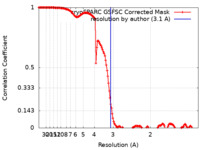
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.1 Å | |||||||||||||||
 データ登録者 データ登録者 | Parker JL / Deme JC / Lea SM / Newstead S | |||||||||||||||
| 資金援助 |  英国, 英国,  米国, 4件 米国, 4件
| |||||||||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Structural basis for antibiotic transport and inhibition in PepT2. 著者: Joanne L Parker / Justin C Deme / Simon M Lichtinger / Gabriel Kuteyi / Philip C Biggin / Susan M Lea / Simon Newstead /   要旨: The uptake and elimination of beta-lactam antibiotics in the human body are facilitated by the proton-coupled peptide transporters PepT1 (SLC15A1) and PepT2 (SLC15A2). The mechanism by which SLC15 ...The uptake and elimination of beta-lactam antibiotics in the human body are facilitated by the proton-coupled peptide transporters PepT1 (SLC15A1) and PepT2 (SLC15A2). The mechanism by which SLC15 family transporters recognize and discriminate between different drug classes and dietary peptides remains unclear, hampering efforts to improve antibiotic pharmacokinetics through targeted drug design and delivery. Here, we present cryo-EM structures of the proton-coupled peptide transporter, PepT2 from Rattus norvegicus, in complex with the widely used beta-lactam antibiotics cefadroxil, amoxicillin and cloxacillin. Our structures, combined with pharmacophore mapping, molecular dynamics simulations and biochemical assays, establish the mechanism of beta-lactam antibiotic recognition and the important role of protonation in drug binding and transport. | |||||||||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_44599.map.gz emd_44599.map.gz | 307.1 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-44599-v30.xml emd-44599-v30.xml emd-44599.xml emd-44599.xml | 21.1 KB 21.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_44599_fsc.xml emd_44599_fsc.xml | 14.6 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_44599.png emd_44599.png | 129 KB | ||
| マスクデータ |  emd_44599_msk_1.map emd_44599_msk_1.map | 325 MB |  マスクマップ マスクマップ | |
| Filedesc metadata |  emd-44599.cif.gz emd-44599.cif.gz | 6.5 KB | ||
| その他 |  emd_44599_additional_1.map.gz emd_44599_additional_1.map.gz emd_44599_additional_2.map.gz emd_44599_additional_2.map.gz emd_44599_half_map_1.map.gz emd_44599_half_map_1.map.gz emd_44599_half_map_2.map.gz emd_44599_half_map_2.map.gz | 161.7 MB 2.2 MB 301.6 MB 301.6 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-44599 http://ftp.pdbj.org/pub/emdb/structures/EMD-44599 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-44599 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-44599 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_44599_validation.pdf.gz emd_44599_validation.pdf.gz | 991.2 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_44599_full_validation.pdf.gz emd_44599_full_validation.pdf.gz | 990.8 KB | 表示 | |
| XML形式データ |  emd_44599_validation.xml.gz emd_44599_validation.xml.gz | 23.8 KB | 表示 | |
| CIF形式データ |  emd_44599_validation.cif.gz emd_44599_validation.cif.gz | 31 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-44599 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-44599 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-44599 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-44599 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|---|
| 「今月の分子」の関連する項目 |
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_44599.map.gz / 形式: CCP4 / 大きさ: 325 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_44599.map.gz / 形式: CCP4 / 大きさ: 325 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
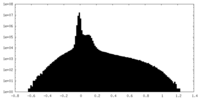
| 注釈 | unsharpened map | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.693 Å | ||||||||||||||||||||||||||||||||||||
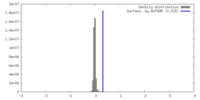
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-マスク #1
| ファイル |  emd_44599_msk_1.map emd_44599_msk_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
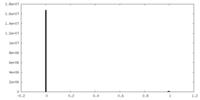
| 投影像・断面図 |
| ||||||||||||
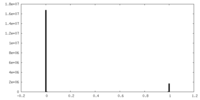
| 密度ヒストグラム |
-追加マップ: unsharpened map
| ファイル | emd_44599_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
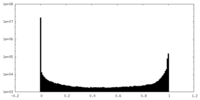
| 注釈 | unsharpened map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
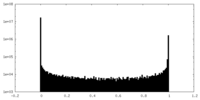
| 密度ヒストグラム |
-追加マップ: unsharpened map
| ファイル | emd_44599_additional_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | unsharpened map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
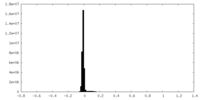
| 密度ヒストグラム |
-ハーフマップ: unsharpened map
| ファイル | emd_44599_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
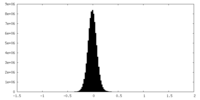
| 注釈 | unsharpened map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: unsharpened map
| ファイル | emd_44599_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | unsharpened map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Complex of the mammalian peptide transporter PepT2 with nanobody ...
| 全体 | 名称: Complex of the mammalian peptide transporter PepT2 with nanobody and bound cefadroxil |
|---|---|
| 要素 |
|
-超分子 #1: Complex of the mammalian peptide transporter PepT2 with nanobody ...
| 超分子 | 名称: Complex of the mammalian peptide transporter PepT2 with nanobody and bound cefadroxil タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1-#2 |
|---|---|
| 由来(天然) | 生物種:  |
-超分子 #2: PepT2
| 超分子 | 名称: PepT2 / タイプ: complex / ID: 2 / 親要素: 1 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  |
-超分子 #3: nanobody
| 超分子 | 名称: nanobody / タイプ: complex / ID: 3 / 親要素: 1 / 含まれる分子: #2 |
|---|---|
| 由来(天然) | 生物種:  |
-分子 #1: Solute carrier family 15 member 2
| 分子 | 名称: Solute carrier family 15 member 2 / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 82.477766 KDa |
| 組換発現 | 生物種:  Homo sapiens (ヒト) Homo sapiens (ヒト) |
| 配列 | 文字列: MNPFQKNESK ETLFSPVSTE EMLPRPPSPP KKSPPKIFGS SYPVSIAFIV VNEFCERFSY YGMKAVLTLY FLYFLHWNED TSTSVYHAF SSLCYFTPIL GAAIADSWLG KFKTIIYLSL VYVLGHVFKS LGAIPILGGK MLHTILSLVG LSLIALGTGG I KPCVAAFG ...文字列: MNPFQKNESK ETLFSPVSTE EMLPRPPSPP KKSPPKIFGS SYPVSIAFIV VNEFCERFSY YGMKAVLTLY FLYFLHWNED TSTSVYHAF SSLCYFTPIL GAAIADSWLG KFKTIIYLSL VYVLGHVFKS LGAIPILGGK MLHTILSLVG LSLIALGTGG I KPCVAAFG GDQFEEEHAE ARTRYFSVFY LAINAGSLIS TFITPMLRGD VKCFGQDCYA LAFGVPGLLM VLALVVFAMG SK MYRKPPP EGNIVAQVIK CIWFALCNRF RNRSGDLPKR QHWLDWAAEK YPKHLIADVK ALTRVLFLYI PLPMFWALLD QQG SRWTLQ ANKMNGDLGF FVLQPDQMQV LNPFLVLIFI PLFDLVIYRL ISKCRINFSS LRKMAVGMIL ACLAFAVAAL VETK INGMI HPQPASQEIF LQVLNLADGD VKVTVLGSRN NSLLVESVSS FQNTTHYSKL HLEAKSQDLH FHLKYNSLSV HNDHS VEEK NCYQLLIHQD GESISSMLVK DTGIKPANGM AAIRFINTLH KDLNISLDTD APLSVGKDYG VSAYRTVLRG KYPAVH CET EDKVFSLDLG QLDFGTTYLF VITNITSQGL QAWKAEDIPV NKLSIAWQLP QYVLVTAAEV MFSVTGLEFS YSQAPSS MK SVLQAAWLLT VAVGNIIVLV VAQFSGLAQW AEFVLFSCLL LVVCLIFSVM AYYYVPLKSE DTREATDKQI PAVQGNMI N LETKNTRLVE GENLYFQ UniProtKB: Solute carrier family 15 member 2 |
-分子 #2: nanobody
| 分子 | 名称: nanobody / タイプ: protein_or_peptide / ID: 2 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 14.494183 KDa |
| 配列 | 文字列: GPSQVQLVES GGGLVQPGGS LRLLCVASGR PFNDYDMGWF RQAPGKEREF VASISWSGRV TDYSDSMKGR CTVSRDNAKG TMFLQMSNL VPRDTAVYYC AAARRRWTFK ATNTEEFYET WGQGTQVTVS SA |
-分子 #3: Cefadroxil
| 分子 | 名称: Cefadroxil / タイプ: ligand / ID: 3 / コピー数: 1 / 式: A1APP |
|---|---|
| 分子量 | 理論値: 363.388 Da |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: FEI FALCON IV (4k x 4k) 平均電子線量: 54.8 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 2.5 µm / 最小 デフォーカス(公称値): 0.8 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー















 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)