+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Cryo-EM reconstruction of Staphylococcus aureus oleate hydratase (OhyA) dimer with a disordered C-terminal membrane-association domain | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | oleate hydratase (OhyA) / phospholipids / membrane binding domain / amphipathic helices / interfacial enzyme / peripheral membrane protein / HYDROLASE | |||||||||
| 機能・相同性 | oleate hydratase / oleate hydratase activity / Oleate hydratase / MCRA family / FAD binding / fatty acid metabolic process / FAD/NAD(P)-binding domain superfamily / Myosin-cross-reactive antigen 機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  | |||||||||
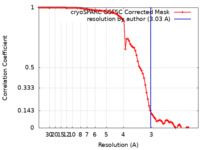
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.03 Å | |||||||||
 データ登録者 データ登録者 | Oldham ML / Qayyum MZ | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: J Biol Chem / 年: 2024 ジャーナル: J Biol Chem / 年: 2024タイトル: The carboxy terminus causes interfacial assembly of oleate hydratase on a membrane bilayer. 著者: Christopher D Radka / Christy R Grace / Hale S Hasdemir / Yupeng Li / Carlos C Rodriguez / Patrick Rodrigues / Michael L Oldham / M Zuhaib Qayyum / Aaron Pitre / William J MacCain / Ravi C ...著者: Christopher D Radka / Christy R Grace / Hale S Hasdemir / Yupeng Li / Carlos C Rodriguez / Patrick Rodrigues / Michael L Oldham / M Zuhaib Qayyum / Aaron Pitre / William J MacCain / Ravi C Kalathur / Emad Tajkhorshid / Charles O Rock /  要旨: The soluble flavoprotein oleate hydratase (OhyA) hydrates the 9-cis double bond of unsaturated fatty acids. OhyA substrates are embedded in membrane bilayers; OhyA must remove the fatty acid from the ...The soluble flavoprotein oleate hydratase (OhyA) hydrates the 9-cis double bond of unsaturated fatty acids. OhyA substrates are embedded in membrane bilayers; OhyA must remove the fatty acid from the bilayer and enclose it in the active site. Here, we show that the positively charged helix-turn-helix motif in the carboxy terminus (CTD) is responsible for interacting with the negatively charged phosphatidylglycerol (PG) bilayer. Super-resolution microscopy of Staphylococcus aureus cells expressing green fluorescent protein fused to OhyA or the CTD sequence shows subcellular localization along the cellular boundary, indicating OhyA is membrane-associated and the CTD sequence is sufficient for membrane recruitment. Using cryo-electron microscopy, we solved the OhyA dimer structure and conducted 3D variability analysis of the reconstructions to assess CTD flexibility. Our surface plasmon resonance experiments corroborated that OhyA binds the PG bilayer with nanomolar affinity and we found the CTD sequence has intrinsic PG binding properties. We determined that the nuclear magnetic resonance structure of a peptide containing the CTD sequence resembles the OhyA crystal structure. We observed intermolecular NOE from PG liposome protons next to the phosphate group to the CTD peptide. The addition of paramagnetic MnCl indicated the CTD peptide binds the PG surface but does not insert into the bilayer. Molecular dynamics simulations, supported by site-directed mutagenesis experiments, identify key residues in the helix-turn-helix that drive membrane association. The data show that the OhyA CTD binds the phosphate layer of the PG surface to obtain bilayer-embedded unsaturated fatty acids. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_42484.map.gz emd_42484.map.gz | 33.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-42484-v30.xml emd-42484-v30.xml emd-42484.xml emd-42484.xml | 21.5 KB 21.5 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_42484_fsc.xml emd_42484_fsc.xml | 8.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_42484.png emd_42484.png | 93 KB | ||
| Filedesc metadata |  emd-42484.cif.gz emd-42484.cif.gz | 6.8 KB | ||
| その他 |  emd_42484_additional_1.map.gz emd_42484_additional_1.map.gz emd_42484_half_map_1.map.gz emd_42484_half_map_1.map.gz emd_42484_half_map_2.map.gz emd_42484_half_map_2.map.gz | 59.7 MB 62.1 MB 62.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-42484 http://ftp.pdbj.org/pub/emdb/structures/EMD-42484 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-42484 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-42484 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_42484_validation.pdf.gz emd_42484_validation.pdf.gz | 879.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_42484_full_validation.pdf.gz emd_42484_full_validation.pdf.gz | 879.2 KB | 表示 | |
| XML形式データ |  emd_42484_validation.xml.gz emd_42484_validation.xml.gz | 16.5 KB | 表示 | |
| CIF形式データ |  emd_42484_validation.cif.gz emd_42484_validation.cif.gz | 21 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-42484 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-42484 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-42484 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-42484 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_42484.map.gz / 形式: CCP4 / 大きさ: 67 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_42484.map.gz / 形式: CCP4 / 大きさ: 67 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.044 Å | ||||||||||||||||||||||||||||||||||||
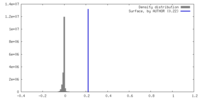
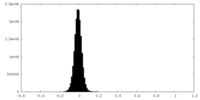
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-追加マップ: DeepEMhancer map
| ファイル | emd_42484_additional_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | DeepEMhancer map | ||||||||||||
| 投影像・断面図 |
| ||||||||||||
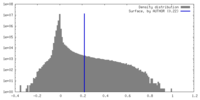
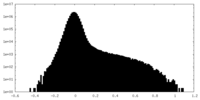
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_42484_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
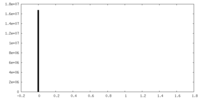
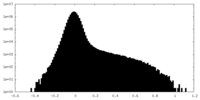
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_42484_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
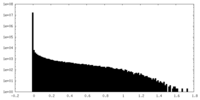
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Homodimer of OhyA
| 全体 | 名称: Homodimer of OhyA |
|---|---|
| 要素 |
|
-超分子 #1: Homodimer of OhyA
| 超分子 | 名称: Homodimer of OhyA / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 139.343 KDa |
-分子 #1: Oleate hydratase
| 分子 | 名称: Oleate hydratase / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 69.892719 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MGSSHHHHHH SSGLVPRGSH MYYSYGNYEA FARPKKPENV ENKSAYLIGS GLASLAAACF LIRDGQMEGS KIHILEELPK AGGSLDGEN MPLKGYVVRG GREMENHFEC LWDLFRSIPS LEIDNASVLD EFYWLNKEDP NYSRCRVIEK QGQRLVTDGD F TLTKTAIK ...文字列: MGSSHHHHHH SSGLVPRGSH MYYSYGNYEA FARPKKPENV ENKSAYLIGS GLASLAAACF LIRDGQMEGS KIHILEELPK AGGSLDGEN MPLKGYVVRG GREMENHFEC LWDLFRSIPS LEIDNASVLD EFYWLNKEDP NYSRCRVIEK QGQRLVTDGD F TLTKTAIK EILDLCLTNE EDLDDVKITD VFSDDFFNSN FWIYWKTMFA FEPWHSAMEM RRYLMRFVHH ISGLADFSAL KF TKYNQYE SLVLPMVEYL KSHGVQFEYD VKVEDIKIDV TTSQKIAREI LIDRNGNAES IKLTINDLVF VTNGSITESS TYG DNDTPA PPTDELGGSW TLWKNLARQS PEFGNPDKFC QNIPKKSWFV SATSTTNNKE IIDTIESICK RDPLAGKTVT GGII TINDS AWQMSFTINR QQQFKDQPEN EISTWIYALY SDVNGDYIKK PITECSGNEI CQEWLYHLGV STDKIEDLAK HASNT IPVY MPYITSYFMT RAIGDRPLVV PHQSQNLAFI GNFAETERDT VFTTEYSVRT AMEAVYQLLN IDRGIPEVIN SPFDLR VLM DAIYELNDHQ DLREITKDSK MQKLALAGFL KKIKGTYIES LLKEHKLL UniProtKB: Myosin-cross-reactive antigen |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3 mg/mL | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.3 構成要素:
| ||||||||||||
| グリッド | モデル: UltrAuFoil R1.2/1.3 / 材質: GOLD / メッシュ: 300 / 支持フィルム - 材質: GOLD / 支持フィルム - トポロジー: HOLEY | ||||||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 283 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TALOS ARCTICA |
|---|---|
| 温度 | 最高: 100.0 K |
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 検出モード: SUPER-RESOLUTION / 撮影したグリッド数: 1 / 実像数: 3248 / 平均露光時間: 3.0 sec. / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 200 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 50.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 2.0 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 79000 |
| 試料ステージ | 試料ホルダーモデル: FEI TITAN KRIOS AUTOGRID HOLDER ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Talos Arctica / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Source name: PDB / Chain - Initial model type: experimental model / 詳細: initial model was a crystal structure |
|---|---|
| 精密化 | 空間: REAL / プロトコル: RIGID BODY FIT |
| 得られたモデル |  PDB-8ur6: |
 ムービー
ムービー コントローラー
コントローラー











 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)