+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Klebsiella pneumoniae encapsulin-associated DyP peroxidase | |||||||||
 マップデータ マップデータ | Klebsiella pneumoniae encapsulin-associated DyP peroxidase | |||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | DyP peroxidase / encapsulin / OXIDOREDUCTASE | |||||||||
| 生物種 |  Klebsiella pneumoniae (肺炎桿菌) Klebsiella pneumoniae (肺炎桿菌) | |||||||||
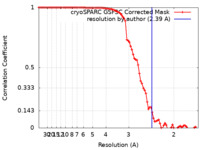
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.39 Å | |||||||||
 データ登録者 データ登録者 | Andreas MP / Jones JA / Giessen TW | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nat Commun / 年: 2024 ジャーナル: Nat Commun / 年: 2024タイトル: Structural basis for peroxidase encapsulation inside the encapsulin from the Gram-negative pathogen Klebsiella pneumoniae. 著者: Jesse A Jones / Michael P Andreas / Tobias W Giessen /  要旨: Encapsulins are self-assembling protein nanocompartments capable of selectively encapsulating dedicated cargo proteins, including enzymes involved in iron storage, sulfur metabolism, and stress ...Encapsulins are self-assembling protein nanocompartments capable of selectively encapsulating dedicated cargo proteins, including enzymes involved in iron storage, sulfur metabolism, and stress resistance. They represent a unique compartmentalization strategy used by many pathogens to facilitate specialized metabolic capabilities. Encapsulation is mediated by specific cargo protein motifs known as targeting peptides (TPs), though the structural basis for encapsulation of the largest encapsulin cargo class, dye-decolorizing peroxidases (DyPs), is currently unknown. Here, we characterize a DyP-containing encapsulin from the enterobacterial pathogen Klebsiella pneumoniae. By combining cryo-electron microscopy with TP and TP-binding site mutagenesis, we elucidate the molecular basis for cargo encapsulation. TP binding is mediated by cooperative hydrophobic and ionic interactions as well as shape complementarity. Our results expand the molecular understanding of enzyme encapsulation inside protein nanocompartments and lay the foundation for rationally modulating encapsulin cargo loading for biomedical and biotechnological applications. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_41904.map.gz emd_41904.map.gz | 59.7 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-41904-v30.xml emd-41904-v30.xml emd-41904.xml emd-41904.xml | 18.8 KB 18.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_41904_fsc.xml emd_41904_fsc.xml | 8.4 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_41904.png emd_41904.png | 129.9 KB | ||
| Filedesc metadata |  emd-41904.cif.gz emd-41904.cif.gz | 6.5 KB | ||
| その他 |  emd_41904_half_map_1.map.gz emd_41904_half_map_1.map.gz emd_41904_half_map_2.map.gz emd_41904_half_map_2.map.gz | 59.3 MB 59.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-41904 http://ftp.pdbj.org/pub/emdb/structures/EMD-41904 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-41904 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-41904 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_41904_validation.pdf.gz emd_41904_validation.pdf.gz | 927.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_41904_full_validation.pdf.gz emd_41904_full_validation.pdf.gz | 927.2 KB | 表示 | |
| XML形式データ |  emd_41904_validation.xml.gz emd_41904_validation.xml.gz | 16.3 KB | 表示 | |
| CIF形式データ |  emd_41904_validation.cif.gz emd_41904_validation.cif.gz | 21 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41904 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41904 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41904 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41904 | HTTPS FTP |
-関連構造データ
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_41904.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_41904.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Klebsiella pneumoniae encapsulin-associated DyP peroxidase | ||||||||||||||||||||||||||||||||||||
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.832 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: Half Map B
| ファイル | emd_41904_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half Map B | ||||||||||||
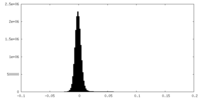
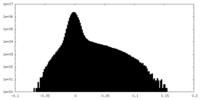
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: Half Map A
| ファイル | emd_41904_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 注釈 | Half Map A | ||||||||||||
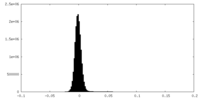
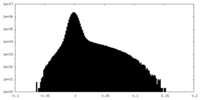
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Klebsiella pneumoniae family 1 encapsulin-associated DyP peroxidase
| 全体 | 名称: Klebsiella pneumoniae family 1 encapsulin-associated DyP peroxidase |
|---|---|
| 要素 |
|
-超分子 #1: Klebsiella pneumoniae family 1 encapsulin-associated DyP peroxidase
| 超分子 | 名称: Klebsiella pneumoniae family 1 encapsulin-associated DyP peroxidase タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: #1 |
|---|---|
| 由来(天然) | 生物種:  Klebsiella pneumoniae (肺炎桿菌) Klebsiella pneumoniae (肺炎桿菌) |
| 分子量 | 理論値: 240 KDa |
-分子 #1: Family 1 encapsulin-associated DyP peroxidase
| 分子 | 名称: Family 1 encapsulin-associated DyP peroxidase / タイプ: protein_or_peptide / ID: 1 詳細: Residues 1-352 are K.p. DyP peroxidase (NCBI: WP_193221875.1). Residues 1-2 and 316-352 are disordered. Residues 353-370 are a TEV protease site, linker, and HIS-tag that are disordered in the structure. コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Klebsiella pneumoniae (肺炎桿菌) Klebsiella pneumoniae (肺炎桿菌) |
| 分子量 | 理論値: 40.691395 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MACPISQSVS QPVDERLTRA AIFLVVTINP GKAAEVAVRT LCGTLSSLVR GVGFRILDGG LSCVMGVSSG GWERLFGDEK PEYLHVFQE INGVHHAPST PGDLLFHIRA ARMDLCFELA SRILSDLGSS VCVVDSVQGF RYFDDRDLLG FVDGTENPVA Q AAVDATLI ...文字列: MACPISQSVS QPVDERLTRA AIFLVVTINP GKAAEVAVRT LCGTLSSLVR GVGFRILDGG LSCVMGVSSG GWERLFGDEK PEYLHVFQE INGVHHAPST PGDLLFHIRA ARMDLCFELA SRILSDLGSS VCVVDSVQGF RYFDDRDLLG FVDGTENPVA Q AAVDATLI GEEDHTFSGG SYVIVQKYLH DLDKWNAIPV EQQEKIIGRE KLSDIELKDA DKPSYAHNVL TSIEEDGEDV DI LRDNMPF GDPGKGEFGT YFIGYSRKPA RIERMLENMF VGNPPGNYDR ILDVSRAITG TLFFIPTVSF LDSVEPQPSV SQQ TDDAKY IYDSPGTKGE SGSLNIGSLK KEVQDEENLY FQGGSGGHHH HHHH |
-分子 #2: Mesoheme
| 分子 | 名称: Mesoheme / タイプ: ligand / ID: 2 / コピー数: 1 / 式: MH0 |
|---|---|
| 分子量 | 理論値: 620.519 Da |
| Chemical component information |  ChemComp-MH0: |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 0.45 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
詳細: 20 mM Tris pH 7.5, 150 mM NaCl | |||||||||
| グリッド | モデル: Quantifoil R2/1 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. / 前処理 - 雰囲気: AIR / 詳細: 60 seconds at 5 mA | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV / 詳細: Blot force: 5 Blot time: 2 seconds. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) 検出モード: COUNTING / デジタル化 - サイズ - 横: 5760 pixel / デジタル化 - サイズ - 縦: 4092 pixel / 撮影したグリッド数: 1 / 実像数: 2468 / 平均露光時間: 1.89747 sec. / 平均電子線量: 50.02 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.8 µm / 最小 デフォーカス(公称値): 0.8 µm / 倍率(公称値): 105000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
+ 画像解析
画像解析
-原子モデル構築 1
| 初期モデル | PDB ID: Chain - Source name: Other / Chain - Initial model type: in silico model 詳細: An AlphaFill model containing bound heme was used as starting model |
|---|---|
| 詳細 | Initial fitting was performed using ChimeraX v1.2.5. The model was then manually refined and mutated using Coot v9.8.1 followed by real-space refinement using Phenix v1.20.1-4487-000. |
| 精密化 | 空間: REAL / プロトコル: FLEXIBLE FIT / 温度因子: 107.7 当てはまり具合の基準: Cross-correlation coefficient |
| 得られたモデル |  PDB-8u4z: |
 ムービー
ムービー コントローラー
コントローラー








 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)