[日本語] English
 万見
万見- EMDB-41078: Acinetobacter baumannii 118362 family 2A cargo-loaded encapsulin shell -
+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Acinetobacter baumannii 118362 family 2A cargo-loaded encapsulin shell | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | encapsulin / virus like particle / protein nanocompartment | |||||||||
| 機能・相同性 | :  機能・相同性情報 機能・相同性情報 | |||||||||
| 生物種 |  Acinetobacter baumannii 118362 (バクテリア) Acinetobacter baumannii 118362 (バクテリア) | |||||||||
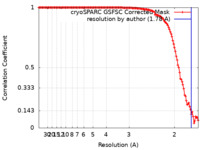
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 1.78 Å | |||||||||
 データ登録者 データ登録者 | Andreas MP / Benisch R / Giessen TW | |||||||||
| 資金援助 |  米国, 1件 米国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Sci Adv / 年: 2024 ジャーナル: Sci Adv / 年: 2024タイトル: A widespread bacterial protein compartment sequesters and stores elemental sulfur. 著者: Robert Benisch / Michael P Andreas / Tobias W Giessen /  要旨: Subcellular compartments often serve to store nutrients or sequester labile or toxic compounds. As bacteria mostly do not possess membrane-bound organelles, they often have to rely on protein-based ...Subcellular compartments often serve to store nutrients or sequester labile or toxic compounds. As bacteria mostly do not possess membrane-bound organelles, they often have to rely on protein-based compartments. Encapsulins are one of the most prevalent protein-based compartmentalization strategies found in prokaryotes. Here, we show that desulfurase encapsulins can sequester and store large amounts of crystalline elemental sulfur. We determine the 1.78-angstrom cryo-EM structure of a 24-nanometer desulfurase-loaded encapsulin. Elemental sulfur crystals can be formed inside the encapsulin shell in a desulfurase-dependent manner with l-cysteine as the sulfur donor. Sulfur accumulation can be influenced by the concentration and type of sulfur source in growth medium. The selectively permeable protein shell allows the storage of redox-labile elemental sulfur by excluding cellular reducing agents, while encapsulation substantially improves desulfurase activity and stability. These findings represent an example of a protein compartment able to accumulate and store elemental sulfur. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_41078.map.gz emd_41078.map.gz | 204.2 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-41078-v30.xml emd-41078-v30.xml emd-41078.xml emd-41078.xml | 17.7 KB 17.7 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_41078_fsc.xml emd_41078_fsc.xml | 12.5 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_41078.png emd_41078.png | 174.4 KB | ||
| Filedesc metadata |  emd-41078.cif.gz emd-41078.cif.gz | 6.2 KB | ||
| その他 |  emd_41078_half_map_1.map.gz emd_41078_half_map_1.map.gz emd_41078_half_map_2.map.gz emd_41078_half_map_2.map.gz | 198.3 MB 198.3 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-41078 http://ftp.pdbj.org/pub/emdb/structures/EMD-41078 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-41078 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-41078 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_41078_validation.pdf.gz emd_41078_validation.pdf.gz | 1.1 MB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_41078_full_validation.pdf.gz emd_41078_full_validation.pdf.gz | 1.1 MB | 表示 | |
| XML形式データ |  emd_41078_validation.xml.gz emd_41078_validation.xml.gz | 21.6 KB | 表示 | |
| CIF形式データ |  emd_41078_validation.cif.gz emd_41078_validation.cif.gz | 27.7 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41078 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41078 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41078 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-41078 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8t6rMC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_41078.map.gz / 形式: CCP4 / 大きさ: 216 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_41078.map.gz / 形式: CCP4 / 大きさ: 216 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ボクセルのサイズ | X=Y=Z: 0.84 Å | ||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_41078_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_41078_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : Acinetobacter baumannii 118362 family 2A cargo-loaded encapsulin shell
| 全体 | 名称: Acinetobacter baumannii 118362 family 2A cargo-loaded encapsulin shell |
|---|---|
| 要素 |
|
-超分子 #1: Acinetobacter baumannii 118362 family 2A cargo-loaded encapsulin shell
| 超分子 | 名称: Acinetobacter baumannii 118362 family 2A cargo-loaded encapsulin shell タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all 詳細: Acinetinobacter baumannii 118362 family 2A encapsulin shell with internal cysteine desulfurase cargo protein |
|---|---|
| 由来(天然) | 生物種:  Acinetobacter baumannii 118362 (バクテリア) Acinetobacter baumannii 118362 (バクテリア) |
| 分子量 | 理論値: 1.88 MDa |
-分子 #1: Major membrane protein I
| 分子 | 名称: Major membrane protein I / タイプ: protein_or_peptide / ID: 1 / コピー数: 1 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  Acinetobacter baumannii 118362 (バクテリア) Acinetobacter baumannii 118362 (バクテリア) |
| 分子量 | 理論値: 34.609195 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MAKNTDKAQL ALGDHAARQL ANATKTAPQL STITPRWLTH LLQWIPVEAG IYRLNRVNNT DDIQVACTQR DEATLPQTFV DYAPEPREY FLNGVSTVLD VHTRVADLYS SPHDQIKEQL RLTIETIKER QESELINNPE YGLLASVTDD QRISTLNGPP T PDDLDDLL ...文字列: MAKNTDKAQL ALGDHAARQL ANATKTAPQL STITPRWLTH LLQWIPVEAG IYRLNRVNNT DDIQVACTQR DEATLPQTFV DYAPEPREY FLNGVSTVLD VHTRVADLYS SPHDQIKEQL RLTIETIKER QESELINNPE YGLLASVTDD QRISTLNGPP T PDDLDDLL RKVWKEPGFF LAHPDAIAAF GRECTRRGVP PPTVSLFGSQ FITWRGIPLI PSNKIPVEDG KTKILLLRVG EK RQGIVGL FQPGLAGEQS PGLSVRFMGI NRNAIASYLI SLYCSLAVLT DDALAVLDDV EVDKYHDYPV NYK UniProtKB: UNIPROTKB: A0A009HA42 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 濃度 | 3 mg/mL | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 緩衝液 | pH: 7.5 構成要素:
詳細: 150 mM NaCl, 20 mM Tris pH 7.5 | |||||||||
| グリッド | モデル: Quantifoil R1.2/1.3 / 材質: COPPER / メッシュ: 200 / 支持フィルム - 材質: CARBON / 支持フィルム - トポロジー: HOLEY / 前処理 - タイプ: GLOW DISCHARGE / 前処理 - 時間: 60 sec. / 前処理 - 雰囲気: AIR / 詳細: 60 seconds at 5 mA | |||||||||
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 295 K / 装置: FEI VITROBOT MARK IV 詳細: Blot force: 20 Blot time: 4 seconds Drain time: 0 Wait time: 0. |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | TFS KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 BIOQUANTUM (6k x 4k) デジタル化 - サイズ - 横: 5760 pixel / デジタル化 - サイズ - 縦: 4092 pixel / 撮影したグリッド数: 1 / 実像数: 5936 / 平均露光時間: 3.0 sec. / 平均電子線量: 54.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | C2レンズ絞り径: 100.0 µm / 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / Cs: 2.7 mm / 最大 デフォーカス(公称値): 1.0 µm / 最小 デフォーカス(公称値): 0.5 µm / 倍率(公称値): 105000 |
| 試料ステージ | ホルダー冷却材: NITROGEN |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー



 Z
Z Y
Y X
X