+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of EBV LMP1 dimer | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | EBV latent membrane protein 1 / VIRAL PROTEIN | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報symbiont-mediated activation of host NF-kappaB cascade / transformation of host cell by virus / symbiont-mediated suppression of host JAK-STAT cascade via inhibition of host TYK2 activity / symbiont-mediated suppression of host type I interferon-mediated signaling pathway / virus-mediated perturbation of host defense response / host cell plasma membrane / membrane 類似検索 - 分子機能 | |||||||||
| 生物種 |  human gammaherpesvirus 4 (ヘルペスウイルス) human gammaherpesvirus 4 (ヘルペスウイルス) | |||||||||
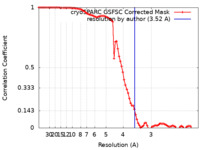
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 3.52 Å | |||||||||
 データ登録者 データ登録者 | Gao P / Huang JF | |||||||||
| 資金援助 | 1件
| |||||||||
 引用 引用 |  ジャーナル: Cell / 年: 2024 ジャーナル: Cell / 年: 2024タイトル: Assembly and activation of EBV latent membrane protein 1. 著者: Jiafeng Huang / Xiaolin Zhang / Xiaohua Nie / Xuyuan Zhang / Yong Wang / Linlong Huang / Xiaohan Geng / Dong Li / Liguo Zhang / Guangxia Gao / Pu Gao /  要旨: Latent membrane protein 1 (LMP1) is the primary oncoprotein of Epstein-Barr virus (EBV) and plays versatile roles in the EBV life cycle and pathogenesis. Despite decades of extensive research, the ...Latent membrane protein 1 (LMP1) is the primary oncoprotein of Epstein-Barr virus (EBV) and plays versatile roles in the EBV life cycle and pathogenesis. Despite decades of extensive research, the molecular basis for LMP1 folding, assembly, and activation remains unclear. Here, we report cryo-electron microscopy structures of LMP1 in two unexpected assemblies: a symmetric homodimer and a higher-order filamentous oligomer. LMP1 adopts a non-canonical and unpredicted fold that supports the formation of a stable homodimer through tight and antiparallel intermolecular packing. LMP1 dimers further assemble side-by-side into higher-order filamentous oligomers, thereby allowing the accumulation and specific organization of the flexible cytoplasmic tails for efficient recruitment of downstream factors. Super-resolution microscopy and cellular functional assays demonstrate that mutations at both dimeric and oligomeric interfaces disrupt LMP1 higher-order assembly and block multiple LMP1-mediated signaling pathways. Our research provides a framework for understanding the mechanism of LMP1 and for developing potential therapies targeting EBV-associated diseases. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_38342.map.gz emd_38342.map.gz | 59.6 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-38342-v30.xml emd-38342-v30.xml emd-38342.xml emd-38342.xml | 12.8 KB 12.8 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| FSC (解像度算出) |  emd_38342_fsc.xml emd_38342_fsc.xml | 8.4 KB | 表示 |  FSCデータファイル FSCデータファイル |
| 画像 |  emd_38342.png emd_38342.png | 42.2 KB | ||
| Filedesc metadata |  emd-38342.cif.gz emd-38342.cif.gz | 5 KB | ||
| その他 |  emd_38342_half_map_1.map.gz emd_38342_half_map_1.map.gz emd_38342_half_map_2.map.gz emd_38342_half_map_2.map.gz | 59.4 MB 59.4 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-38342 http://ftp.pdbj.org/pub/emdb/structures/EMD-38342 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-38342 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-38342 | HTTPS FTP |
-検証レポート
| 文書・要旨 |  emd_38342_validation.pdf.gz emd_38342_validation.pdf.gz | 794.6 KB | 表示 |  EMDB検証レポート EMDB検証レポート |
|---|---|---|---|---|
| 文書・詳細版 |  emd_38342_full_validation.pdf.gz emd_38342_full_validation.pdf.gz | 794.2 KB | 表示 | |
| XML形式データ |  emd_38342_validation.xml.gz emd_38342_validation.xml.gz | 16.2 KB | 表示 | |
| CIF形式データ |  emd_38342_validation.cif.gz emd_38342_validation.cif.gz | 20.8 KB | 表示 | |
| アーカイブディレクトリ |  https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-38342 https://ftp.pdbj.org/pub/emdb/validation_reports/EMD-38342 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-38342 ftp://ftp.pdbj.org/pub/emdb/validation_reports/EMD-38342 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8xh6MC  8xh7C M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_38342.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_38342.map.gz / 形式: CCP4 / 大きさ: 64 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 1.04 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #2
| ファイル | emd_38342_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #1
| ファイル | emd_38342_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : LMP1 dimer
| 全体 | 名称: LMP1 dimer |
|---|---|
| 要素 |
|
-超分子 #1: LMP1 dimer
| 超分子 | 名称: LMP1 dimer / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  human gammaherpesvirus 4 (ヘルペスウイルス) human gammaherpesvirus 4 (ヘルペスウイルス) |
-分子 #1: Latent membrane protein 1
| 分子 | 名称: Latent membrane protein 1 / タイプ: protein_or_peptide / ID: 1 / コピー数: 2 / 光学異性体: LEVO |
|---|---|
| 由来(天然) | 生物種:  human gammaherpesvirus 4 (ヘルペスウイルス) human gammaherpesvirus 4 (ヘルペスウイルス) |
| 分子量 | 理論値: 18.729418 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: SIGLALLLLL LALLFWLYIV MSNWTGGALL VLYSFALMLI IIILIIFIFR RDLLCPLGGL GLLLLMITLL LIALWNLHGQ ALYLGIVLF IFGCLLVLGL WIYFLEILWR LGATIWQLLA FILAFFLAII LLIIALYLQQ NWWTLLVDLL WLLLFMAILI W MY UniProtKB: Latent membrane protein 1 |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 7.5 |
|---|---|
| 凍結 | 凍結剤: ETHANE |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K2 SUMMIT (4k x 4k) 平均電子線量: 60.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.8 µm / 最小 デフォーカス(公称値): 1.2 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
 ムービー
ムービー コントローラー
コントローラー





 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)