+ データを開く
データを開く
- 基本情報
基本情報
| 登録情報 |  | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| タイトル | Structure of Gabija GajA | |||||||||
 マップデータ マップデータ | ||||||||||
 試料 試料 |
| |||||||||
 キーワード キーワード | Anti-Phage / IMMUNE SYSTEM | |||||||||
| 機能・相同性 |  機能・相同性情報 機能・相同性情報endonuclease activity / defense response to virus / 加水分解酵素; エステル加水分解酵素 / hydrolase activity / metal ion binding 類似検索 - 分子機能 | |||||||||
| 生物種 |  | |||||||||
| 手法 | 単粒子再構成法 / クライオ電子顕微鏡法 / 解像度: 2.66 Å | |||||||||
 データ登録者 データ登録者 | Li J / Wang Z / Wang L | |||||||||
| 資金援助 |  中国, 1件 中国, 1件
| |||||||||
 引用 引用 |  ジャーナル: Nature / 年: 2024 ジャーナル: Nature / 年: 2024タイトル: Structures and activation mechanism of the Gabija anti-phage system. 著者: Jing Li / Rui Cheng / Zhiming Wang / Wuliu Yuan / Jun Xiao / Xinyuan Zhao / Xinran Du / Shiyu Xia / Lianrong Wang / Bin Zhu / Longfei Wang /   要旨: Prokaryotes have evolved intricate innate immune systems against phage infection. Gabija is a highly widespread prokaryotic defence system that consists of two components, GajA and GajB. GajA ...Prokaryotes have evolved intricate innate immune systems against phage infection. Gabija is a highly widespread prokaryotic defence system that consists of two components, GajA and GajB. GajA functions as a DNA endonuclease that is inactive in the presence of ATP. Here, to explore how the Gabija system is activated for anti-phage defence, we report its cryo-electron microscopy structures in five states, including apo GajA, GajA in complex with DNA, GajA bound by ATP, apo GajA-GajB, and GajA-GajB in complex with ATP and Mg. GajA is a rhombus-shaped tetramer with its ATPase domain clustered at the centre and the topoisomerase-primase (Toprim) domain located peripherally. ATP binding at the ATPase domain stabilizes the insertion region within the ATPase domain, keeping the Toprim domain in a closed state. Upon ATP depletion by phages, the Toprim domain opens to bind and cleave the DNA substrate. GajB, which docks on GajA, is activated by the cleaved DNA, ultimately leading to prokaryotic cell death. Our study presents a mechanistic landscape of Gabija activation. | |||||||||
| 履歴 |
|
- 構造の表示
構造の表示
| 添付画像 |
|---|
- ダウンロードとリンク
ダウンロードとリンク
-EMDBアーカイブ
| マップデータ |  emd_36541.map.gz emd_36541.map.gz | 197.3 MB |  EMDBマップデータ形式 EMDBマップデータ形式 | |
|---|---|---|---|---|
| ヘッダ (付随情報) |  emd-36541-v30.xml emd-36541-v30.xml emd-36541.xml emd-36541.xml | 14.1 KB 14.1 KB | 表示 表示 |  EMDBヘッダ EMDBヘッダ |
| 画像 |  emd_36541.png emd_36541.png | 79.7 KB | ||
| Filedesc metadata |  emd-36541.cif.gz emd-36541.cif.gz | 5.4 KB | ||
| その他 |  emd_36541_half_map_1.map.gz emd_36541_half_map_1.map.gz emd_36541_half_map_2.map.gz emd_36541_half_map_2.map.gz | 194.1 MB 194.1 MB | ||
| アーカイブディレクトリ |  http://ftp.pdbj.org/pub/emdb/structures/EMD-36541 http://ftp.pdbj.org/pub/emdb/structures/EMD-36541 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-36541 ftp://ftp.pdbj.org/pub/emdb/structures/EMD-36541 | HTTPS FTP |
-関連構造データ
| 関連構造データ |  8jq9MC  8jqbC  8jqcC  8wy4C  8wy5C  8x51C  8x5iC  8x5nC M: このマップから作成された原子モデル C: 同じ文献を引用 ( |
|---|---|
| 類似構造データ | 類似検索 - 機能・相同性  F&H 検索 F&H 検索 |
- リンク
リンク
| EMDBのページ |  EMDB (EBI/PDBe) / EMDB (EBI/PDBe) /  EMDataResource EMDataResource |
|---|
- マップ
マップ
| ファイル |  ダウンロード / ファイル: emd_36541.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) ダウンロード / ファイル: emd_36541.map.gz / 形式: CCP4 / 大きさ: 209.3 MB / タイプ: IMAGE STORED AS FLOATING POINT NUMBER (4 BYTES) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 投影像・断面図 | 画像のコントロール
画像は Spider により作成 | ||||||||||||||||||||||||||||||||||||
| ボクセルのサイズ | X=Y=Z: 0.84 Å | ||||||||||||||||||||||||||||||||||||
| 密度 |
| ||||||||||||||||||||||||||||||||||||
| 対称性 | 空間群: 1 | ||||||||||||||||||||||||||||||||||||
| 詳細 | EMDB XML:
|
-添付データ
-ハーフマップ: #1
| ファイル | emd_36541_half_map_1.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
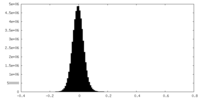
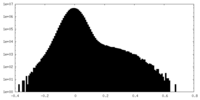
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
-ハーフマップ: #2
| ファイル | emd_36541_half_map_2.map | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
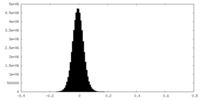
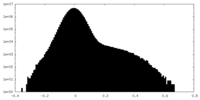
| 投影像・断面図 |
| ||||||||||||
| 密度ヒストグラム |
- 試料の構成要素
試料の構成要素
-全体 : GajA
| 全体 | 名称: GajA |
|---|---|
| 要素 |
|
-超分子 #1: GajA
| 超分子 | 名称: GajA / タイプ: complex / ID: 1 / 親要素: 0 / 含まれる分子: all |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 276 KDa |
-分子 #1: Endonuclease GajA
| 分子 | 名称: Endonuclease GajA / タイプ: protein_or_peptide / ID: 1 / コピー数: 4 / 光学異性体: LEVO EC番号: 加水分解酵素; エステル加水分解酵素 |
|---|---|
| 由来(天然) | 生物種:  |
| 分子量 | 理論値: 67.079469 KDa |
| 組換発現 | 生物種:  |
| 配列 | 文字列: MKFSNITIKN FRNFEKVNIN LDNKNVIFGM NDIGKTNFLY ALRFLLDKEI RKFGFNKSDY HKHDTSKKIE IILTLDLSNY EKDEDTKKL ISVVKGARTS ANADVFYIAL ESKYDDKELY GNIILKWGSE LDNLIDIPGR GNINALDNVF KVIYINPLVD L DKLFAQNK ...文字列: MKFSNITIKN FRNFEKVNIN LDNKNVIFGM NDIGKTNFLY ALRFLLDKEI RKFGFNKSDY HKHDTSKKIE IILTLDLSNY EKDEDTKKL ISVVKGARTS ANADVFYIAL ESKYDDKELY GNIILKWGSE LDNLIDIPGR GNINALDNVF KVIYINPLVD L DKLFAQNK KYIFEESQGN ESDEGILNNI KSLTDQVNQQ IGEMTIIKGF QQEITSEYRS LKKEEVSIEL KSEMAIKGFF SD IIPYIKK DGDSNYYPTS GDGRRKMLSY SIYNYLAKKK YEDKIVIYLI EEPEISLHRS MQIALSKQLF EQSTYKYFFL STH SPELLY EMDNTRLIRV HSTEKVVCSS HMYNVEEAYG SVKKKLNKAL SSALFAERVL LIEGPSEKIL FEKVLDEVEP EYEL NGGFL LEVGGTYFNH YVCTLNDLGI THIIKTDNDL KSKKGKKGVY ELLGLNRCLN LLGRENLDEI TIDIPEDIKG KKKKE RLNE RKKEIFKQYK NEVGEFLGER IYLSEIDLEN DLYSAIGESM KRIFENEDPV HYLQKSKLFN MVELVNNLST KDCFDV FEH EKFACLKELV GSDRG UniProtKB: Endonuclease GajA |
-実験情報
-構造解析
| 手法 | クライオ電子顕微鏡法 |
|---|---|
 解析 解析 | 単粒子再構成法 |
| 試料の集合状態 | particle |
- 試料調製
試料調製
| 緩衝液 | pH: 8 |
|---|---|
| 凍結 | 凍結剤: ETHANE / チャンバー内湿度: 100 % / チャンバー内温度: 8 K / 装置: FEI VITROBOT MARK IV |
- 電子顕微鏡法
電子顕微鏡法
| 顕微鏡 | FEI TITAN KRIOS |
|---|---|
| 撮影 | フィルム・検出器のモデル: GATAN K3 (6k x 4k) / 平均電子線量: 50.0 e/Å2 |
| 電子線 | 加速電圧: 300 kV / 電子線源:  FIELD EMISSION GUN FIELD EMISSION GUN |
| 電子光学系 | 照射モード: FLOOD BEAM / 撮影モード: BRIGHT FIELD / 最大 デフォーカス(公称値): 1.8 µm / 最小 デフォーカス(公称値): 1.6 µm |
| 実験機器 |  モデル: Titan Krios / 画像提供: FEI Company |
- 画像解析
画像解析
| 初期モデル | モデルのタイプ: INSILICO MODEL |
|---|---|
| 最終 再構成 | 解像度のタイプ: BY AUTHOR / 解像度: 2.66 Å / 解像度の算出法: FSC 0.143 CUT-OFF / 使用した粒子像数: 3023069 |
| 初期 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
| 最終 角度割当 | タイプ: MAXIMUM LIKELIHOOD |
-原子モデル構築 1
| 精密化 | 空間: REAL / プロトコル: AB INITIO MODEL |
|---|---|
| 得られたモデル |  PDB-8jq9: |
 ムービー
ムービー コントローラー
コントローラー











 Z (Sec.)
Z (Sec.) Y (Row.)
Y (Row.) X (Col.)
X (Col.)